
【题目】氨是一种重要的化工产品,也是重要的化工原料。某化学小组在实验室制备氨并完成相关性质实验。
(1)实验一:用如图所示装置制备并收集 NH3。
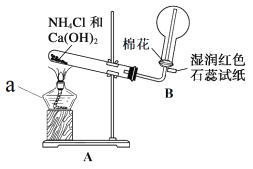
仪器 a 的名称为____________,装置 A 中产生 NH3 的化学方程式为____________, 装置 B 中用圆底烧瓶收集 NH3 的方法为____________(填“向上排空气法”或“向下 排空气法”),当湿润红色石蕊试纸颜色变为____________色,表示已经收集满 NH3。
(2)实验二:用如图所示装置进行 NH3 的喷泉实验。
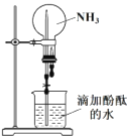
引发该喷泉实验的操作是先____________,再打开止水夹,使烧杯内的水通过导管进入烧瓶形成喷泉,说明 NH3 具有的物理性质是____________,烧瓶内溶液呈红色, 说明 NH3 的水溶液呈____________性。
【答案】酒精灯 Ca(OH)2 + 2NH4Cl= CaCl2+ 2NH3↑+ 2H2O 向下排空气法 蓝 挤压胶头滴管,将水挤入烧瓶 极易溶解于水 碱
【解析】
(1) 仪器 a 的名称为酒精灯,答案为酒精灯
装置 A 中产生 NH3 的化学方程式为:Ca(OH)2 + 2NH4Cl![]() CaCl2+ 2NH3↑+ 2H2O
CaCl2+ 2NH3↑+ 2H2O
答案为:Ca(OH)2 + 2NH4Cl![]() CaCl2+ 2NH3↑+ 2H2O
CaCl2+ 2NH3↑+ 2H2O
装置 B 中所用圆底烧瓶口向下,所以收集NH3的方法为向下排空气法。
答案为:向下排空气法
氨气溶于水后,所得溶液显碱性,能使湿润的红色石蕊试纸颜色变蓝色。所以当湿润红色石蕊试纸颜色变为蓝色时,表示已经收集满NH3。答案为:蓝
(2)引发喷泉的方法是设法减小烧瓶内气体的压强,所以可采用水溶减压法,即挤压胶头,让水进入烧瓶,氨气溶于水导致烧瓶内气体压强减小。
答案为:挤压胶头滴管,将水挤入烧瓶
打开止水夹,使烧杯内的水通过导管进入烧瓶形成喷泉,说明 NH3 具有的物理性质是极易溶于水。答案为:极易溶解于水
烧瓶内溶液呈红色, 说明NH3的水溶液呈碱性。答案为碱


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】羟氨![]() 在水溶液中的电离方程式为:
在水溶液中的电离方程式为:![]() ,用0.1mol/L盐酸滴定20mL 0.1mol/L
,用0.1mol/L盐酸滴定20mL 0.1mol/L![]() 溶液,恒定25℃时,滴定过程中由水电离出来的OHˉ浓度的负对数与盐酸体积的关系如图所示,下列说法错误的是( )
溶液,恒定25℃时,滴定过程中由水电离出来的OHˉ浓度的负对数与盐酸体积的关系如图所示,下列说法错误的是( )

A.B点对应的溶液中![]()
B.C点对应的溶液中![]()
C.A到C溶液中,![]() 电离常数不变
电离常数不变
D.由A到D,水电离出的![]() 先减小后增大
先减小后增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类冶炼最多的金属元素是_______;请写出它与水在一定条件反应的化学方程式________熔点最低的金属是_________;导电性最好的金属是_________;人体内最多的金属元素是_________;海水中含量最多的金属元素是_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化六氨合钴([Co(NH3)6]Cl3)是一种橙黄色晶体,实验室制备过程如下:
Ⅰ.将研细的6 g CoCl26H2O晶体和4 g NH4Cl固体加入锥形瓶中,加水,加热溶解,冷却;
Ⅱ.加入13.5 mL浓氨水,用活性炭作催化剂,混合均匀后逐滴滴加13.5 mL 5% H2O2溶液,水浴加热至50~60℃,保持20 min。用冰浴冷却,过滤,得粗产品;
Ⅲ.将粗产品溶于50 mL热的稀盐酸中,______,向滤液中缓慢加入6.7 mL浓盐酸,有大量橙黄色晶体析出,冰浴冷却后过滤;
Ⅳ.先用冷的2 mol·L1 HCl溶液洗涤晶体,再用少许乙醇洗涤,干燥,得产品。
(1)[Co(NH3)6]Cl3中Co的化合价是______。
(2)CoCl2遇浓氨水生成Co(OH)2沉淀,加入浓氨水前先加入NH4Cl可避免沉淀生成,原因是______。
(3)溶液中CoCl2、NH4Cl和浓氨水混合后,与H2O2溶液反应生成[Co(NH3)6]Cl3的化学方程式是______。
(4)补全Ⅲ中的操作:______。
(5)沉淀滴定法测定制备的产品中Cl-的质量分数:
ⅰ.准确称取a g Ⅳ中的产品,配制成100 mL溶液,移取25 mL溶液于锥形瓶中;
ⅱ.滴加少量0.005 mol·L1 K2CrO4溶液作为指示剂,用c mol·L1 AgNO3溶液滴定至终点;
ⅲ.平行测定三次,消耗AgNO3溶液的体积的平均值为v mL,计算晶体中Cl-的质量分数。
已知:溶解度:AgCl 1.3×106 mol·L1,Ag2CrO4(砖红色)6.5×105 mol·L1
①ⅱ中,滴定至终点的现象是______。
②制备的晶体中Cl-的质量分数是______(列计算式,Cl的相对原子质量:35.5)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于Na2CO3与NaHCO3的性质判断正确的是
A.常温下溶解度:Na2CO3<NaHCO3
B.与同浓度同体积的盐酸反应的速率:Na2CO3>NaHCO3
C.热稳定性:Na2CO3<NaHCO3
D.与澄清石灰水反应,均有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是

A.利用如图装置可制备Fe(OH)2
B.需要加热才能进行的化学反应一定是吸热反应
C.对铅蓄电池进形充电时,铅电极应连接外电源的正极
D.已知:H+(aq)+OH-(aq)=H2O(l) ΔH= -57.3 kJ·mol-1,若将1L 0.5mol·L-1盐酸与1L 0.55mol·L-1 NaOH的溶液混合,能放出28.65kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
A.如图表示反应2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0在有无催化剂时的能量变化
2SO3(g) ΔH<0在有无催化剂时的能量变化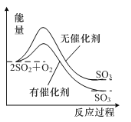
B.如图表示电解精炼铜时纯铜和粗铜的质量随时间的变化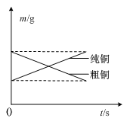
C.如图表示铅蓄电池放电时负极质量随转移电子物质的量的变化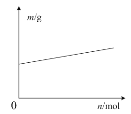
D.如图表示反应2NO2(g)![]() N2O4(g)和2NO2(g)
N2O4(g)和2NO2(g)![]() N2O4(l)的能量变化
N2O4(l)的能量变化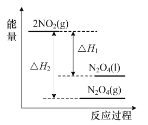
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氧化三铁俗称为磁性氧化铁,通常用作颜料、抛光剂和电讯器材等。某化学兴趣小组取磁性氧化铁进行铝热反应实验并对产物进行探究。
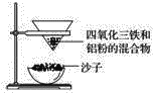
(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是__________。
(2)取少许反应生成的“铁块”溶于盐酸,滴加硫氰化钾溶液后溶液不变红,则______(填“能”或“不能”)说明“铁块”一定不含四氧化三铁,理由是_________。
(3)设计一个简单的实验方案,证明上述所得的“铁块”中含有金属铝,该实验所用的试剂是__________,反应的离子方程式为___________。
(4)请写出此铝热反应的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H2(g)+![]() O2(g)=H2O(g) ΔH1=akJ·mol1
O2(g)=H2O(g) ΔH1=akJ·mol1
②2H2(g)+O2(g)=2H2O(g) ΔH2=bkJ·mol1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=ckJ·mol1
O2(g)=H2O(l) ΔH3=ckJ·mol1
④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol1
下列关系式中正确的是
A.a<c<0B.b>d>0C.2a=b<0D.2c=d>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com