
【题目】根据要求回答下列问题。
①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧CO2
(1)写出Na2O2的电子式________,存在的化学键类型有________________。
(2)写出HClO电子式________________,写出CO2的结构式_______。
(3)含有共价键的离子化合物是_______(填序号)
(4)用电子式表示CaBr2的形成过程_________________________________ 。
【答案】![]() 离子键、非极性键(共价键)
离子键、非极性键(共价键) ![]() O=C=O ③⑤⑥
O=C=O ③⑤⑥ ![]()
【解析】
(1)Na2O2为离子化合物,含离子键、O-O非极性键;
(2)次氯酸是共价化合物,氯原子、氢原子分别与氧原子形成共价键,据此书写电子式,CO2的电子式为![]() ,据此书写结构式;
,据此书写结构式;
(3)一般来说,活泼金属与非金属形成离子键,非金属元素之间形成共价键,只含共价键的化合物为共价化合物,据此分析解答;
(4) CaBr2为离子化合物,只含离子键,据此书写CaBr2的形成过程。
(1)过氧化钠是离子化合物,由钠离子与过氧根离子构成,过氧化钠的电子式为![]() ,含离子键和O-O非极性共价键,故答案为:
,含离子键和O-O非极性共价键,故答案为:![]() ;离子键和非极性共价键;
;离子键和非极性共价键;
(2)HClO为共价化合物,电子式是![]() ,CO2的电子式为
,CO2的电子式为![]() ,结构式为O=C=O,故答案为:
,结构式为O=C=O,故答案为:![]() ;O=C=O;
;O=C=O;
(3)①CaBr2为离子化合物,只含离子键,②H2O为共价化合物,只含共价键,③NH4Cl为离子化合物,含离子键和共价键,④H2O2为共价化合物,只含共价键,⑤Na2O2为离子化合物,含离子键和共价键,⑥Ca(OH)2为离子化合物,含离子键和共价键,⑦HClO为共价化合物,只含共价键,⑧CO2为共价化合物,只含共价键,其中含有共价键的离子化合物是③⑤⑥,故答案为:③⑤⑥;
(4) CaBr2为离子化合物,只含离子键,CaBr2的形成过程用电子式表示为![]() ,故答案为:
,故答案为:![]() 。
。


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
【题目】中和热的测定实验(如图)。
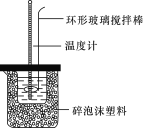
(1)量取反应物时,取50 mL 0.50 mol·L-1的盐酸,还应加入的试剂是________(填序号)。
A.50mL0.50mol·L-1NaOH溶液
B.50mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
(2)在实验过程中,该同学需要测定并记录的实验数据有_____________(填序号)。
A.盐酸的浓度
B.盐酸的温度
C.氢氧化钠溶液的浓度
D.氢氧化钠溶液的温度
E.水的比热容
F.溶液混合后的最高温度
(3)若用50 mL 0.5 mol·L-1醋酸溶液代替上述盐酸测定中和热,所得数据_____________(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,正确的是
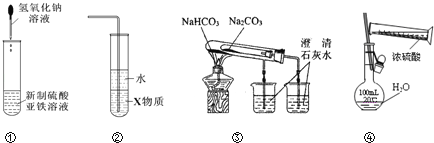
A.利用装置①可制备氢氧化亚铁并长时间观察其颜色
B.装置②中X若为四氯化碳,可用于吸收HCl气体,并防止倒吸
C.装置③验证Na2CO3和NaHCO3两种固体的热稳定性
D.通过④的方法配制一定浓度的稀硫酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的锌碘单液流电池,其原理如下图所示。下列说法不正确的是 ( )。
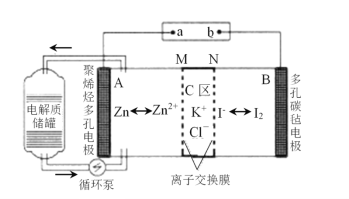
A.放电时B电极反应式为:I2+2e-=2I-
B.M为阳离子交换膜,N为阴离子交换膜
C.充电时,A极增重65g时,C区增加离子数为4NA
D.放电时电解质储罐中离子总浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K、Al、Cu、H、C、O、S、Cl是常见的八种元素。
(1)从明矾[KAl(SO4)2·12H2O]制备 Al、K2SO4和H2SO4的过程如下图所示:
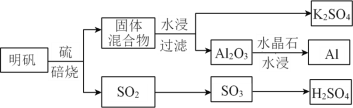
焙烧明矾的化学方程式为_________________________________________________。
(2)K位于元素周期表第________周期第________族。
(3)S的基态原子核外有________个未成对电子;Cl的基态原子核外电子排布式为____________。
(4)用“>”或“<”填空:
第一电离能 | 离子半径 | 熔点 | 酸性 |
O____S | Cl-____K+ | KCl____Al2O3 | H2SO4____HClO4 |
(5)SO2的价层电子对个数是________,该分子为结构为________;SO3中硫原子采用杂化方式为___________。
(6)新制备的Cu(OH)2可将乙醛氧化成乙酸,而自身还原成Cu2O。乙酸的沸点明显高于乙醛,其主要原因是____________________。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有________个铜原子。
(7)Al单质为面心立方晶体,其晶胞参数a=0.405 nm,列式表示Al单质的密度__________g·cm-3(列出计算式子,不必计算出结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是元素周期表中前18号某种金属元素对应的单质及其化合物之间的转化关系(“→”所指的转化都是一步完成)。
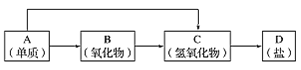
(1)若B为呼吸面具中的供氧剂,其供氧时每生成1molO2,反应过程中转移的电子数为_____,A与FeCl3溶液反应的离子方程式________________________。
(2)写出一个“C→D”转化的化学方程式_________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是葡萄酒中常用的抗氧化剂。一种以硫黄为原料制取Na2S2O5的生产工艺如下:
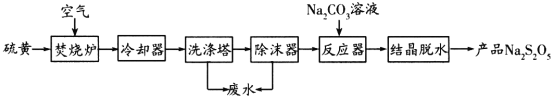
已知:结晶脱水发生的反应:![]()
回答下列问题:
(1)Na2S2O5中硫元素的化合价为________。
(2)焚烧炉中反应的化学方程式为________________。
(3)反应器中发生反应的离子方程式为________________。
(4)葡萄酒酿造过程中添加Na2S2O5会放出一种有刺激性气味的气体,该气体是一种食品添加剂。实验室中检验该气体的常用试剂是________________。
(5)废水中的硫单质(S8)能与碱反应,化学反应:![]() ,反应中氧化剂与还原剂的物质的量之比为________。
,反应中氧化剂与还原剂的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学小组在验证反应“![]() ”的实验中检测到Fe3+,发现和探究过程如下:
”的实验中检测到Fe3+,发现和探究过程如下:
向硝酸酸化的0.05mol·L-1硝酸银溶液(pH≈2)中加入过量铁粉,静置片刻,烧杯底部有黑色固体,溶液呈黄色。
(1)探究反应产物
①取上层清液,滴入酸性高锰酸钾溶液中,溶液紫色褪去,说明溶液中含有的离子是________(写化学式)。
②取少量黑色固体,洗涤后,加稀硝酸溶解固体,再加盐酸,观察到________,证明黑色固体中含有Ag。
(2)对“溶液呈黄色”进行探究
①甲认为溶液中有Fe3+;乙认为铁粉过量时不可能有Fe3+,乙的理由是________(用离子方程式表示)。
②对Fe3+产生的原因作出如下假设:
假设Ⅰ:空气中的O2将Fe2+氧化;
假设Ⅱ:酸性溶液中![]() 具有氧化性,将Fe2+氧化;
具有氧化性,将Fe2+氧化;
假设Ⅲ:溶液中的________将Fe2+氧化。
③实验验证:
ⅰ.向硝酸酸化的NaNO3溶液(pH≈2)中加入过量铁粉,搅拌后静置,取不同时间的上层清液滴加KSCN溶液,3min时溶液呈浅红色,30min后,溶液几乎无色。
ⅱ.向ⅰ中所得上层清液中加入________溶液,有黑色固体析出,向上层清液中滴加KSCN溶液,溶液变红。
④综合上述实验得知,假设________(填序号)正确,氧化Fe2+的离子方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.为探究硫酸铜晶体(CuSO4·xH2O)受热分解后所得产物,设计实验装置如图所示,部分实验现象为:A中蓝色晶体逐渐变成白色粉末,继续加热最终变成黑色;B中产生白色沉淀;D中溶液变成红色。(洗气瓶中试剂均足量)

(1)分析推测该硫酸铜晶体最终分解产物可能有_______________________________。
(2)D中的反应分两步进行,写出第一步反应的离子方程式_____________________。
II.测定硫酸铜晶体(CuSO4·xH2O)中结晶水x的值,实验装置和过程如下:取硫酸铜晶体7.23 g置于硬质试管中,先通N2排除体系内空气,酒精喷灯高温加热充分,待A中蓝色晶体最终变成黑色,停止加热,再次鼓入N2至装置冷却到室温。(洗气瓶中试剂均足量)
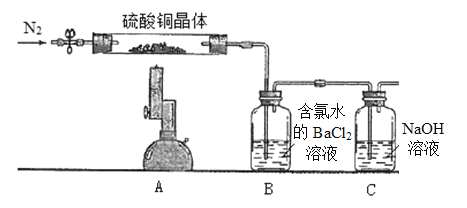
(1)取B中白色沉淀经过滤洗涤干燥称量得固体6.99 g,经计算可得CuSO4·xH2O中x=__________,再次鼓入N2的目的是____________________。
(2)某同学提出,要测定晶体中结晶水x的值,也可将B装置用装有浓硫酸的洗气瓶替换,最终测浓硫酸增重即可计算得到结果,评价该同学的方案是否可行?(如果不可行,请说明理由)_____________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com