
【题目】下列说法中正确的是
A.已知t1℃时,反应C+CO2![]() 2CO △H>0的速率为υ,若升高温度,逆反应速率减小
2CO △H>0的速率为υ,若升高温度,逆反应速率减小
B.恒压容器中发生反应N2+O2![]() 2NO,若在容器中充入He,正逆反应速率均不变
2NO,若在容器中充入He,正逆反应速率均不变
C.当一定量的锌粉和过量的6molL1盐酸反应时,为了减慢反应速率,又不影响产生H2的总量,可向反应器中加入少量的CuSO4溶液
D.待反应PCl5(g)![]() PCl3(g)+Cl2(g) 达到平衡后,保持温度和体积不变,再充PCl5(g)达到新的平衡,新平衡和原平衡相比PCl5(g)的转化率减少
PCl3(g)+Cl2(g) 达到平衡后,保持温度和体积不变,再充PCl5(g)达到新的平衡,新平衡和原平衡相比PCl5(g)的转化率减少
科目:高中化学 来源: 题型:
【题目】图为周期表中短周期的一部分,若R原子核外有3个未成对电子,说法正确的是

A.原子半径大小顺序是:Y>X>R
B.其气态氢化物的稳定性顺序是:Z>Y>X>R
C.X、Y、Z中Z的氧化物对应的水化物的酸性最强
D.R的气态氢化物与它的含氧酸之间能发生化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.101kPa时,2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1,则H2的燃烧热ΔH=-572kJ·mol-1
B.一定条件下发生反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4kJ·mol-1,此条件下将1.5mol H2和过量N2充分反应,放出热量46.2kJ
2NH3(g) ΔH=-92.4kJ·mol-1,此条件下将1.5mol H2和过量N2充分反应,放出热量46.2kJ
C.若将等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
D.已知:2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”是当今社会提出的一个新概念。在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%。在用丙炔合成甲基丙烯酸甲酯(![]() )的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物可以是
)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物可以是
A.CO和CH3OHB.CO2和H2OC.H2和COD.CH3OH和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为合成![]() 查阅资料得知一条合成路线:
查阅资料得知一条合成路线:

原料气CO的制备原理:HCOOH![]() CO↑+H2O,并设计出原料气的制备装置(如图)。
CO↑+H2O,并设计出原料气的制备装置(如图)。
(提示:甲酸(HCOOH)通常是一种无色易挥发的液体,它在浓硫酸作用下易分解)
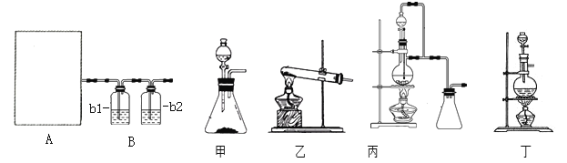
请完成下列问题:
(1)图A是利用甲酸制取CO的发生装置.根据实验原理,应选择图_____(填“甲”、“乙”、“丙”或“丁”);选择的理由是______________________。
(2)若用以上装置制备干燥纯净的CO,b1和b2中盛装的试剂分别是____________,_____。
(3)CO还可以和丙烯和氢气制取正丁醇,方程式如下:
CH3CH=CH2+CO+H2![]() CH3CH2CH2CHO
CH3CH2CH2CHO![]() CH3CH2CH2CH2OH;
CH3CH2CH2CH2OH;
在制取原料丙烯时,会产生少量SO2、CO2及水蒸气,某小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是_______(填序号)。
①2%品红溶液 ②溴水 ③石灰水 ④无水CuSO4 ⑤饱和Na2SO3溶液
(4)产物![]() 中往往会混有少量甲苯,为了制取较纯净的产物,该小组对这两种有机物的物理性质进行了查阅,资料如下:
中往往会混有少量甲苯,为了制取较纯净的产物,该小组对这两种有机物的物理性质进行了查阅,资料如下:
甲苯是无色透明液体,密度0.87,沸点:110.6℃,不溶于水,可混溶于苯等多数有机溶剂。无色或淡黄色透明液体,密度1.015,沸点204-205℃,微溶于水,易溶于醇、醚。通过这些资料,该小组设计了某些方法来进行产物的提纯,合理的是_________。
A 分液 B过滤 C蒸馏 D将甲苯氧化成苯甲酸再进行分液
(5)得到较纯净的产物之后,某位同学为了研究产物的化学性质,将产物和甲苯分别取样,并分别滴加溴水,发现溴水最终都褪色了,于是得出结论:产物和甲苯的化学性质相似。这位同学的结论是否正确?若不正确,请说明理由。_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯能在多种条件下发生水解反应:CH3COOC2H5+H2O![]() CH3COOH+C2H5OH。已知该反应的速率随c(H+)的增大而加快。下图为CH3COOC2H5的水解速率随时间的变化图。下列说法中正确的是
CH3COOH+C2H5OH。已知该反应的速率随c(H+)的增大而加快。下图为CH3COOC2H5的水解速率随时间的变化图。下列说法中正确的是

A. 图中A、B两点表示的c(CH3COOC2H5)相等
B. 反应初期水解速率增大可能是溶液中c(H+)逐渐增大所致
C. 图中t0时说明反应达到平衡状态
D. 图中tB时CH3COOC2H5的转化率等于tA时的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
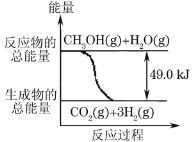
①CH3OH(g)+H2O(g)→CO2(g)+3H2(g) -49.0kJ
②CH3OH(g)+![]() O2(g)→CO2(g)+2H2(g)+192.9kJ
O2(g)→CO2(g)+2H2(g)+192.9kJ
下列说法正确的是( )
A.1molCH3OH完全燃烧放热192.9kJ
B.反应①中的能量变化如图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+![]() O2(g)→CO2(g)+2H2(g)+Q的Q<192.9kJ
O2(g)→CO2(g)+2H2(g)+Q的Q<192.9kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关平衡常数的说法中,正确的是 ( )
A. 改变条件,反应物的转化率增大,平衡常数也一定增大
B. 反应2NO2(g)![]() N2O4(g) △H <0,升高温度该反应平衡常数增大
N2O4(g) △H <0,升高温度该反应平衡常数增大
C. 对于给定可逆反应,温度一定时,其正、逆反应的平衡常数相等
D. CO2+H2 ![]() CO+H2O的平衡常数表达式为K==
CO+H2O的平衡常数表达式为K==![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某含Br—废水中提取Br2的过程包括:过滤、氧化、萃取(需选择合适萃取剂)及蒸馏等步骤。已知:
物质 | Br2 | CCl4 | 正十二烷 |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |
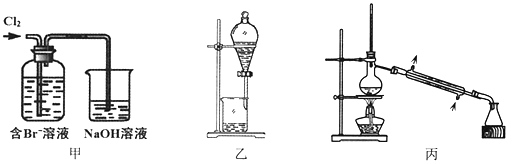
下列说法不正确的是
A. 甲装置中Br—发生的反应为:2Br-+ Cl2 = Br2 + 2Cl-
B. 甲装置中NaOH溶液每吸收0.1mol Cl2,转移0.1mol e—
C. 用乙装置进行萃取,溶解Br2的有机层在下层
D. 用丙装置进行蒸馏,先收集到的是Br2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com