
【题目】“绿色化学”是当今社会提出的一个新概念。在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%。在用丙炔合成甲基丙烯酸甲酯(![]() )的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物可以是
)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物可以是
A.CO和CH3OHB.CO2和H2OC.H2和COD.CH3OH和H2
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
【题目】I.硝酸钾用途广泛,工业上一般用复分解反应制取硝酸钾(相关物质的溶解度曲线见表)。以硝酸钠和氯化钾为原料制备硝酸钾的工艺流程如下:
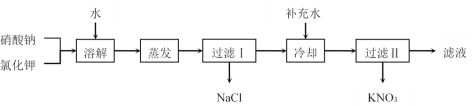

完成下列填空:
(1)为了加速固体溶解,可采取的措施有__________(至少写两种);实验室进行蒸发结晶操作时,为了防止液滴飞溅,进行的操作是_____________。
(2)过滤I所得滤液中含有的离子是________;过滤I所得滤液在进行冷却结晶前应补充少量水,目的是______________。
(3)检验产品KNO3中杂质的方法是________________。
II.实验室模拟工业上用氯化钾和硝酸铵为原料制取硝酸钾的过程如下:
取40 g NH4NO3和37.25 g KCl固体加入100 g水中,加热至90℃,固体溶解, 用冰水浴冷却至5℃以下,过滤(a)。在滤液中再加入NH4NO3,加热蒸发,当体积减小到约原来的![]() 时,保持70℃过滤(b),滤液可循环使用。完成下列填空:
时,保持70℃过滤(b),滤液可循环使用。完成下列填空:
(4)过滤(a)得到的固体物质主要是__________;在滤液中再加入NH4NO3的目的是________________________。
(5)为检测硝酸钾样品中铵盐含量,称取1.564 g样品,加入足量的NaOH浓溶液,充分加热,生成的气体用20.00 mL 0.102 mol/L H2SO4溶液全部吸收,滴定过量的H2SO4用去0.089 mol/L标准NaOH溶液16.55 mL。滴定过程中使用的指示剂是________;样品中含铵盐(以氯化铵计)的质量分数是___________(保留3位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以烯烃为原料可以合成多种高聚物的合成路线如下:
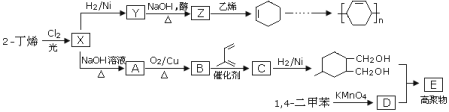
已知:烯烃和X2在一定条件下能发生取代,且能发生双烯合成如![]() 。
。
请回答下列问题:
(1)X中含有的官能团为_____________________________________;
(2)Y→Z的化学方程式为_____________________________;
(3)高聚物E的结构简式为____________________________;甲是A的一种同分异构体,其能实现转化:![]() ,甲的名称为________;
,甲的名称为________;
(4)由![]() 可以合成
可以合成![]() 。按合成路线的顺序,涉及反应的反应类型有:______________。
。按合成路线的顺序,涉及反应的反应类型有:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定CO2的相对分子质量,某实验小组三位同学选用含NaHCO3的样品(质量均为m1g)和其它合理的试剂,进行了以下三个实验。完成下列填空:
甲用重量法确定CO2的质量,装置如下图:
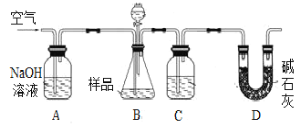
(1)B中反应的化学方程式为____________________________________________________。
(2)实验中持续缓缓通入空气,其作用之一是把生成的CO2全部排入后续装置中,使之完全被吸收;另有作用为___________________________________________________________。
(3)不能提高测定精确度的措施是___________。
a.向B内加入酸之前,排尽装置内的CO2气体
b.向B内滴加酸时不宜过快
c.在B、C之间增添盛有饱和NaHCO3溶液的洗气装置
d.在D后增添盛有碱石灰的干燥管
乙用滴定法确定CO2的物质的量,将样品配制成100mL溶液,从中取出20.00 mL,用c mol·L-1的盐酸滴定(甲基橙作指示剂)。当______________________________________________________时,停止滴定。平行测定三次,有关实验数据记录如下表。m1 g样品产生CO2的物质的量为_____________。
实验编号 | 待测液体积 (mL) | 消耗盐酸体积(mL) | |
初读数 | 末读数 | ||
1 | 20.00 | 0.00 | 25.02 |
2 | 20.00 | 0.20 | 28.80 |
3 | 20.00 | 1.30 | 26.28 |
丙用气体体积法确定CO2的体积,装置如图所示。

(4)为了减小实验误差,量气管中加入的液体X为___________________溶液;
(5)若该装置气密性良好,读数平视,但测得的“CO2体积”数据仍然偏小,其原因可能是____________________________________________________________________________。
(6)确定CO2的相对分子质量,选用___________________(限用“甲”、“乙”、“丙”进行填写)的实验数据为最佳。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下2L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如下表所示。下列说法正确的是( )
X | Y | W | |
n(起始状态)/mol | 2 | 1 | 0 |
n(平衡状态)/mol | 1 | 0.5 | 1.5 |
A.该温度下达平衡后,增大压强平衡不移动
B.该反应方程式可表示为:X+2Y=3W
C.升高温度,若W的体积分数减小,则此反应ΔH>0
D.恒温恒容时,增加X的物质的量,平衡向正向移动,X的转化率提高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组拟探究H+浓度对MnO2与H2O2反应速率的影响。现取等量MnO2和下表有关物质,在相同温度下进行4组实验,分别记录收集20.0mL氧气所需时间。
实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
水的体积/mL | 15 | 14.5 | V4 | 13.5 |
所需时间t/s | t1 | t2 | t3 | t4 |
已知酸性条件下时:MnO2+H2O2+2H+=Mn2++O2↑+2H2O
(1)实验Ⅰ发生反应的化学方程式为__,实验Ⅱ中MnO2的作用是__。
(2)上表中V1=__mL,V3=___mL。
(3)若实验测得t2>t3>t4,则可得出的实验结论是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.已知t1℃时,反应C+CO2![]() 2CO △H>0的速率为υ,若升高温度,逆反应速率减小
2CO △H>0的速率为υ,若升高温度,逆反应速率减小
B.恒压容器中发生反应N2+O2![]() 2NO,若在容器中充入He,正逆反应速率均不变
2NO,若在容器中充入He,正逆反应速率均不变
C.当一定量的锌粉和过量的6molL1盐酸反应时,为了减慢反应速率,又不影响产生H2的总量,可向反应器中加入少量的CuSO4溶液
D.待反应PCl5(g)![]() PCl3(g)+Cl2(g) 达到平衡后,保持温度和体积不变,再充PCl5(g)达到新的平衡,新平衡和原平衡相比PCl5(g)的转化率减少
PCl3(g)+Cl2(g) 达到平衡后,保持温度和体积不变,再充PCl5(g)达到新的平衡,新平衡和原平衡相比PCl5(g)的转化率减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数 (25 |
|
|
|
下列选项错误的是( )
A.CN + H2O + CO2 → HCN +HCO3﹣
B.2HCOOH + CO32﹣ → 2HCOO + H2O + CO2↑
C.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者
D.等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)抽烟对人体有害,烟草不完全燃烧产生的CO被吸进肺里跟血液中的血红蛋白(用Hb表示)化合,发生反应:CO+HbO2![]() O2+HbCO。实验表明,HbCO的浓度即使只有HbO2浓度的2%,也足以使人的智力受损。试回答:
O2+HbCO。实验表明,HbCO的浓度即使只有HbO2浓度的2%,也足以使人的智力受损。试回答:
①上述反应的平衡常数表达式为K=_____________________。
②抽烟后,吸入肺部的空气中测得的CO和O2的浓度分别为10-6 mol·L-1和10-2 mol·L-1。已知37℃时,平衡常数K=220,这时HbCO的浓度__________HbO2浓度的0.02倍(填“大于”“等于”、或“小于”)。
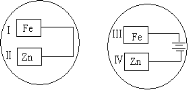
(2)把锌片和铁片放在盛有食盐水和酚酞的表面皿中,如图所示。最先观察到酚酞变红的现象的区域是________和__________。(填序号“I”“II”“III”或“IV”)
(3)一定条件下,在体积为3 L的密闭容器中,CO与H2反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
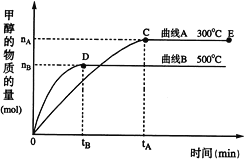
根据题意完成下列各题:
①反应达到平衡时,平衡常数表达式K=___________,升高温度,K值 ________________。(填“增大”、“减小”或“不变”)。
②在500 ℃,从反应开始到平衡,氢气的平均反应速率v (H2)=___________________。
③在其他条件不变的情况下,对处于E点的体系体积压缩到原来的![]() ,下列有关该体系的说法正确的是__________
,下列有关该体系的说法正确的是__________
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时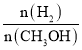 增大
增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com