
【题目】为测定CO2的相对分子质量,某实验小组三位同学选用含NaHCO3的样品(质量均为m1g)和其它合理的试剂,进行了以下三个实验。完成下列填空:
甲用重量法确定CO2的质量,装置如下图:
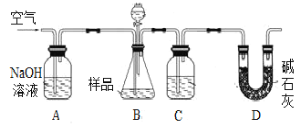
(1)B中反应的化学方程式为____________________________________________________。
(2)实验中持续缓缓通入空气,其作用之一是把生成的CO2全部排入后续装置中,使之完全被吸收;另有作用为___________________________________________________________。
(3)不能提高测定精确度的措施是___________。
a.向B内加入酸之前,排尽装置内的CO2气体
b.向B内滴加酸时不宜过快
c.在B、C之间增添盛有饱和NaHCO3溶液的洗气装置
d.在D后增添盛有碱石灰的干燥管
乙用滴定法确定CO2的物质的量,将样品配制成100mL溶液,从中取出20.00 mL,用c mol·L-1的盐酸滴定(甲基橙作指示剂)。当______________________________________________________时,停止滴定。平行测定三次,有关实验数据记录如下表。m1 g样品产生CO2的物质的量为_____________。
实验编号 | 待测液体积 (mL) | 消耗盐酸体积(mL) | |
初读数 | 末读数 | ||
1 | 20.00 | 0.00 | 25.02 |
2 | 20.00 | 0.20 | 28.80 |
3 | 20.00 | 1.30 | 26.28 |
丙用气体体积法确定CO2的体积,装置如图所示。

(4)为了减小实验误差,量气管中加入的液体X为___________________溶液;
(5)若该装置气密性良好,读数平视,但测得的“CO2体积”数据仍然偏小,其原因可能是____________________________________________________________________________。
(6)确定CO2的相对分子质量,选用___________________(限用“甲”、“乙”、“丙”进行填写)的实验数据为最佳。
【答案】2NaHCO3+H2SO4=Na2SO4+CO2↑+H2O 搅拌B、C中的反应物,使反应充分进行 c 滴入1滴盐酸,溶液刚好由黄色变橙色,且半分钟内不变色 0.125c mol 饱和碳酸氢钠 测定气体体积时水准管的液面高于量气管的液面或有CO2溶解在水中或其他合理的答案 甲和乙
【解析】
空气进入装置A中,氢氧化钠吸收空气中的二氧化碳,排除空气中的气体对实验的干扰;锥形瓶中发生碳酸氢钠与酸的反应,产生大量二氧化碳,持续缓缓通入空气,把生成的CO2全部排入后续装置中,经过装置C时,将制得的二氧化碳干燥,最后通入碱石灰中,通过碱石灰增重,计算生成二氧化碳的质量。
(1)B中发生碳酸氢钠与酸的反应,反应的化学方程式2NaHCO3+H2SO4=Na2SO4+CO2↑+H2O;
(2)装置A中的出气导管伸入装置B的液面以下,实验中持续缓缓通入空气,把生成的CO2全部排入后续装置中,使之完全被吸收;通过气体翻动反应液体,搅拌B、C中的反应物,使反应充分进行;
(3) a.向B内加入酸之前,排尽装置内的CO2气体,保证最后吸收的气体完全由反应制备,提高反应精确度;
b.向B内滴加酸时不宜过快,使碳酸氢钠与酸充分反应,提高反应效率;
c.在B、C之间增添盛有饱和NaHCO3溶液的洗气装置对反应结果无作用,此反应不需要收集二氧化碳,不用饱和碳酸氢钠溶液;
d.在D后增添盛有碱石灰的干燥管,保证气体被彻底吸收,确保实验结果准确。
综上所述,不能提高测定精确度的措施是c。
乙用滴定法确定CO2的物质的量,用c mol·L-1的盐酸滴定(甲基橙作指示剂)。当滴入1滴盐酸,溶液刚好由黄色变橙色,且半分钟内不变色时,停止滴定。平行测定三次,由表可知,待测液20ml,消耗盐酸平均25ml,根据反应方程式NaHCO3+HCl=NaCl+CO2↑+H2O,m1 g样品产生CO2的物质的量![]() ;
;
丙用气体体积法确定CO2的体积,用连通器原理,通过收集二氧化碳气体,计算气体体积。 (4)为了减小实验误差,降低溶液对二氧化碳的吸收,量气管中加入的液体X为饱和碳酸氢钠溶液;
(5)若该装置气密性良好,但测得的“CO2体积”数据仍然偏小,其原因可能是测定气体体积时水准管的液面高于量气管的液面或有CO2溶解在水中;
(6)甲、乙实验可以计算气体质量,而丙实验只能知道气体体积和物质的量,故确定CO2的相对分子质量,选用甲、乙的实验数据为最佳。


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】工业炼铁用一氧化碳还原氧化铁时会发生如下一系列反应:
3Fe2O3+CO=2Fe3O4+CO2 Fe3O4+CO=3FeO+CO2 FeO+CO=Fe+CO2
某次实验中,用CO还原4.80g氧化铁,当固体质量变成4.56g时,测得此固体中只存在2种氧化物。则此固体成分和它们的物质的量之比可能的是
A.n(FeO):n(Fe3O4)=1∶1B.n(Fe2O3):n(FeO)=2∶1
C.n(Fe2O3):n(FeO)=1∶2D.n(Fe2O3):n(Fe3O4)=1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对如图装置(铁的防护)的分析正确的是( )
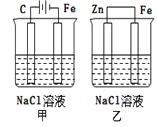
A.甲装置是牺牲阳极的阴极保护法
B.乙装置是牺牲阳极的阴极保护法
C.一段时间后甲、乙装置中pH均增大
D.甲、乙装置中铁电极的电极反应式均为:2H++2e→H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.101kPa时,2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1,则H2的燃烧热ΔH=-572kJ·mol-1
B.一定条件下发生反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4kJ·mol-1,此条件下将1.5mol H2和过量N2充分反应,放出热量46.2kJ
2NH3(g) ΔH=-92.4kJ·mol-1,此条件下将1.5mol H2和过量N2充分反应,放出热量46.2kJ
C.若将等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
D.已知:2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香料G的一种合成工艺如下图所示。
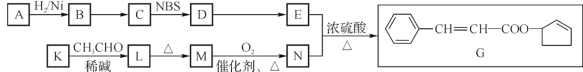
已知:A的分子式为C5H8O,它有两种不同环境的氢原子。
CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2
CH3CHO+CH3CHO![]()
![]()
![]()
![]() CH3CH=CHCHO+H2O
CH3CH=CHCHO+H2O
完成下列填空:
(1)A的结构简式为________________________________。
(2)D中官能团的名称为____________________________。
(3)检验M已完全转化为N的实验操作是___________________________________________。
(4)E与浓硫酸共热可制得H,H可制备一种高分子化合物Q。写出Q的结构简式_________。
(5)写出满足下列条件的L的两种同分异构体的结构简式(不考虑立体异构):__________。
①能发生银镜反应 ②能发生水解反应 ③苯环上的一氯代物有两种
(6)以1-丁醇和NBS为原料可以制备顺丁橡胶(![]() )。请设计合成路线(其他无机原料任选)并用如下方式表示:_____________________________。
)。请设计合成路线(其他无机原料任选)并用如下方式表示:_____________________________。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”是当今社会提出的一个新概念。在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%。在用丙炔合成甲基丙烯酸甲酯(![]() )的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物可以是
)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物可以是
A.CO和CH3OHB.CO2和H2OC.H2和COD.CH3OH和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯能在多种条件下发生水解反应:CH3COOC2H5+H2O![]() CH3COOH+C2H5OH。已知该反应的速率随c(H+)的增大而加快。下图为CH3COOC2H5的水解速率随时间的变化图。下列说法中正确的是
CH3COOH+C2H5OH。已知该反应的速率随c(H+)的增大而加快。下图为CH3COOC2H5的水解速率随时间的变化图。下列说法中正确的是

A. 图中A、B两点表示的c(CH3COOC2H5)相等
B. 反应初期水解速率增大可能是溶液中c(H+)逐渐增大所致
C. 图中t0时说明反应达到平衡状态
D. 图中tB时CH3COOC2H5的转化率等于tA时的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.澄清石灰水与过量的小苏打溶液反应:![]()
B.往明矾溶液中加入氢氧化钡溶液至Al3+完全沉淀: A13++2SO42-+2Ba2++3OH-![]() A1(OH)3↓+2BaSO4↓
A1(OH)3↓+2BaSO4↓
C.向NaHSO4溶液中滴加![]() 至刚好沉淀完全:
至刚好沉淀完全:![]() ↓
↓![]()
D.向含有0.1 mol溶质的FeI2溶液中通入0.1 mol的Cl2:2I— +Cl2![]() I2+2Cl--
I2+2Cl--
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com