
【题目】I.硝酸钾用途广泛,工业上一般用复分解反应制取硝酸钾(相关物质的溶解度曲线见表)。以硝酸钠和氯化钾为原料制备硝酸钾的工艺流程如下:
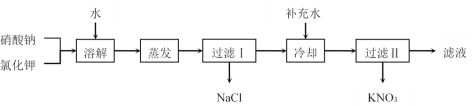

完成下列填空:
(1)为了加速固体溶解,可采取的措施有__________(至少写两种);实验室进行蒸发结晶操作时,为了防止液滴飞溅,进行的操作是_____________。
(2)过滤I所得滤液中含有的离子是________;过滤I所得滤液在进行冷却结晶前应补充少量水,目的是______________。
(3)检验产品KNO3中杂质的方法是________________。
II.实验室模拟工业上用氯化钾和硝酸铵为原料制取硝酸钾的过程如下:
取40 g NH4NO3和37.25 g KCl固体加入100 g水中,加热至90℃,固体溶解, 用冰水浴冷却至5℃以下,过滤(a)。在滤液中再加入NH4NO3,加热蒸发,当体积减小到约原来的![]() 时,保持70℃过滤(b),滤液可循环使用。完成下列填空:
时,保持70℃过滤(b),滤液可循环使用。完成下列填空:
(4)过滤(a)得到的固体物质主要是__________;在滤液中再加入NH4NO3的目的是________________________。
(5)为检测硝酸钾样品中铵盐含量,称取1.564 g样品,加入足量的NaOH浓溶液,充分加热,生成的气体用20.00 mL 0.102 mol/L H2SO4溶液全部吸收,滴定过量的H2SO4用去0.089 mol/L标准NaOH溶液16.55 mL。滴定过程中使用的指示剂是________;样品中含铵盐(以氯化铵计)的质量分数是___________(保留3位小数)。
【答案】加热、搅拌、研细颗粒 用玻璃棒不断搅拌滤液 K+、NO3-、Na+、Cl- 减少NaCl的结晶析出 取少量固体溶于水,加入硝酸酸化的硝酸银溶液,若生成白色沉淀说明含有杂质 KNO3 增大铵根离子的浓度,有利于氯化铵结晶析出 甲基橙 8.92%
【解析】
硝酸钠和氯化钾用水溶解,得到的溶液中含有K+、NO3-、Na+、Cl-,由于在溶液中NaCl的溶解度较小,且受温度影响不大,采取蒸发浓缩,析出NaCl晶体,过滤分离出NaCl晶体。由于硝酸钾溶解度受温度影响比硝酸钠大,采取冷却结晶析出硝酸钾,过滤出硝酸钾晶体后,向滤液中加入NH4NO3,可增大溶液中NH4+浓度,有利于NH4Cl结晶析出。
I.(1)加热、搅拌、研细颗粒等都可以加快物质溶解;实验室进行蒸发结晶操作时,为防止液滴飞溅,要用玻璃棒不断搅拌滤液,使溶液受热均匀;
(2)过滤I后析出部分NaCl,滤液I含有K+、NO3-、Na+、Cl-;氯化钠溶解度较小,浓缩析出NaCl晶体后,直接冷却会继续析出NaCl晶体,在进行冷却结晶前应补充少量水,可以减少NaCl的结晶析出;
(3)产品KNO3中可能含有Na+、Cl-杂质离子,检验的方法是:取少量固体溶于水,加入硝酸酸化的硝酸银溶液,若生成白色沉淀说明含有杂质NaCl,即含有杂质;
II.(4)取40 g NH4NO3和37.25 g KCl固体加入100 g水中,加热至90℃所有固体均溶解,用冰水浴冷却至5℃以下时,硝酸钾的溶解度最小,首先析出的是硝酸钾晶体;在滤液中加入硝酸铵可以增大铵根离子浓度,使NH4Cl晶体析出;
(5)由于恰好反应时生成的溶质为(NH4)2SO4和Na2SO4,溶液为酸性,则应该选用甲基橙为指示剂;
硫酸总的物质的量n(H2SO4)=c·V=0.102 mol/L×0.02 L=0.00204 mol,含有氢离子的物质的量为n(H+)=2n(H2SO4)=2×0.00204 mol =0.00408mol,氢氧化钠的物质的量n(NaOH)= c·V =0.089 mol/L×0.01655 L=0.001473 mol,所以氨气的物质的量n(NH3)=0.00408 mol-0.001473 mol=0.002607 mol,所以根据N元素守恒,可知样品中氯化铵的物质的量为0.002607 mol,
则样品中氯化铵的质量分数为:![]() ×100%≈8.92%。
×100%≈8.92%。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】蒽(![]() )与苯炔(
)与苯炔(![]() )反应生成化合物X(X结构中三个苯环呈立体对称结构),如下图:
)反应生成化合物X(X结构中三个苯环呈立体对称结构),如下图:
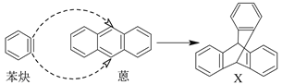
(1)蒽与X都属于_________________(填编号)。
a.环烃 b.不饱和烃 c.烷烃 d.芳香烃
(2)苯炔的分子式为_____________,苯炔不具有的性质______________(填编号)。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(3)X的一个氢原子被甲基取代的所有同分异构体数为__________(填编号)。
a.2种 b.3种 c.4种 d.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2CO3的电离常数:K1=4.4×10-7,K2=4.7×10-11,HClO的电离常数:2.95×10-8。反应:Cl2+H2O![]() HCl+HClO达到平衡后,要使c(HClO)增大可加入( )
HCl+HClO达到平衡后,要使c(HClO)增大可加入( )
A.NaOHB.HClC.CaCO3(固体)D.H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水生产过程中,可用氯气等物质作消毒剂,明矾等物质作絮凝剂。出厂的自来水中含少量可溶性矿物质。完成下列填空:
(1)自来水中含硫量约70 mg/L,它只能以______(填微粒符号)形态存在,不能以其它形态存在的原因是________________________。
(2)已知在碱性条件下,氯气会发生自身氧化还原反应,某反应体系中的物质为:KClO3、Cl2、KCl、KOH、H2O。
①写出该反应的化学方程式。____________________________。
②该反应中氧化剂与还原剂的质量比为_________。
(3)实验室利用反应6HCl+KClO3 → KCl+3H2O+3Cl2↑制取Cl2,当产生标准状况下的气体3.36 L时,转移电子_____mol。
(4)不同环境中,物质的性质可能会有所不同。根据上述两题的反应中KClO3和Cl2的氧化性强弱比较,你能得出的结论是________________________。
(5)铝铵矾[NH4Al(SO4)212H2O]也是常用的工业净水剂,其净水的化学原理是________________(用离子方程式表示)。
(6)在向铝铵矾溶液中逐滴滴加氢氧化钡溶液的过程中,下列关系可能正确的是_________。(选填编号)
a.n(SO42-)>n(NH4+)>n(A13+)>n(OH-)
b.n(A13+)>n(NH4+)>n(SO42-)>n(H+)
c.n(BaSO4)>n[A1(OH)3]>n(NH3·H2O)>n(A1O2-)
d.n(NH3·H2O)>n(BaSO4)>n[A1(OH)3]>n(A1O2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对乙酰氨苯酚(M)是常用的消炎解热镇痛药。其合成路线如下:
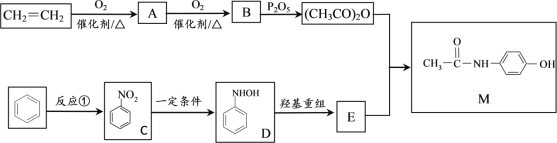
完成下列填空:
(1)A的结构简式为____________。C→D的反应类型为___________________。
(2)实验室中进行反应①的实验时添加试剂的顺序为________________________。
(3)下列有关E的说法正确的是____________。(选填编号)
a.分子式为C6H6NO b.能与溴水发生加成反应
c.遇到FeCl3溶液能发生显色反应 d.既能和氢氧化钠溶液反应,又能和盐酸反应
(4)已知![]() 与
与![]() 的性质相似,写出一定条件下M与NaOH溶液反应的化学方程式。______________________
的性质相似,写出一定条件下M与NaOH溶液反应的化学方程式。______________________
(5)满足下列条件的M的同分异构体有_____________种。
①苯环上只有两种不同环境的氢原子;②苯环上连有-NH2;③属于酯类物质。
(6)N-邻苯二甲酰甘氨酸( )是重要的化工中间体,工业上以邻二甲苯和甘氨酸(NH2-CH2-COOH)为原料通过一系列的反应制取该化合物,请参照上述流程的相关信息,写出最后一步反应的化学方程式。_____________________
)是重要的化工中间体,工业上以邻二甲苯和甘氨酸(NH2-CH2-COOH)为原料通过一系列的反应制取该化合物,请参照上述流程的相关信息,写出最后一步反应的化学方程式。_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为周期表中短周期的一部分,若R原子核外有3个未成对电子,说法正确的是

A.原子半径大小顺序是:Y>X>R
B.其气态氢化物的稳定性顺序是:Z>Y>X>R
C.X、Y、Z中Z的氧化物对应的水化物的酸性最强
D.R的气态氢化物与它的含氧酸之间能发生化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业炼铁用一氧化碳还原氧化铁时会发生如下一系列反应:
3Fe2O3+CO=2Fe3O4+CO2 Fe3O4+CO=3FeO+CO2 FeO+CO=Fe+CO2
某次实验中,用CO还原4.80g氧化铁,当固体质量变成4.56g时,测得此固体中只存在2种氧化物。则此固体成分和它们的物质的量之比可能的是
A.n(FeO):n(Fe3O4)=1∶1B.n(Fe2O3):n(FeO)=2∶1
C.n(Fe2O3):n(FeO)=1∶2D.n(Fe2O3):n(Fe3O4)=1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”是当今社会提出的一个新概念。在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%。在用丙炔合成甲基丙烯酸甲酯(![]() )的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物可以是
)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物可以是
A.CO和CH3OHB.CO2和H2OC.H2和COD.CH3OH和H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com