
| A、甲醛 | B、乙醛 | C、甲酸 | D、甲醇 |
科目:高中化学 来源: 题型:
| A、沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
| B、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| C、根据是否有丁达尔效应将分散系分为溶液、胶体和浊液 |
| D、使用静电除尘器除去空气中的飘尘利用了胶体的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
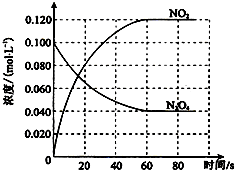 在容积为100L的容器中,通入一定量的N2O4,发生反应N2O4g)═2NO2 (g),随温度升高,混合气体的颜色变深.
在容积为100L的容器中,通入一定量的N2O4,发生反应N2O4g)═2NO2 (g),随温度升高,混合气体的颜色变深.查看答案和解析>>
科目:高中化学 来源: 题型:
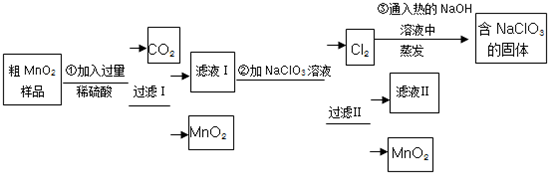
查看答案和解析>>
科目:高中化学 来源: 题型:


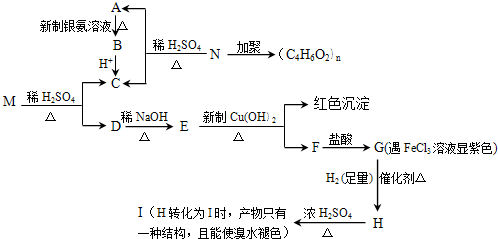
查看答案和解析>>
科目:高中化学 来源: 题型:
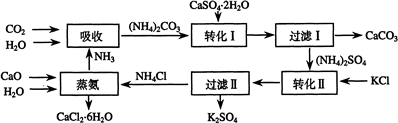
 通过资源化利用的方式将CO2转化为具有工业应用价值的产品(如图所示),是一种较为理想的减排方式,下列说法中正确的是( )
通过资源化利用的方式将CO2转化为具有工业应用价值的产品(如图所示),是一种较为理想的减排方式,下列说法中正确的是( )| A、CO2经催化分解为C、CO、O2的反应为放热反应 |
| B、除去Na2CO3固体中少量NaHCO3可用热分解的方法 |
| C、过氧化尿素和SO2都能使品红溶液褪色,其原理相同 |
| D、由CO2和H2合成甲醇,原子利用率达100% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度(℃) | 0 | 20 | 60 |
| K2SO4溶解的量(g) | 7.4 | 11.1 | 18.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
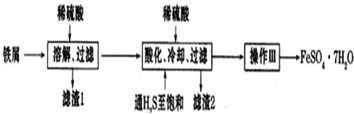
| 25℃ | 饱和H2S溶液 | SnS沉淀完全 | FeS开始沉淀 | FeS开始沉淀 |
| pH | 3.9 | 1.6 | 3.0 | 5.5 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com