
【题目】下列有关说法不正确的是
A.元素周期表中有7个主族、7个副族
B.稀有气体元素原子的最外层电子数均为8
C.氢是原子半径最小的元素
D.硫元素位于第3周期ⅥA族
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列字母分别代表某一元素。根据表中所列元素回答下列问题:

(1)元素d在周期表中的位置是_____________,h与f原子序数相差______________
(2)b、c、f的简单离子半径最小的是___________(填离子符号),原子半径最小的是______(填化学式)
(3)表中第三周期元素的非金属性最强是_________(用元素符号表示), e、f、g三种元素的气态氢化物最不稳定的是__________(用化学式表示)
(4)g元素与b元素的最高价氧化物对应水化物反应的化学方程式为________________________
利用元素周期表,我们可以认识更多元素的性质
(5)元素周期表位于对角线的两种元素其性质相似称之为对角线规则。根据周期表对角线规律,金属Be单质及其化合物的性质与铝单质及其化合物的性质相似。则鉴别Be(OH)2和Mg(OH)2可选用的试剂为__________溶液
(6)铅(Pb)、锡(Sn)、锗(Ge)与元素(C)、硅(Si)同主族,常温下其单质在空气中,锡、锗不反应而铅表面生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
① 锗的原子序数为__________;
② 铅(Pb)、锡(Sn)、锗(Ge)的+4价氢氧化物的碱性由强到弱的顺序为__________(填化学式)
(7)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来最重大突破。己知铷(Rb)是37号元素,质量数是85,与钠同主族。回答下列问题:
①铷在周期表中的位置为___________________
②同主族元素的同类化合物的性质相似,请写出:
AlCl3与过量的RbOH反应的离子方程式:_____________________________
③现有铷和另一种碱金属形成的混合金属50g,当它与足量水反应时,放出标准状况下的氢气22.4L,这种碱金属可能是__________
A.Li(7) B.Na(23) C.K(40) D.Cs(133)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 L(标准状况下)某气态烃,完全燃烧生成的CO2和水蒸气在273 ℃、1.01×105 Pa下体积为y L,当冷却至标准状况时体积为x L。下列用x、y表示该烃的化学式正确的是
A. CxHy-2x B. CxHy-x C. CxH2y-2x D. CxHy
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,其中N的化合价为________,是_____________(用“电解质”或者“非电解质”填空)。NaN3受热分解产生N2和Na,则该反应方程式为: ________。已知常温常压下气体摩尔体积为24.5L/mol,则在常温常压下,反应130g NaN3能产生_____________L的N2。
(2)Fe2O3是主氧化剂,与Na反应生成的还原产物为________________(已知该反应为置换反应)。若已知2.3gNa完全反应,转移的电子物质的量为____________。
(3)KClO4是助氧化剂,反应过程中与Na作用生成KC1和Na2O,请用单线桥表示该反应电子转移:KClO4+8Na= KCl+4Na2O_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学知识在生活中有重要意义,下列说法不正确的是( )
A. 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮氧化变质
B. 烧碱可以用于治疗胃酸过多
C. 计算机芯片所用的材料是高纯度的硅
D. 纯净的二氧化硅是生产光纤制品的基本原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取镁的工业生产流程如下:
海水![]() Mg(OH)2
Mg(OH)2![]() MgCl2·6H2O
MgCl2·6H2O![]() MgCl2
MgCl2![]() Mg
Mg
下列说法错误的是( )
A. 此法的优点之一是原料来源丰富
B. 该提取镁的过程中涉及置换、分解、复分解和氧化还原反应
C. 步骤①②③的目的是从海水中提取无水MgCl2
D. 步骤②中加盐酸的离子方程式为Mg(OH)2+2H+Mg2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物D是重要的有机化工中间体,以丙烯为原料合成D的流程如下:

已知:
①在一定条件下,烯烃中α—H能与C12发生取代反应,生成氯代烯烃,但双键碳上的氢原子很难发生取代反应。
②
回答下列问题:
(1)B的结构简式为___________,B→C的反应类型是___________。
(2)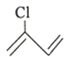 的名称为___________,该有机物分子中最多有___________个原子共平面。
的名称为___________,该有机物分子中最多有___________个原子共平面。
(3)反应C→D的化学方程式为______________________________________________。
(4)写出用1,3-丁二烯为原料制备化合物 的合成路线_________(其他试剂任选。提示:可利用1,3-丁二烯与Cl2的1,4-加成反应)。合成路线流程图示例:CH3CH2OH
的合成路线_________(其他试剂任选。提示:可利用1,3-丁二烯与Cl2的1,4-加成反应)。合成路线流程图示例:CH3CH2OH![]() CH2=CH2
CH2=CH2![]() CH3CH2Cl。
CH3CH2Cl。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com