
(一)、某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5um的悬浮颗粒物)其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)对PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol.L | 4x10ˉ6 | 6x 10ˉ6 | 2x10ˉ5 | 4x10ˉ5 | 3x10ˉ5 | 2x10ˉ5 |
 H= -241.8KJ/mol C(s)+1/2O2(g)=CO(g)
H= -241.8KJ/mol C(s)+1/2O2(g)=CO(g)  H= -110.5KJ/mol
H= -110.5KJ/mol
(一)
(1)观察表格中发现NH4+水解显酸性,PM2.5的酸碱性为酸性。试样的PH值根据溶液中电荷守恒计算H+离子浓度为10-4,PH值为4。
(2)焦炭与水蒸汽反应的热化学方程式:C(s)+H2O(g)="CO(g)+H2(g)" H=+131.3kJ/mol 洗涤含SO2的烟气,根据酸性氧化物的性质选a.Ca(OH)2 b.Na2CO3。(二)(9分)(1) NH4NO3(1分);(2)②③(2分)
(3) 稀HNO3、浓HNO3(每空1分,共3分) :CO2(N2、H2合理答案均可)
(二)(1)NH4NO3; (2)>;②③
(2)>;②③
(3)a:H2O;稀HNO3;浓HNO3;b:CO2(或N2、H2,合理答案均可);c:装置②中液面上方气体仍为无色,装置③中液面上方气体由无色变为红棕色
解析试题分析:
(一)(1)观察表格中发现NH4+水解显酸性,PM2.5的酸碱性为酸性。试样的PH值根据溶液中电荷守恒计算H+离子浓度为10-4,PH值为4。
(2)焦炭与水蒸汽反应的热化学方程式:C(s)+H2O(g)="CO(g)+H2(g)" H=+131.3kJ/mol
(3)洗涤含SO2的烟气,根据酸性氧化物的性质选a.Ca(OH)2 b.Na2CO3。
(二)(1)由上述分析可知,X为NH4NO3,D为Na,
(2)C为O,E为S,非金属性C>E,可利用气态氢化物的稳定性及单质之间的置换反应来说明,故②③能说明这一结论;
(3)a.BC为NO,BC2为NO2,浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC,则①中为水,②中为稀硝酸,③中为浓硝酸可验证浓硝酸的氧化性比稀硝酸的氧化性强,
生成的二氧化氮在⑤中与碱反应;
b.为避免NO被氧化,在实验之前应通入的该气体可以是CO2(N2、H2等合理答案均可);
c.该实验成功可观察到装置②中液面上方气体仍为无色,装置③中液面上方气体由无色变为红棕色。
考点:本题考查位置、结构、性质的应用,注意元素的推断是解答本题的关键,明确非金属性的比较及硝酸的性质是解答本题的关键,(3)中实验为解答的难点,把握NO易被氧化及有关的反应即可解答,题目难度较大。


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:填空题
某化合物M(式量为80)俗称黑肥宝,它由原子序数不大于20的X、Y、Z三种元素组成,X、Y、Z的原子序数依次增大,其关系为Z=X+2Y。X、Y是同周期相邻的两种元素。M微溶于水,在常温下与水作用发生缓慢水解,最终产物为一种白色沉淀A与气体B,该气体能使湿润的红色石蕊试纸变蓝,A在高温条件下可分解产生一种有温室效应的气体。(注:以下回答若涉及到具体物质均用相应的化学式或元素符号表示)
(1)化合物M的化学式为 ;Z的原子结构示意图为 。
(2)写出下列反应的化学方程式。A在高温下分解: ; M与水反应生成A和B: 。
(3)Z的氢化物可作为一种储氢材料,写出其与水反应的化学方程式 。
(4)储氢材料的研究很广泛。下列物质中,可作为储氢材料的是 。(填编号)
| A.Ca(OH)2 | B.MgH2 | C.O2 | D.LaNi5 |
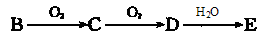 (强酸),将C和D的混气体通入NaOH溶液中恰好完全反应得到一种盐,请设计一个实验方案检验其中的阴离子 。
(强酸),将C和D的混气体通入NaOH溶液中恰好完全反应得到一种盐,请设计一个实验方案检验其中的阴离子 。查看答案和解析>>
科目:高中化学 来源: 题型:填空题
完成下列填空
(1)向煤中加入适量的 ,可以大大减少燃烧产物中SO2的量。
(2)铝制品具有良好抗腐蚀性的原因是 。
(3)在少量的胆矾晶体中加入3 mL浓硫酸,片刻后变白色,证明浓硫酸具有 性。
(4)区别氯化铁溶液与氢氧化铁胶体的实验名称是 实验。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知A、B、C、D、E五种主族元素分属三个短周期,且原子序数依次增大。A、C同主族,可形成离子化合物CA;B、D同主族,可形成DB2、DB3两种分子。请回答下列问题:
(1)元素E在元素周期表中的位置是
(2)A、B两种元素能形成两种常温下呈液态的化合物M、N,具有强氧化性的化合物M的电子式可表示为 ;化合物N在同主族元素形成有具有相同结构的物质中,具有较高的沸点,其原因是 。
(3)A、B、C、D中的三种或四种元素能形成多种离子化合物,其水溶液呈碱性的有 (写出所有化合物,用化学式表示,下同),呈酸性的有 (写出所有化合物)。
(4)元素B、E的单质或两元素之间形成的化合物可作水消毒剂的有 (写出其中两种物质的化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
五种元素原子半径最大是(写元素符号)
X与Z形成的化合物中,既含极性键又含非极性键的是(写分子式)————
由以上某些元素组成的化合物A、B、C、D有如下转化关系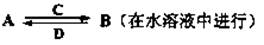
①其中C是溶于水显酸性的气体;D是淡黄色固体。写出C与D反应的化学方程式
②如果A由四种元素组成、B均由三种元素组成,B为两性不溶物,则A为(填名称)
由A与过量C反应转化为B的离子方程式
③如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。则B为(填化学式) 。A、B浓度均为0.1mol/L的混合溶液,碱性较强的是(填溶液名称)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号) 。
(2)由以上某些元素组成的化合物A、B、C、D有如下转化关系: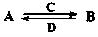 (在水溶液中进行)其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式: ;D的电子式: 。
(在水溶液中进行)其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式: ;D的电子式: 。
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为 ;由A转化为B的离子方程式为 。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因: 。常温下,A、B浓度均为0.1mol·L-1的混合溶液中,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系: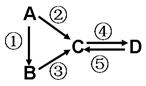
⑴若A是淡黄色固体,C、D是氧化物, C是造成酸雨的主要物质,但C也有其广泛的用途,写出其中的两个用途 。
⑵若B是气态氢化物。C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气主要成分,写出该反应的化学方程式 。
⑶若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置是 。
⑷若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式 。D的化学式是 。
⑸若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学兴趣小组的同学利用下图所示实验装置进行某些气体的制备、性质等实验(图中夹持装置有省略)。请按要求填空: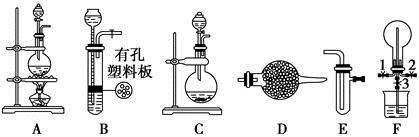
Ⅰ.探究氯气与氨气的反应
(1)为制取干燥氨气,可将装置C与________(填装置编号)连接;装置C中的烧瓶内固体宜选用________。
a.碱石灰 b.氯化钙
c.五氧化二磷 d.生石灰
(2)装置A、E、E连接可制取纯净、干燥的氯气,则两个E装置内的药品依次是________________。
(3)装置F可用于探究氯气与氨气(已知氯气与氨气可发生反应:3Cl2+2NH3=N2+6HCl)的反应。实验时打开弹簧夹1、3,关闭2,先向烧瓶中通入________,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体。实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子_____________________________________。
Ⅱ.探究某些物质的性质
(4)利用装置A、E,可设计实验比较Cl-和Br-的还原性强弱,能证明结论的实验现象是_______________________________________________________。
(5)若利用装置A、E进行乙烯与溴水反应的实验,写出反应的化学方程式_________________________________________
(6)将装置B、C分别与F相连后,进行H2S与SO2反应的实验。F的烧瓶中发生反应的化学方程式为______________________;F的烧杯所起的作用是_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期中的A、B、C、D、E五种元素,原子序数依次增大,A和D,C和E分别同主族,A为非金属元素,且A与B的原子序数之和等于C的原子序数,C2-与D+的核外电子数相等。则下列说法正确的是
A.B与A只能组成BA3化合物
B.C、D、E形成的化合物与稀硫酸可能发生氧化还原反应
C.A、B、C形成的化合物一定不能发生水解反应
D.E的氧化物对应的水化物一定有强的氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com