
【题目】锌铝合金是以Zn、Al 为主,Cu、Mg为辅的多元化合金。测定其中Cu含量的实验步骤如下:
①称取该合金样品1.100 g,用稀H2SO4和H2O2溶解后煮沸除去过量H2O2,残液定容于250mL容量瓶中;
②用移液管移取50.00mL配制液于250mL碘量瓶中,调节溶液的pH=3~4,加入过量KI溶液2Cu2++4I-=2CuI↓+I2)和3-4滴淀粉溶液;
③用1.100x10-2mol/LNa2S2O3溶液滴定生成的I2至终点(I2+2S2O32-=2I-+S4O62-),消耗Na2S2O3溶液6.45mL。
请回答:
(1)步骤①中溶解Cu的离子方程式___________________。
(2)步骤③中判断滴定终点的方法_______________________。
(3)合金中Cu的质量分数_____________。(结果保留三位有效数字)
【答案】 Cu+H2O2+2H+=Cu2++2H2O 当最后一滴Na2S2O3溶液滴入时,溶液蓝色褪去,半分钟颜色不再变化 2.06%
【解析】(1)酸性条件下,Cu与双氧水反应生成铜离子和水,其反应的离子方程式为:Cu+2H++H2O2═Cu2++2H2O;故答案为:Cu+2H++H2O2═Cu2++2H2O;
(2)淀粉溶液为指示剂,当最后一滴Na2S2O3溶液滴入时,I2与a2S2O3恰好反应,I2被完全消耗,溶液蓝色褪去,半分钟颜色不变,说明滴定到达终点,故答案为:当最后一滴Na2S2O3溶液滴入时,溶液蓝色褪去,半分钟颜色不变;
(3)由②可知发生反应2Cu2++4I-=2CuI↓+I2,I2+2S2O32-=2I-+S4O62-,
根据关系式:2Cu~~2Cu2+~~I2~~2S2O32-,
2 2
n(Cu) 0.01100mol/L×6.45×10-3L×5
所以 n(Cu)=0.01100mol/L×6.45×10-3L×5=5.5×6.45×10-5mol,合金中Cu的质量分数为![]() ×100%=2.06%,答:合金中Cu的质量分数为2.06%。
×100%=2.06%,答:合金中Cu的质量分数为2.06%。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是( )
A. 5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,生成28gN2,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28gN2,转移的电子数目为3.75NA
B. 室温下,0.2mol·L-1的Na2SO4溶液中含Na+数目为0.4NA
C. 标准状况下,NA个HF分子所占的体积约为22.4L
D. 高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W![]() X+H2O+CO2↑ ②Z+CO2―→X+O2
X+H2O+CO2↑ ②Z+CO2―→X+O2
③Z+H2O―→Y+O2↑ ④X+Ca(OH)2―→Y+CaCO3↓
试回答下列问题:
(1)W、X、Y、Z的化学式分别是W__________、X__________、Y__________、Z__________。
(2)以上4个化学反应,属于氧化还原反应的是________(填反应序号),反应中的氧化剂是____________(写化学式),还原剂是____________(写化学式)。
(3)若反应④在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化学反应的化学方程式:
①离子方程式:________________。
②化学方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知五种元素的原子序数的大小顺序为C>A>B>D>E;其中,A、C同周期,B、C同主族;A与B 形成离子化合物A2B,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子分子。试回答下列问题:
(1)画出元素C的原子结构示意图:________。
(2)写出元素D在元素周期表中的位置:第____周期,第____族;该元素形成的单质的结构式为______。
(3)写出下列物质的电子式:A、B、E形成的化合物______;D、E形成的化合物______。
(4)D、E形成的化合物受热蒸发,吸收的热量用于克服________。
(5)A、B两元素组成的化合物A2B2属于______(填“离子”或“共价”)化合物,其存在的化学键有______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用1L 0.1mol·L-1NaOH溶液吸收0.07molCO2,所得溶液中n(Na2CO3)和n(NaHCO3)之比约为
A. 3︰4 B. 3︰1 C. 2︰3 D. 3︰2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,在“H2A—HA-—A2-”的水溶液体系中,H2A、HA-和A2- 三者中各自所占的物质的量分数(α)随溶液pH变化的关系如图所示。下列说法正确的是
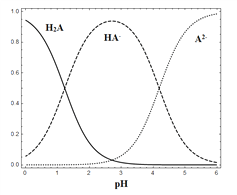
A. 在含H2A、HA-和A2- 的溶液中,加入少量NaOH固体,α(HA-)一定增大
B. 将等物质的量的NaHA和Na2A混合物溶于水,所得的溶液中α(HA-)=α(A2-)
C. NaHA溶液中,HA-的水解能力小于HA-的电离能力
D. 在含H2A、HA-和A2-的溶液中,若c(H2A)+2c(A2-)+c(OH-)=c(H+),则α(H2A)和α(HA-)一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究铁、铜及其化合物的性质,某同学设计并进行了下列实验。
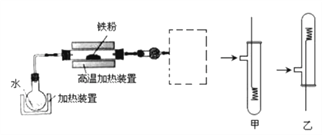
已知: 3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g)
Fe3O4(s)+4H2(g)
请回答:
(1) 虚线框处宜选择的装置是_____ (填“甲”或“乙”); 实验时应将螺旋状铜丝加热,变黑后再趁热迅速伸入所制得的纯净氢气中,观察到的实验现象是_________。
(2)实验后,取硬质玻璃管中适量的固体,用一定浓度的盐酸溶解,滴加KSCN溶液,没有出现血红色,说明该固体中没有+3价的铁,判断结论是否正确并说明理由_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据要求填空:
(1)水的电离与溶液的酸碱性密切相关。
①常温下,某柠檬水溶液的pH=3,其中的c(OH-)=__________。
②常温下,浓度均为0.1 molL-1的CH3COOH溶液和CH3COONa溶液中,水的电离程度大小关系是:前者_____________后者(填“>”“<”或“=”);
③常温下,浓度均为0.1 molL-1的NaX和NaY两种盐溶液,其pH分别为8 和10,则HX 和HY的酸性强弱关系是:HX_________HY(填“>”或“<”)。
(2)研究化学能与电能相互转化的装置、过程和效率的科学,叫做电化学。
①某原电池装置如右图,则:

该原电池的负极是__________(填“Zn”或“Cu”),正极的电极反应式为_______________________;
②用铂电极电解某金属氯化物(XCl2)的溶液,当收集到2.24 LCl2(标准状况)时,阴极增重6.4 g,则该金属的相对原子质量为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W、R原子序数依次增大。m、p、r是这些元素组成的二元化合物,n、q、s是这些元素组成的三元化合物且属于离子化合物。其中s的水溶液俗称水玻璃。常温下0.1mol·L-1 n溶液的pH为13,m是典型的两性物质。上述物质的转化关系如图所示,下列说法正确的是( )

A. 简单氢化物的沸点:R>Y
B. W的最高价氧化物对应的水化物碱性比Z的强
C. 单质的熔点:Z>R>W
D. s是制备硅胶和木材防火剂等的原料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com