
【题目】下列有关物质性质实验的叙述,正确的是
A.钠在空气中燃烧,生成淡黄色的氧化钠
B.钠是一种强还原剂,可以把钛从其盐溶液中置换出来
C.将灼热的铜丝放入盛有氯气的集气瓶中,生成棕黄色的雾
D.Fe(OH)3胶体具有吸附性,能吸附水中的悬浮颗粒并沉降,因而可用于净水
 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示:
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
资料显示,反应分两步进行:① 2Fe3++H2O2 == 2Fe2++O2↑+2H+,② H2O2+2Fe2++2H+ == 2H2O+2Fe3+。反应过程中能量变化如下图所示。下列说法错误的是
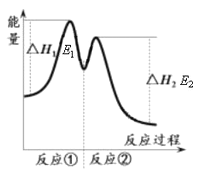
A. Fe3+的作用是增大过氧化氢的分解速率
B. 反应①是吸热反应、反应②是放热反应
C. 反应2H2O2(aq) == 2H2O(l)+O2(g)的ΔH=E1-E2<0
D. 0~6 min的平均反应速率:v(H2O2)=3.33×10-2 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,在半透膜袋里盛有淀粉的氯化钠溶液,将半透膜袋悬挂在蒸馏水中,回答下列问题:(知识支持:淀粉遇碘单质变蓝)
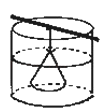
(1)取袋内液体,分为两份,一份中加入AgNO3溶液,则现象为________.另一份中加入碘水,现象为________
(2)一段时间后,做如下实验:取烧杯内液体,分为两份,一份中加入AgNO3溶液,则现象为________.另一份中加入碘水,现象为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠晶体(Na2MoO4·2H2O)常用于制造阻燃剂和无公害型冷水系统的金属抑制剂。下图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图:

回答下列问题:
(1)提高焙烧效率的方法有____________。(写一种)
(2)“焙烧”时MoS2转化为MoO3,该反应过程的化学方程式为________________________,氧化产物是________(写化学式)。
(3)“碱浸”时含钼化合物发生的主要反应的化学方程式为__________________________。
(4)若“除重金属离子”时加入的沉淀剂为Na2S,则废渣成分的化学式为________。
(5)测得“除重金属离子”中部分离子的浓度:c(MoO42-)=0.40mol/L,c(SO42-)=0.04mol/L。“结晶”前需先除去SO42-,方法是加入Ba(OH)2固体。假设加入Ba(OH)2固体后溶液体积不变,当SO42-完全沉淀(c(SO42-)≤1.0×10-5mol/L)时,BaMoO4是否会析出?____________________________________。(请计算说明)[已知:Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8]
(6)钼精矿在碱性条件下,加入NaClO溶液,也可以制备钼酸钠,同时有SO42-生成,该反应的离子方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是 ( )
A. 2 mol H2O的摩尔质量和1 mol H2O的摩尔质量
B. 200 mL 1 mol·L-1氯化钙溶液中c(Cl-)和100 mL 2 mol·L-1氯化钾溶液中c(Cl-)
C. 64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D. 20% NaOH溶液中NaOH的物质的量浓度和10% NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关苯甲酸重结晶实验的说法错误的是
A. 溶解粗苯甲酸过程中,加热、玻璃棒搅拌均能提高苯甲酸的溶解度
B. 苯甲酸溶解时,若加水加热后仍有不溶物,说明该不溶物是不溶性杂质
C. 过滤时,趁热过滤可防止苯甲酸晶体提前析出
D. 冷却结晶时,温度过低杂质将析出,故此时温度不是越低越好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某三原子分子构成的气体,其摩尔质量为M g/mol,该气体质量为m g,阿伏加德罗常数为NA , 则:
(1)该气体在标准状况下的体积为 ________ L.
(2)该气体在标准状况下的密度为 ________ g/L.
(3)该气体所含原子总数为 ________ 个.
(4)该气体的一个分子的质量为 ________ g.
(5)该气体完全溶于水形成V L溶液(不考虑反应),所得溶液的物质的量浓度为________mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的氯气通入30 mL浓度为10 mol/L的氢氧化钠浓溶液中,加热少许时间后均完全反应溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是( )
A. Cl2在反应中仅作氧化剂
B. ClO3—中心原子采用sp2杂化
C. n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1
D. 与NaOH反应的氯气一定为0.15 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示三套实验装置,分别回答下列问题。
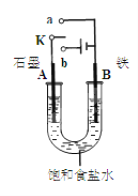
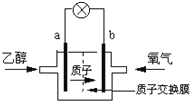
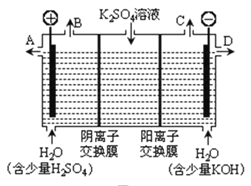
图1图2图3
(1)图1中,① 若开始时开关K与a连接,则该装置为_____(填装置名称),电极A的电极反应式为________________________
②若开始时开关K与b连接,则总反应的离子方程式为 ___________________________
(2)2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200°C左右时供电,电池示意如图2所示:
①______极(填a或b)为电池的正极,电池工作时电流方向为_________(填a→b或b→a)
②写出该电池负极的电极反应式________________________________________
(3)用图3装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾(电解槽内的阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)。
①该电解槽的阴极反应式为_____________________。
②制得的硫酸溶液从出口____(填“A”、“D”)导出,并简述原因__________________________(请用化学用语和文字解释)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com