
【题目】下列有关苯甲酸重结晶实验的说法错误的是
A. 溶解粗苯甲酸过程中,加热、玻璃棒搅拌均能提高苯甲酸的溶解度
B. 苯甲酸溶解时,若加水加热后仍有不溶物,说明该不溶物是不溶性杂质
C. 过滤时,趁热过滤可防止苯甲酸晶体提前析出
D. 冷却结晶时,温度过低杂质将析出,故此时温度不是越低越好
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中能大量共存的是( )
A.K+、HCO3﹣、CO32﹣、Br﹣
B.SO32﹣、HSO3﹣、OH﹣、K+
C.Fe3+、Cu2+、NO3﹣、SO32﹣
D.H+、Na+、NO3﹣、Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸 | CH3COOH | H2CO3 |
电离平衡常数(常温) | Ka=1.8×10-5 | Ka1=4.3×10-7; Ka2=5.6×10-11 |
下列判断正确的是
A. 向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,则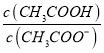 =18
=18
C. NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将200mL0.01mol/LNaOH与50mL某浓度的Ca (OH)2溶液混合(混合后体积变化忽略不计),所得溶液中OH﹣的物质的量浓度是0.016mol/L,则Ca(OH)2溶液的物质的量浓度是mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质实验的叙述,正确的是
A.钠在空气中燃烧,生成淡黄色的氧化钠
B.钠是一种强还原剂,可以把钛从其盐溶液中置换出来
C.将灼热的铜丝放入盛有氯气的集气瓶中,生成棕黄色的雾
D.Fe(OH)3胶体具有吸附性,能吸附水中的悬浮颗粒并沉降,因而可用于净水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg·L-1。我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5 mg·L-1。水中溶解氧的测定步骤如下:
(1)向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;
(2)加入适量稀H2SO4,搅拌,等MnO(OH)2与I-完全反应生成Mn2+和I2后;
(3)用Na2S2O3标准溶液滴定至终点。
测定过程中物质的转化关系如下:
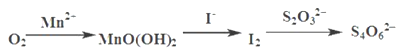
已知:MnO(OH)2+2I-+4H+ =Mn2++I2+3H2O 2S2O32- +I2= S4O62-+2I-
①加入稀硫酸后搅拌的作用是__________;Na2S2O3标准溶液应装在______________滴定管中(填酸式或碱式)。
②滴定过程中以_____________为指示剂;达到滴定终点的标志为____________________。
③写出O2将Mn2+氧化成MnO(OH)2的离子方程式____________________;
④若加入的稀H2SO4溶液反应后,若溶液pH过低,滴定时会产生明显的误差。写出产生误差的一个原因(用离子方程式表示)__________________。
⑤下列操作使测得水样中溶氧量(DO)比实际值偏高的是__________________。
A.第(1)步操作静置时没有密封 B.装Na2S2O3标准溶液的滴定管没有润洗
C.滴定前锥形瓶洗净后没有干燥 D.滴定前读数正确,滴定后俯视读数
⑥取加过一定量CaO2·8H2O的池塘水样l00.00mL,按上述方法测定水中溶解氧量,消耗0.01000
mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧为____________mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是一种有机光电材料中间体,由A制备F的一种合成路线如下:

已知:![]()
回答下列问题:
(1)A的结构简式为________,C的化学名称是______。
(2)①、③的反应类型分别是______、_______。
(3)②的反应条件是_______,有机物X的结构简式为____________。
(4)反应⑤的化学方程式为___________________。
(5)芳香化合物H是D的同分异构体,满足下列条件的同分异构体共有____种;
a.能发生银镜反应 b.含有—C≡CH结构 c.无—C≡C—O—结构
写出其中核磁共振氢谱峰面积比为1:2:2:1的一种有机物的结构简式_______。
(6)写出由1-丁炔和乙炔为原料制取化合物 的合成略线(其他试剂任选)_____。
的合成略线(其他试剂任选)_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g) 达到平衡。下列说法正确的是( )
CH3OH(g) 达到平衡。下列说法正确的是( )
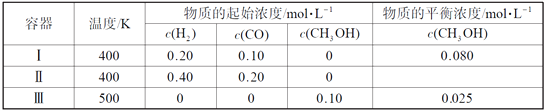
A. 该反应的逆反应放热
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C. 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 1mol苯乙烯中含碳碳双键数为4NA
B. 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5mol
C. 标准状况下,2.24LCl2溶于水,转移6.02×1022个电子
D. 1L0.1molL-1的氨水中有0.1NA个NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com