
A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如右图所示(部分产物已略去)。
(1)若A为金属单质,D是某强酸的稀溶液,则反应B+A→C的离子方程式为 。
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则反应 A+D→B的离子方程式为 。
(3)若A为强碱,D为气态酸性氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如图a或图b所示(不考虑D的溶解和水的挥发)。
①若图a符合事实,则D为 (填化学式),此时图a中x 7(填“>”“<”或“=”)
②若图b符合事实,且图b中y<7,B的焰色反应为黄色,则B溶液中各离子浓度由大到小的顺序是 。
(8分)
(1)2Fe3+ +Fe=3Fe2+(2分)
(2)Al3++4OH-= [Al(OH)4]- (2分)
(3)①CO2 (1分);> (1分)②c(Na+)> c(HSO3-)> c(H+)> c(SO32-)> c(OH-)(2分)
解析试题分析:
(1)A为金属单质,D是某强酸的稀溶液,推出A为Fe、D是稀硝酸,B是硝酸铁,B+A→C的离子方程式为2Fe3+ +Fe=3Fe2+。
(2)A、B为盐,D为强碱,A的水溶液显酸性,推出A为AlCl3,D为NaOH等强碱。
(3)①图中pH不随时间变化,A为强碱,D为气态酸性氧化物,推出A为NaOH等强碱,D为CO2。B溶质应为碳酸氢钠,由于水解溶液的pH>7。②溶液的pH<7,且氧化后酸性增强,溶质应为亚硫酸氢钠。HSO3-的电离程度大于水解程度,所以c(Na+)> c(HSO3-)> c(H+)> c(SO32-)> c(OH-)。
考点:考查物质推断、元素及其化合物性质、溶液中离子浓度判断等相关知识。


科目:高中化学 来源: 题型:推断题
如图所示的无机物的转化关系中,部分生成物和反应条件已略去。其中A与F是两种酸式盐;常温下B、C、Y、Z是气体,且B能使Z的水溶液褪色;E是一种常见的化肥;X中含有20个电子。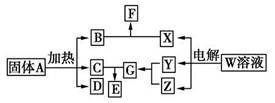
(1)写出X的电子式:________________ ;E中含有的化学键类型是________________。
(2)Z与C以物质的量之比3?1反应也能生成G,同时生成另一种二元化合物H,已知该反应中只有一种元素的化合价发生改变,则H的化学式为________________。H大量用于面粉的漂白和消毒,它与水反应的化学方程式为________________。
(3)将体积均为560 mL(标准状况)的B和Z同时缓缓通入水中,得到1.0 L溶液,则溶液中c(H+)=________mol/L。
(4)A~G七种物质中,属于电解质的有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
由五种短周期主族元素组成的单质及化合物(或其溶液),它们的转化关系如下图所示。其中,A、B、C、D、E为单质,常温下A为固体,B、C、D、E为气体;G的焰色反应为黄色;D和E的反应在工农业生产中有重要的意义;K为G和I反应的产物之一。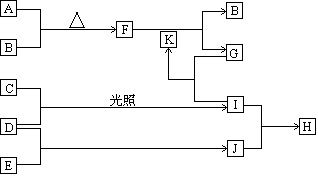
(1)写出五种单质的名称
(2)I、J相遇反应生成H,反应的现象是 ,化学反应方程式为 ,H物质的电子式为
(3)F的颜色为 ,F和K反应的化学方程式为 。
(4)G和H也可以发生反应,若G和H恰好完全反应,则A、B、C、D、E的物质的量之比为 。
(5)D和E的反应是典型的可逆反应,并且是放热反应。该反应的化学方程式为
请用某两种物质的反应速率间的等量关系表明该反应已经达到化学平衡,该等量关系可以是 ;反应物的总能量E反与生成物的总能量E生的大小关系是:E反 E生。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
已知:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素。其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;G原子核外最外层电子数与B相同,其余各层均充满。B、E两元素组成化合物B2E的晶体为离子晶体。C、F的原子均有三个能层,C原子的第一至第四电离能(kJ/mol)分别为:578、1817、2745、ll575;C与F能形成原子数目比为1:3、熔点为190℃的化合物Q。
(1)B的单质晶体为体心立方堆积模型,其配位数为 ;E元素的最高价氧化物分子的立体构型是 。F元素原子的核外电子排布式是 ,F的高价离子与A的简单氢化物形成的配离子的化学式为 .
(2)试比较B、D分别与F形成的化合物的熔点高低并说明理由 。
(3)A、G形成某种化合物的晶胞结构如图所示 。若阿伏伽德罗常数为NA,该化合物晶体的密度为 a g/cm3,其晶胞的边长为 cm。
。若阿伏伽德罗常数为NA,该化合物晶体的密度为 a g/cm3,其晶胞的边长为 cm。
(4)在1.0l×105 Pa、t1℃时,气体摩尔体积为53.4 L/mol,实验测得Q的气态密度为5.00g/L,则此时Q的组成为(写化学式) 。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
A、B、C、D均是短周期元素,A和B同周期, B和C同族,A元素族序数是周期数的三倍,B原子最外层电子数是内层电子数的二倍,B与A能生成化合物BA2,C与A生成化合物CA2, A的阴离子与D的阳离子电子层结构相同,都与氖原子的电子层结构相同,D 的单质与A 的单质在不同条件下反应,可生成D2A或D2A2。请回答
(1)写出元素符号A: ,B: ,C: 。
(2)D2A的电子式 ,BA2的结构式 。
(3)D2A2的化学式 ,灼烧这化合物火焰呈 色。
(4)C在元素周期表中的位置是 ,其原子结构示意图为 。
(5)比较A、B气态氢化物的沸点 ;原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
14分)A~J分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物, A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置是 ;
(2)检验C溶液中阳离子方法是(写出操作,现象及结论)
;
(3)写出反应①化学方程式: ;
(4)写出反应④离子方程式: ;
(5)写出反应⑥化学方程式: ;
(6)写出反应③阳极的电极反应式: ;
(7)从能量变化角度看,反应①②③中,属于△H<0的反应是 (填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(15分)化合物F是合成治疗心血管病的重要药物——美多心安的中间体。其中一种合成路线如下:
回答下列问题:
(1)A的化学名称为 。 (2) B生成C的反应类型为 。
(3)由C生成D的化学方程式为: 。(4)E的分子式为 。
(5)F的结构简式为 。1mol F与足量金属钠反应产生的气体在标准状况下的体积为 。
(6)B有多种同分异构体,写出同时满足下列条件的B的所有同分异构体的结构简式 。
①既能发生银镜反应,又能发生水解反应。
②核磁共振氢谱图中4组吸收峰、且峰面积之比为1:2:6:3。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(27分)氨的合成原理为:N2(g)+3H2(g)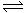 2NH3(g);△H= —92.4 KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如下图。回答下列问题:
2NH3(g);△H= —92.4 KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如下图。回答下列问题: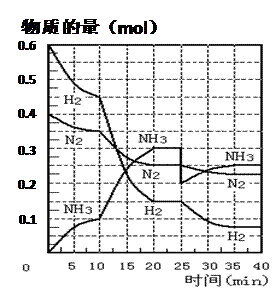
(1)10 min内以NH3表示的平均反应速率 ;
(2)在10 ~20 min内:NH3浓度变化的原因可能是 ;
| A.加了催化剂 | B.缩小容器体积 |
| C.降低温度 | D.增加NH3物质的量 |
 2NH3(g) +
2NH3(g) + 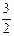 O2(g) ;△H =" a" kJ·mol—1
O2(g) ;△H =" a" kJ·mol—1| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
 2NH3(g) ΔH= -92 .4kJ·mol—1
2NH3(g) ΔH= -92 .4kJ·mol—1查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com