
14分)A~J分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物, A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置是 ;
(2)检验C溶液中阳离子方法是(写出操作,现象及结论)
;
(3)写出反应①化学方程式: ;
(4)写出反应④离子方程式: ;
(5)写出反应⑥化学方程式: ;
(6)写出反应③阳极的电极反应式: ;
(7)从能量变化角度看,反应①②③中,属于△H<0的反应是 (填序号)。
(每空2分)
(1)第四周期 第VIII族
(2)取少量C溶液滴加KSCN,溶液不显红色,再加氯水,溶液呈红色,证明是Fe2+
(3)8Al+3Fe3O4 4Al2O3+9Fe
4Al2O3+9Fe
(4)2Al+2H2O+2OH-=2AlO2-+3H2↑
(5)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(6)2O2--4e-=O2↑
(7)①②
解析试题分析:根据反应的流程图可知F是Fe(OH)3,E是Fe(OH)2,则A是Fe,B是Fe3O4,C是FeCl2,D是FeCl3,所以Fe元素在元素周期表中的位置是第四周期第VIII族;
(2)C中的阳离子是亚铁离子,检验其方法是取少量C溶液滴加KSCN,溶液不显红色,再加氯水,溶液呈红色,证明是Fe2+
(3)G为主族元素的固态氧化物,与氢氧化钠溶液反应,且电解得I也与氢氧化钠溶液反应,所以I是Al,G是Al2O3,H是氧气,J则是偏铝酸钠。反应①是铝热反应,化学方程式8Al+3Fe3O4 4Al2O3+9Fe;
4Al2O3+9Fe;
(4)反应④是Al与氢氧化钠溶液反应,离子方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑
(5)反应⑥是氢氧化亚铁在空气中变为氢氧化铁的反应,化学方程式为
4Fe(OH)2+O2+2H2O=4Fe(OH)3
(6)反应③是电解氧化铝,阳极是阴离子放电,电极反应式为2O2--4e-=O2↑
(7)从能量变化角度看,反应①②③中,铝热反应、燃烧反应都是放热反应,而电解反应是吸热反应,所以属于△H<0的反应是①②。
考点:考查物质的推断,离子的检验,化学方程式、离子方程式的书写,反应热效应的判断,物质性质的判断


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
用0.102 6 mol·L-1的盐酸滴定25.00 mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如下图所示,正确的读数为( )
| A.22.30 mL | B.22.35 mL | C.23.65 mL | D.23.70 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如右图所示(部分产物已略去)。
(1)若A为金属单质,D是某强酸的稀溶液,则反应B+A→C的离子方程式为 。
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则反应 A+D→B的离子方程式为 。
(3)若A为强碱,D为气态酸性氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如图a或图b所示(不考虑D的溶解和水的挥发)。
①若图a符合事实,则D为 (填化学式),此时图a中x 7(填“>”“<”或“=”)
②若图b符合事实,且图b中y<7,B的焰色反应为黄色,则B溶液中各离子浓度由大到小的顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E+原子核外有3层电子且各层均处于全满状态。
请填写下列空白。
(1)E元素基态原子的核外电子排布式为_________________。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为_____________(填元素符号),其原因为_____________________。
(3)B2A4是重要的基本石油化工原料。B2A4分子中B原子轨道的杂化类型为__________;
1 mol B2A4分子中含__________molσ键。
(4)已知D、E能形成晶胞如图所示的两种化合物,化合物的化学式,甲为__________,乙为_____________;高温时,甲易转化为乙的原因为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
短周期元素A、B、C、D、E原子序数依次增大。A是周期表中原子半径最小的元素,B原子的价电子数等于该元素最低化合价的绝对值,C与D能形成D2C和D2C2两种化合物,而D是同周期中金属性最强的元素,E的负一价离子与C和A形成的某种化合物分子含有相同的电子数。
(1)A、C、D形成的化合物中含有的化学键类型为 。
(2)已知:①E-E→2E·;△H=+a kJ·mol-1
② 2A·→A-A;△H=-b kJ·mol-1
③E·+A·→A-E;△H=-c kJ·mol-1(“·”表示形成共价键所提供的电子)
写出298K时,A2与E2反应的热化学方程式 。
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g) X(g);△H=-dJ·mol-1(d>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
X(g);△H=-dJ·mol-1(d>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 molA2、1 molBC | 1 molX | 4 molA2、2 molBC |
| 平衡时n(X) | 0.5mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 | α1 | α2 | α3 |

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(16分)下图中A、B、C、D、E、F、G均有机化合物。据图回答问题: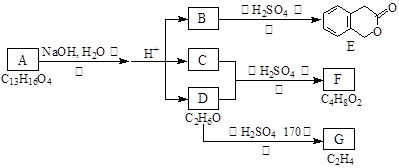
(1)D的化学名称是 。
(2)反应③的化学方程式是 。(有机物须用结构简式表示,下同)
(3)B的分子式是 ,A的结构简式是 。反应①的反应类型是 。
(4)符合下列3个条件的B的同分异构体的数目有多个。
i)含有邻二取代苯环结构、ii)与B有相同官能团、
iii)不与FeCl3溶液发生显色反应。
写出其中任意一个同分异构体的结构简式 。
(5)反应④的化学方程式是 。
G是重要的工业原料,用化学方程式表示G形成高聚物的反应
。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(本题共13分)
慢心律是一种治疗心律失常的药物,它的合成路线如下:
47.由B→C的反应类型为 。
48.写出A与浓溴水反应的化学方程式 。
49.由A制备B的过程中有少量副产物E,它与B互为同分异构体,E的结构简式为
。
50.写出同时满足下列条件的D的一种同分异构体的结构简式 。
①属于 -氨基酸;
-氨基酸;
②是苯的衍生物,且苯环上的一氯代物只有两种;
③分子中含有两个甲基。 51.已知乙烯在催化剂作用下与氧气反应可以生成环氧乙烷( )。写出以
51.已知乙烯在催化剂作用下与氧气反应可以生成环氧乙烷( )。写出以
邻甲基苯酚( )和乙醇为原料制备
)和乙醇为原料制备  的合成路线流程图(无机试剂任用)。
的合成路线流程图(无机试剂任用)。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
【化学—选修5:有机化学基础】(15分)
苯的同系物是人类最早认识的芳香族化合物,其中对二甲苯(英文名称p—xylene,缩写为PX)是化学工业的重要原料。
(1)写出PX的结构简式______________。
(2)PX可能发生的反应有_____ __、___ _____。(填反应类型,只填两种。)
(3)有机物M存在如下图所示的转化关系,其中A 是PX的一种同分异构体。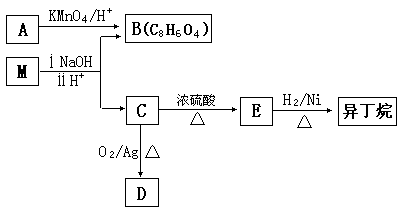
已知:M的分子式为C16H22O4,D能发生银镜反应。
①B的苯环上存在3 种不同化学环境的氢原子,则B 的结构简式是__________。
②D分子中所含的官能团是______________(填化学式)。
③M的结构简式是_______________。
(4)F是B 的一种同分异构体,具有如下特征:
a.是苯的对位二取代物;b.遇FeCl3溶液显示紫色;c.能与碳酸氢钠溶液反应。
写出F与NaHCO3溶液反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实验步骤 | 解释或实验结论 |
| ⑴称取A 9.0 g,升温使其汽化,测其密度是相同条件下H2的45倍。 | 试通过计算填空: ⑴A的相对分子质量为: 。 |
| ⑵将此9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g | ⑵A的分子式为: 。 |
| ⑶另取A 9.0 g,跟足量的NaHCO3粉末反应,生成2.24 L CO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况) | ⑶A中官能团的结构简式: 、 。 |
⑷A的核磁共振氢谱如下图: | ⑷A中含有 种氢原子 |
| ⑸综上所述,A的结构简式 。A与浓H2SO4混合,在一定条件下反应生成六元环状物B,B的结构简式 。 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com