
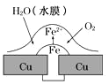
【题目】铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法正确的是
A.阳极电极反应式为:2H++2e→H2↑
B.此过程中铁做负极,被氧化
C.此过程中铜会被腐蚀,发生氧化反应
D.此过程中电子从Fe移向Cu,铁铆钉发生还原反应
【答案】B
【解析】
根据图片知,水中溶解了氧气,铜、铁和水构成了原电池,较活泼的金属作负极,较不活泼的金属作正极,发生吸氧腐蚀,负极上铁失电子发生氧化反应,正极上氧气得电子发生还原反应,原电池放电时,电子从负极流向正极。
根据图片知,水中溶解了氧气,铜、铁和水构成了原电池,较活泼的金属作负极,较不活泼的金属作正极,发生吸氧腐蚀。
A.该过程是吸氧腐蚀,正极上氧气得电子发生还原反应,电极反应式为:O2+2H2O+4e-=4OH-,A错误;
B.负极上Fe失去电子,发生氧化反应,电极反应式为:Fe-2e-=Fe2+,B正确;
C.该原电池中铜作正极,原电池放电时,负极Fe失电子容易被腐蚀,正极Cu被保护,所以铜不被腐蚀,C错误;
D.该原电池放电时,外电路上电子从负极铁流向正极铜,铁铆钉发生了氧化反应,D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】下列物质的工业制备原理的方程式书写正确的是
A.氢氧化钠:Na2CO3+Ca(OH)2![]() CaCO3↓+2NaOH
CaCO3↓+2NaOH
B.乙醇:C6H12O6![]() 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑
C.二氧化硫:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D.氯气:Ca(ClO)2+4HCl(浓)![]() CaCl2+2Cl2↑+2H2O
CaCl2+2Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名“![]() ” tián),Ts的原子核外最外层电子数是7,下列说法不正确的是
” tián),Ts的原子核外最外层电子数是7,下列说法不正确的是
A.TS是第七周期第VIIA族元素B.中子数为176的Ts核素符号是![]() Ts
Ts
C.Ts在同周期元素中金属性最弱D.Ts的同位素原子具有相同的电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)系统命名法给下列有机物命名:
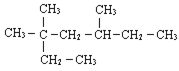 ______
______
(2)某烷烃的相对分子质量为114,该烷烃的化学式为______。
(3)完全燃烧0.2mol某烃,燃烧产物依次通过浓硫酸和碱石灰,实验结束后,称得浓硫酸增重18g,碱石灰增重35.2g。则:
①该烃的化学式__________;
②写出其可能的结构简式:__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S16O2与18O2在高温条件下发生反应2SO2+O2![]() 2SO3,达到化学平衡后,平衡混合物中含18O的微粒( )
2SO3,达到化学平衡后,平衡混合物中含18O的微粒( )
A. 只有SO3 B. 只有SO2、SO3 C. 有SO2、SO3、O2 D. 只有O2、SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在玻璃生产中,熔炉里原料发生的主要反应为:2Na2CO3+CaCO3+3SiO2![]() 2Na2SiO3+CaSiO3+3CO2↑。
2Na2SiO3+CaSiO3+3CO2↑。
(1)某反应物在熔融状态下不导电,它属于______晶体。
(2)上述反应里所涉及的短周期元素原子半径由大到小的顺序为________。
(3)碳和硅属于同族元素,该族元素的原子最外层电子的价层电子表示式为________。
(4)写一个能比较碳元素和氧元素非金属性强弱的化学反应方程式:________。
(5)CO2的电子式为_______。
(6)反应物Na2CO3与CaCO3均能制备二氧化碳,但是往往不是都能使用稀硫酸,请说明理由。______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢(H2S)的转化是资源利用和环境保护的重要研究课题。
(1)H2S和CO混合加热可制得羰基硫(COS)。已知羰基硫与CO2的结构相似,但它能在O2中完全燃烧。羰基硫可作粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。制备羰基硫反应方程式为:
CO(g)+H2S(g)![]() COS(g)+H2(g)
COS(g)+H2(g)
①羰基硫的电子式为_________
②羰基硫分子中三种原子半径由大到小的顺序________________
③羰基硫的沸点比二氧化碳_________(填“高或低”)理由是_____________________
④写出羰基硫在O2中完全燃烧的化学方程式__________________________________
(2)H2S具有还原性,在硫酸存在的条件下,能与KMnO4反应生成一种淡黄色沉淀,写出该反应的离子方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列氧化还原反应相关问题:
I.配平下面的氧化还原方程式:_______
___ Na2SO3+____ KIO3+____ H2SO4 =____ Na2SO4+____ K2SO4+____ I2+____ H2O
II.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为
![]() (浓)
(浓)![]()
![]() 。
。
(1)请分析该反应中电子转移的情况(用双线桥表示)_______________。
(2)浓盐酸在反应中显示出来的性质是________(填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
若标准状况下产生4.48L Cl2,则参加反应的KClO3的质量为_______g,被氧化的盐酸的物质的量为________mol,转移电子的物质的量为________mol。
(3)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是Cl2的________倍。(提示:ClO2与Cl2消毒时氯元素都被还原为最低价)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol的镁、铝混合物溶于100 mL 2mol/LH2SO4溶液中,然后再滴加1 mol/L NaOH溶液。请回答:
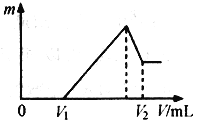
⑴若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。当V1=160mL时,则金属粉末中n(Mg)=______________mol,V2=______________mL。
⑵若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)_________mL。
⑶若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com