
����Ŀ���ں�����������ʼʱ�ݻ���Ϊ5L�ļס������ܱ�������(��Ϊ������������Ϊ��ѹ����)�������з�Ӧ��N2(g)+3H2(g)![]() 2NH3(g) ��H2=-92.4kJ/mol ���й����ݼ��ض�ƽ��״̬���±���
2NH3(g) ��H2=-92.4kJ/mol ���й����ݼ��ض�ƽ��״̬���±���
���� | ��ʼͶ�� | ��ƽ��ʱ | ||
�� | 2molN2 | 3molH2 | 0molNH3 | 1.5molNH3 |
�� | amolN2 | bmolH2 | 0molNH3 | 1.2molNH3 |
(1)��ƽ���ͬ�����ʵ����������ͬ����ʼʱ������ͨ���N2�����ʵ���Ϊ ����ʼʱ���е�ѹǿ�Ǽ������� �����ҵ�ƽ�ⳣ��Ϊ
(2)�����ܱ������п��Է��������ķֽⷴӦ����ƽ����ı��±��з�Ӧ����x�����и�����y��x�������������� (ѡ�����)��
a | b | c | d | |
x | �¶� | �¶� | ����H2�����ʵ��� | ���백�������ʵ��� |
y | ��������ƽ����Է������� | ƽ�ⳣ��K | ���������ܶ� | ��ƽ��ʱ������ת���� |
(3)�о���������������ʱ���ı���ʼ�����������ʵ����Է�Ӧ��Ӱ�죬ʵ������ͼ��ʾ(ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ���)��
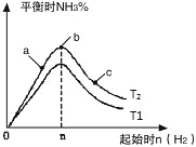
����T2��T1�Ĺ�ϵ�ǣ�T2 T1(����ڡ������ڡ������ڡ�����ȷ����)��
��a��b��c�����У�N2ת������ߵ��� (����ĸ)��
���������ݻ�Ϊ1L��T2������ʼ��ϵ�м���1molN2��3molH2������5min��Ӧ�ﵽƽ��ʱH2��ת����Ϊ60%����NH3�ķ�Ӧ����Ϊ ����������������䣬����ʼʱ�������ڷ���2molN2��6molH2����ƽ���ų�������ΪQ����Q_________110.88kJ(�>������<����=��)��
���𰸡�(1)1.6mol 0.8 107(mol/L)-2 (2) bc
(3) < b 0.24mol.L-1.min-1 >
��������
���������(1)�ס�������ʵ����ͬ�����ʵ����������ͬ��˵���ﵽ��ͬ��ƽ��״̬�����������V��![]() ��V=4L����������ʽ��
��V=4L����������ʽ��
�ף� N2+3H2![]() 2NH3��
2NH3��
��ʼ�� 2 3 0
�仯�� 0.75 2.25 1.5
ƽ���� 1.25 0.75 1.5
�ң� N2+3H2![]() 2NH3��
2NH3��
��ʼ�� a b 0
�仯�� 0.6 1.8 1.2
ƽ���� a-0.6 b-1.8 1.2
![]() ����a=1.6mol��
����a=1.6mol��![]() ����b=2.4mol��
����b=2.4mol��
��ʼʱ�������е�ѹǿ�Ǽ������ı���Ϊ��![]() ��
��
�ҵ�ƽ�ⳣ��k=![]() =107(mol/L)-2��
=107(mol/L)-2��
(2)a���÷�Ӧ�����ȷ�Ӧ�������¶�ƽ��������Ӧ�����ƶ���������������ʵ���������������������䣬ƽ����Է���������С����a����b��ƽ�ⳣ��ֻ���¶��йأ��¶ȸı�ƽ�ⳣ���ı䣬�����¶�ƽ��������Ӧ�����ƶ���ƽ�ⳣ������b��ȷ��c�������������������������������������䣬��������ܶ�����c��ȷ��d�����백����ƽ��������Ӧ�����ƶ�������ת���ʼ�С����d�����ʴ�Ϊbc��
(3)��Ϊ��ӦΪ���ȷ�Ӧ���¶�����ѧƽ���������ȷ�����У���T1��T2�����ﰱ���������ӣ�ƽ�����ƣ���T2��T1��
��b�����ƽ��״̬��c���ּ�������������ƽ�������ƶ���������ת��������
����ѧƽ������ʽ������ʽ���㣬
N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
��ʼ��(mol)1 3 0
�仯��(mol)0.6 3��60% 1.2
ƽ����(mol)0.4 1.2 1.2
��Ӧ����v=![]() =0.24mol��L-1��min-1����ʱ��Ӧ�ų�����=92.4kJ/mol��1.8/3=55.44KJ�����ƽ�����H2��ת����Ϊ60%ʱ�ų�������������ʼʱ�������ڷ���2mol N2��6mol H2���൱������ѹǿƽ��������У���Ӧ�ǿ��淴Ӧ���ܽ��г��ף��ų�����С��2��92.4kJ/mol=184.8KJ������H2��ת����Ϊ60%ʱ�ų���������2������������55.44KJ��2=110.88kJ��
=0.24mol��L-1��min-1����ʱ��Ӧ�ų�����=92.4kJ/mol��1.8/3=55.44KJ�����ƽ�����H2��ת����Ϊ60%ʱ�ų�������������ʼʱ�������ڷ���2mol N2��6mol H2���൱������ѹǿƽ��������У���Ӧ�ǿ��淴Ӧ���ܽ��г��ף��ų�����С��2��92.4kJ/mol=184.8KJ������H2��ת����Ϊ60%ʱ�ų���������2������������55.44KJ��2=110.88kJ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2CO(g)��O2(g)===2CO2(g) ��H����566 kJ��mol��1
Na2O2(s)��CO2(g)===Na2CO3(s)��![]() O2(g) ��H����226 kJ��mol��1
O2(g) ��H����226 kJ��mol��1
���������Ȼ�ѧ����ʽ�жϣ�����˵����ȷ����( )
A. CO��ȼ����Ϊ283 kJ
B. ��ͼ�ɱ�ʾ��CO����CO2�ķ�Ӧ���̺�������ϵ

C. 2Na2O2(s)��2CO2(s)===2Na2CO3(s)��O2(g) ��H>��452 kJ��mol��1
D. CO(g)��Na2O2(s)��Ӧ�ų�509 kJ����ʱ������ת����Ϊ6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ƽ�ⳣ��K��˵��������ȷ����
A�����κ�����������ѧƽ�ⳣ����һ���㶨ֵ
B���ı䷴Ӧ��Ũ�Ȼ�������Ũ�ȶ���ı�ƽ�ⳣ��K
C��ƽ�ⳣ��Kֻ���¶��й����뷴ӦŨ�ȡ�ѹǿ��
D����ƽ�ⳣ��K�Ĵ�С�����ƶ�һ����Ӧ���еij̶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ԫ���������Ա��ֵ�������������ɵ�һ��Ԫ�ء�����˵����ȷ����
A. ���ʶ��ܸ���ˮ���ϣ����ܱ�����ú����
B. �����ڿ�����ȼ��ʱ��������������
C. ���ʶ���������Ȼ�����ȶ�����
D. ����ʱ������ɫ����ɫ��Ӧ��Ӧ����ɫ�ܲ����۲�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������״̬�У�����֤�����淴ӦN2 + 3H2![]() 2NH3�Ѵ�ƽ��״̬��
2NH3�Ѵ�ƽ��״̬��
��һ��N��N�����ѵ�ͬʱ����3��H��H������
��һ��N��N�����ѵ�ͬʱ����6��N��H������
��������������ʱ����ϵѹǿ���ٸı�
�ܦ�(NH3)����(N2)�ͦ�(H2)�����ٸı�
�ݺ��º���ʱ���ܶȱ��ֲ���
�ަ���(H2)=0.03 mol��L-1��min-1������(NH3)=0.02 mol��L-1��min-1
A. ȫ�� B. �ڢۢܢ� C. �ۢܢݢ� D. �ڢۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������ԭ��Ӧ��������ȷ���ǣ� ��
A������������ԭ����ԭ��������
B���е��ʲμӻ����ɵķ�Ӧһ������������ԭ��Ӧ
C��ʧ�����ѵ����ʣ���õ��ӵ�����һ��ǿ
D��һ��Ԫ�ر��������϶�����һ��Ԫ�ر���ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ʱ��0.1mol/LijһԪ��HA��ˮ����0.1%�������룬���������������( )
A������Һ��pH=4
B������ĵ���ƽ�ⳣ��ԼΪ1��10-7
C�������¶ȣ���Һ��pH����
D����HA �������c(H+) ԼΪˮ�������c(H+) ��106��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����VL����MgSO4��K2SO4�Ļ����Һ�ֳ����ȷݣ�һ�ݼ��뺬amolNaOH����Һ��ǡ��ʹþ������ȫ����Ϊ������þ�������ݼ��뺬bmolBaCl2����Һ��ǡ��ʹ�����������ȫ����Ϊ���ᱵ����ԭ�����Һ�м����ӵ�Ũ��Ϊ �� ��
A�� ![]() B��
B�� ![]()
C�� ![]() D��
D�� ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ը����(������ʼ����0.4molK2CrO4)Ϊԭ�ϣ��绯ѧ���Ʊ��ظ���ص�ʵ��װ��ʾ��ͼ���£�����˵����ȷ����

A. �������ң�ͨ�����Һ���ɳ�ɫ��Ϊ��ɫ
B. ��·����0.2mol����ͨ��ʱ��������������Һ���ٵ�������Ϊ1.4g
C. �����������K��Cr�����ʵ���֮��Ϊ3:2����˹��̵�·�й�ת�Ƶ�����Ϊ0.1NA
D. ���ⶨ����Һ��K��Cr�����ʵ���֮��Ϊd�����ʱ����ص�ת����Ϊ2-d
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com