
【题目】下列实验结果不能作为相应定律或原理的证据之一的是( )
A | B | C | D | |
勒夏特列原理 | 元素周期律 | 盖斯定律 | 阿伏加德罗定律 | |
实验方案 |
|
|
|
|
结果 | 左球气体颜色加深 右球气体颜色变浅 | 烧瓶中冒气泡 试管中出现浑浊 | 测得 |
|
(B中试剂为浓盐酸、碳酸钠溶液、硅酸钠溶液)
A.AB.BC.CD.D
【答案】B
【解析】
A.![]() 是放热反应,升高温度,平衡向生成二氧化氮的方向移动,颜色变深,可以作为勒夏特列原理的证据之一;
是放热反应,升高温度,平衡向生成二氧化氮的方向移动,颜色变深,可以作为勒夏特列原理的证据之一;
B、比较元素的非金属性,应用元素最高价氧化物对应水化物的酸性比较,浓盐酸不是氯的最高价氧化物对应水化物,无法比较氯和碳的非金属性;生成的二氧化碳中含有HCl气体,氯化氢与二氧化碳都能与硅酸钠溶液反应生成硅酸沉淀,故也无法比较碳和硅的非金属性,不能证明元素周期律;
C、△H=△H1+△H2,化学反应的热效应只与起始和终了状态有关,与变化途径无关,可以证明盖斯定律;
D、在同温同压下,气体的体积比等于方程式的化学计量数之比等于气体的物质的量之比,电解水生成的氧气和氢气体积比等于物质的量之比,可以证明阿伏加德罗定律;
故答案为B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】关于化合物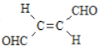 ,下列叙述正确的有( )
,下列叙述正确的有( )
A.分子间可形成氢键B.分子中既有极性键又有非极性键
C.分子中有7个![]() 键和1个
键和1个![]() 键D.C原子的杂化方式是sp2和sp3
键D.C原子的杂化方式是sp2和sp3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如右图所示。下列有关说法错误的是( )

A. d为石墨,铁片腐蚀加快
B. d为石墨,石墨上电极反应为:O2 + 2H2O + 4e == 4OH–
C. d为锌块,铁片不易被腐蚀
D. d为锌块,铁片上电极反应为:2H+ + 2e == H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分短周期元素原子的最外层电子数与原子序数的关系如图所示,下列说法正确的是 ( )
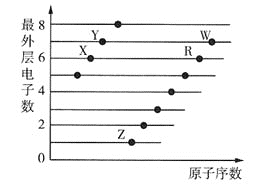
A.X、Y、Z、R、W五种元素的最高正化合价均等于其族序数
B.同周期元素中,W的电负性最大,Z的第一电离能最大
C.R、W所形成的氧化物的水化物的酸性强弱为![]()
D.X、Y、R、W四种元素形成的简单氢化物中最稳定的是Y的简单氢化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的分子式为![]() ,A属于第ⅥA族元素,B属于第ⅦA族元素,A和B在同一周期,它们的电负性分别为
,A属于第ⅥA族元素,B属于第ⅦA族元素,A和B在同一周期,它们的电负性分别为![]() 和
和![]() ,已知
,已知![]() 分子的键角为
分子的键角为![]() 。下列推断不正确的是
。下列推断不正确的是 ![]()
![]()
A.![]() 分子的空间构型为V形
分子的空间构型为V形
B.![]() 键为极性共价键,
键为极性共价键,![]() 分子为非极性分子
分子为非极性分子
C.![]() 分子中A原子采取
分子中A原子采取![]() 杂化
杂化
D.![]() 分子中无H原子,分子间不能形成氢键
分子中无H原子,分子间不能形成氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物同分异构体说法中错误的是
A. 三联苯(![]() )的一氯代物有4种
)的一氯代物有4种
B. 立方烷(![]() )经硝化可得到六硝基立方烷,其可能的结构有3种
)经硝化可得到六硝基立方烷,其可能的结构有3种
C. β-月桂烯(![]() )与溴发生1:1加成反应,产物(只考虑位置异构)有3种
)与溴发生1:1加成反应,产物(只考虑位置异构)有3种
D. 酯类化合物C4H8O2在酸性条件下水解得到的醇可能有4种不同结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用AG表示溶液的酸碱度,AG=![]() 。25℃,用0.100mol·L-1NaOH液滴定20.00 mL 0.100 mol·L-1 HNO2溶液, AG与所加NaOH溶液的体积(V)关系如图所示。下列说法不正确的是
。25℃,用0.100mol·L-1NaOH液滴定20.00 mL 0.100 mol·L-1 HNO2溶液, AG与所加NaOH溶液的体积(V)关系如图所示。下列说法不正确的是

A. D点溶液中的pH=11.25
B. B点溶液中存在2c(H+)-2c(OH-)=c(NO2-)-c(HNO2)
C. C点时,加入NaOH溶液的体积小于20.00 mL
D. 25℃时,HNO2的电离平衡常数Ka=1.0×10-5.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢分解反应过程中,能量变化如图所示:下列说法正确的是

A. 催化剂可以改变过氧化氢分解反应的焓变
B. CuCl2或FeCl3可以催化H2O2分解反应
C. 催化剂不能改变反应路径
D. H2O2分解是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中列出11种元素在周期表中的位置,按要求回答下列各题:
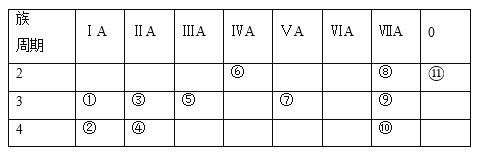
(1)这11种元素中,化学性质最不活泼的元素是______(填元素符号,下同),得电子能力最强的原子是______,失电子能力最强的单质与水反应的化学方程式__________。
(2)元素④的离子结构示意图为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com