
【题目】二氧化氯![]() 作为一种高效强氧化剂,已被联合国世界卫生组织
作为一种高效强氧化剂,已被联合国世界卫生组织![]() 列为AⅠ级安全消毒剂。常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定,温度过高或水溶液中
列为AⅠ级安全消毒剂。常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定,温度过高或水溶液中![]() 的质量分数高于
的质量分数高于![]() 等均有可能引起爆炸,易与碱液反应生成盐和水。
等均有可能引起爆炸,易与碱液反应生成盐和水。
![]() 某研究小组设计如图所示实验制备
某研究小组设计如图所示实验制备![]() 溶液,其反应的化学方程式为
溶液,其反应的化学方程式为![]() 。
。
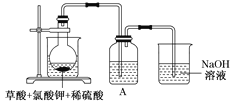
![]() 在反应开始之前将烧杯中的水加热到
在反应开始之前将烧杯中的水加热到![]() ,然后停止加热,并使其温度保持在
,然后停止加热,并使其温度保持在![]() 之间。控制温度的目的是___________,图中装置中缺少的一种必需的玻璃仪器是_______________________。
之间。控制温度的目的是___________,图中装置中缺少的一种必需的玻璃仪器是_______________________。
![]() 装置A用于溶解产生的二氧化氯气体,其中最好盛放________
装置A用于溶解产生的二氧化氯气体,其中最好盛放________![]() 填标号
填标号![]() 。
。
a.20mL60℃的温水 b.100mL冰水 c.100mL饱和食盐水 d.100mL沸水
![]() 在烧瓶中加入12.25gKClO3和9g草酸
在烧瓶中加入12.25gKClO3和9g草酸![]() ,然后再加入足量的稀硫酸,水浴加热,反应后生成
,然后再加入足量的稀硫酸,水浴加热,反应后生成![]() 的质量为________。
的质量为________。
![]() 用
用![]() 处理过的饮用水
处理过的饮用水![]() 为
为![]() 常含有一定量对人体不利的亚氯酸根离子
常含有一定量对人体不利的亚氯酸根离子![]() 。饮用水中
。饮用水中![]() 、
、![]() 的含量可用连续碘量法进行测定,实验步骤如下:
的含量可用连续碘量法进行测定,实验步骤如下:
步骤1:准确量取一定体积的水样加入锥形瓶中;
步骤2:调节水样的pH至![]() ;
;
步骤3:加入足量的KI晶体;
步骤4:加入少量指示剂,用一定浓度的![]() 溶液滴定至终点;
溶液滴定至终点;
步骤5:再调节溶液的![]() ;
;
步骤6:继续用相同浓度的![]() 溶液滴定至终点。
溶液滴定至终点。
![]() 步骤1中若要量取20.00mL水样,则应选用的仪器是____________________。
步骤1中若要量取20.00mL水样,则应选用的仪器是____________________。
![]() 步骤
步骤![]() 的目的是测定水样中
的目的是测定水样中![]() 的含量,其反应的化学方程式为2ClO2+2KI=2KClO2+I2,2Na2S2O3+I2=Na2S4O6+2NaI,则步骤4中加入的指示剂为______________,滴定达到终点时溶液的颜色变化为______________。
的含量,其反应的化学方程式为2ClO2+2KI=2KClO2+I2,2Na2S2O3+I2=Na2S4O6+2NaI,则步骤4中加入的指示剂为______________,滴定达到终点时溶液的颜色变化为______________。
![]() 步骤5的目的是使
步骤5的目的是使![]() 将溶液中的
将溶液中的![]() 还原为
还原为![]() 以测定其含量,该反应的离子方程式为____________________________。
以测定其含量,该反应的离子方程式为____________________________。
【答案】保证反应所需温度、防止温度过高发生爆炸 温度计 b 6.75g 25mL的酸式滴定管![]() 或20.00mL的移液管
或20.00mL的移液管![]() 淀粉溶液 蓝色褪去
淀粉溶液 蓝色褪去 ![]()
【解析】
![]() 由题目所给信息可知,
由题目所给信息可知,![]() 性质非常不稳定,温度过高,二氧化氯的水溶液有可能爆炸,应降低反应温度。实验中应用温度计控制温度,因为要确保在反应开始之前将烧杯中的水加热到
性质非常不稳定,温度过高,二氧化氯的水溶液有可能爆炸,应降低反应温度。实验中应用温度计控制温度,因为要确保在反应开始之前将烧杯中的水加热到![]() ,然后停止加热,另一个原因就是保证反应所需的温度,并使其温度保持在
,然后停止加热,另一个原因就是保证反应所需的温度,并使其温度保持在![]() 之间,所以必须要用温度计。
之间,所以必须要用温度计。
故答案为:保证反应所需温度、防止温度过高发生爆炸;温度计;
![]() 二氧化氯易溶于水,则可用水吸收,为防止温度过高或浓度过大而爆炸,应在低温下吸收,则b符合。
二氧化氯易溶于水,则可用水吸收,为防止温度过高或浓度过大而爆炸,应在低温下吸收,则b符合。
故答案为:b;
![]() ,
,![]() ,
,
根据方程式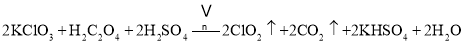 可知道,
可知道,![]() 过量,用
过量,用![]() 的量计算,则生成的
的量计算,则生成的![]() ,
,![]() 。
。
故答案为:![]() ;
;
![]() 根据题意水样pH为
根据题意水样pH为![]() ,呈酸性,且25mL与所量取的体积接近,故用25mL酸式滴定管或
,呈酸性,且25mL与所量取的体积接近,故用25mL酸式滴定管或![]() 的移液管。
的移液管。
故答案为:![]() 的酸式滴定管
的酸式滴定管![]() 或
或![]() 的移液管
的移液管![]() ;
;
![]() 根据题意可知滴定过程中出现了碘单质,碘遇淀粉变蓝,故选淀粉做指示剂;滴定到终点时,碘单质正好反应完,故滴定达到终点时溶液的颜色变化为溶液蓝色褪去。
根据题意可知滴定过程中出现了碘单质,碘遇淀粉变蓝,故选淀粉做指示剂;滴定到终点时,碘单质正好反应完,故滴定达到终点时溶液的颜色变化为溶液蓝色褪去。
故答案为:淀粉溶液;蓝色褪去;
步骤5的目的是用
![]() 将溶液中的
将溶液中的![]() 还原为
还原为![]() 以测定其含量,则
以测定其含量,则![]() 被氧化为
被氧化为![]() ,故该反应的离子方程式为
,故该反应的离子方程式为![]() 。
。
故答案为:![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同族,它们原子的最外层电子排布式为ns1。B和D也属同族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子的最外层电子数等于D原子的最外层电子数的一半。请回答下列问题:
(1)写出C元素基态原子的电子排布式: ________________ 。
(2)用电子排布图表示D元素原子的价电子:__________。
(3)元素B与D的电负性的大小关系是B___ D (填“>”“<”或“=”,下同), E与C的第一电离能大小关系是E____C。
(4)写出元素E和C的最高价氧化物对应的水化物之间反应的离子方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液氨与水性质相似,也存在微弱的电离:2NH3![]() NH4++NH2—,其离子积常数K=c(NH4+)·c(NH2—)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变的是
NH4++NH2—,其离子积常数K=c(NH4+)·c(NH2—)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变的是
A. 液氨的电离平衡 B. 液氨的离子积常数
C. c(NH4+) D. c(NH2—)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,AgX(X=Cl、Br)的溶度积与c(Ag+)和c(X-)的相互关系如下图所示,其中A线表示AgCl,B线表示AgBr,已知p(Ag+)=-lgc(Ag+),p(X-)=-lgc(X-)。下列说法正确的是( )

A. c点可表示AgCl的不饱和溶液
B. b点的AgCl溶液加入AgNO3晶体可以变成a点
C. t℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常数K=10-4
AgBr(s)+Cl-(aq)平衡常数K=10-4
D. t℃时,取a点的AgCl溶液和b点AgBr溶液等体积混合,会析出AgBr沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。Q点时欲使溶液恢复到起始状态,可向溶液中加入
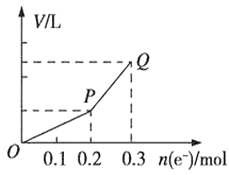
A. 0.1 mol CuO
B. 0.1 mol CuCO3
C. 0.1 mol Cu(OH)2
D. 0.05 mol Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰化物有剧毒,冶金工业会产生大量含氰化物的废水,其中氰化物以CN-等形式存在于废水中。某化学小组同学对含氰化物废水处理进行研究。
Ⅰ.查阅资料:含氰化物的废水处理方法。
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。
Ⅱ.实验验证:处理CN-的效果。
化学兴趣小组的同学在密闭系统中用如图装置进行实验,以测定CN-被处理的百分率,实验步骤如下:
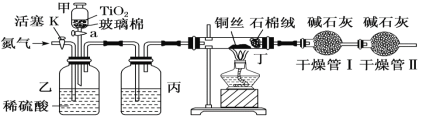
步骤1:取一定量废水进行加热蒸发、浓缩。
步骤2:取浓缩后含CN-的废水与过量NaClO溶液的混合液共200 mL(设其中CN-的浓度为0.2 mol·L-1)倒入甲中,塞上橡皮塞。
步骤3:点燃酒精灯对丁装置加热。
步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞。
步骤5:打开活塞K,通一段时间N2,关闭活塞K。
步骤6:实验完成后测定干燥管Ⅰ(含碱石灰)的质量m2[实验前干燥管Ⅰ(含碱石灰)的质量m1]。
回答下列问题:
(1)在处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式为:___________。
(2)对丁装置加热放在步骤3进行的原因是:___________。
(3)丙装置中的试剂是:___________。
(4)装置中石棉绒作用为:___________。
(5)干燥管Ⅱ的作用是:_____________________________。
(6)请简要说明实验中通入N2的目的是:______________________________。
(7)若干燥管Ⅰ中碱石灰增重1.408 g,则该实验中测得CN-被处理的百分率为:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化阿托醛![]() 是一种重要的化工原料,其合成路线如下:
是一种重要的化工原料,其合成路线如下:
(1)氢化阿托醛被催化氧化后的含氧官能团的名称是____________.
(2)在合成路线上②③的反应类型分别为②_____________③________________.
(3)反应④发生的条件是_____________________.
(4)由![]() 反应的化学方程式为_______________________________
反应的化学方程式为_______________________________
(5)1mol氢化阿托醛最多可和____mol氢气加成,1mol氢化阿托醛发生银镜反应可生成________molAg.
(6)D与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,则X的结构简式为________.D有多种同分异构体,能满足苯环上有两个取代基,且能使FeCl3溶液显紫色的同分异构体有______种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据杂化轨道理论和价层电子对互斥模型,判断下列分子或者离子的空间构型正确的是 ( )
选项 | 分子式 | 中心原子杂化方式 | 价层电子对互斥模型 | 分子或离子的立体构型 |
A | SO2 | sp | 直线形 | 直线形 |
B | H2O | sp2 | 平面三角形 | V形 |
C | NH3 | sp2 | 三角锥形 | 三角锥形 |
D | CH4 | sp3 | 正四面体形 | 正四面体形 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体完全燃烧后所得CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列对混合烃的判断正确的是:
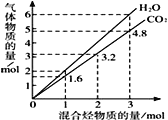
①一定有乙烯 ②一定有甲烷 ③一定有丙烷 ④一定没有乙烷⑤可能有甲烷 ⑥可能有乙炔(C2H2)
A. ②④ B. ②③⑥ C. ②⑥ D. ①③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com