
【题目】Ⅰ.铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
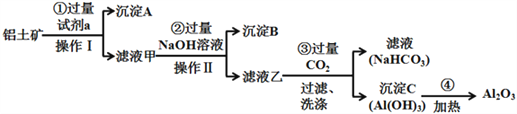
(1)沉淀A的成分是(填化学式)_________。
(2)步骤②中加入过量NaOH溶液发生反应的离子方程式,除了H++OH﹣=H2O外,还有:
_____________________________、________________________________;
(3)步骤③中加入(或通入)的过量试剂b是______________。
Ⅱ. 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
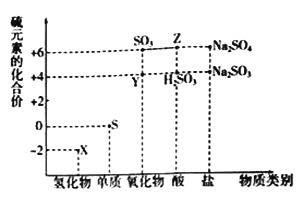
(4)从硫元素化合价的角度分析,图中既有氧化性又有还原性的化合物有______________(填化学式)。
(5)将X与Y混合,可生成淡黄色固体,该反应的化学方程式为_________________________。
(6)Na2S2O3是重要的化工原料,从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是______(填代号).
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
【答案】SiO2 Fe3++3OH﹣=Fe(OH)3↓ Al3++4OH﹣=AlO2﹣+2H2O CO2 SO2、H2SO3、Na2SO3 SO2 +2 H2S = 3S↓ + 2H2O b
【解析】
Ⅰ.铝土矿中加入过量试剂a,然后操作I得到沉淀A和滤液甲,则操作I为过滤,滤液甲中加入过量NaOH溶液经操作II后得到沉淀B和滤液乙,操作II是过滤;Al2O3、SiO2能溶于强碱溶液而Fe2O3不溶于强碱溶液,SiO2不溶于稀盐酸而Fe2O3、Al2O3能溶于稀盐酸,根据图知,滤液甲中含有铝元素,则试剂a为稀盐酸,沉淀A为SiO2,滤液甲中溶质为氯化铝和氯化铁、HCl,沉淀B为Fe(OH)3,滤液乙中含有NaAlO2和NaOH、NaCl,向滤液乙中通入过滤二氧化碳得到滤液为碳酸氢钠溶液,沉淀C为Al(OH)3,加热氢氧化铝得到氧化铝。
Ⅱ.(4)S元素的化合价有-2价、0价、+4价、+6价,具有中间价态的元素既有还原性又有氧化性;
(5)将H2S与SO2混合,可生成淡黄色固体,是利用二氧化硫的氧化性氧化硫化氢生成淡黄色沉淀S和水,元素化合价降低的物质为氧化剂;
(6)Na2S2O3中S为+2价,从氧化还原反应的角度分析,反应物中S元素化合价必须分别大于2和小于2;
Ⅰ.(1)通过以上分析知,A、B、a分别是SiO2、Fe(OH)3、盐酸,故沉淀A的成分是SiO2;
(2)步骤②中加入过量NaOH溶液后,稀盐酸、铁离子、铝离子都和NaOH溶液反应,发生反应的离子方程式除H++OH-=H2O外,还有Fe3++3OH-=Fe(OH)3↓、 Al3++4OH﹣=AlO2﹣+2H2O(或Al3++4OH-=[Al(OH)4]-);
(3)过量的稀盐酸能溶解生成的氢氧化铝而得不到氢氧化铝,步骤③中通入过量CO2气体而不加入过量盐酸。
Ⅱ.(4)具有中间价态的元素既有还原性又有氧化性,S元素的化合价有-2价、0价、+4价、+6价,所以0价和+4价S的化合物既有还原性又有氧化性,即SO2,H2SO3、Na2SO3;
(5)X为H2S,与SO2混合可生成淡黄色固体,是利用二氧化硫的氧化性氧化硫化氢生成淡黄色沉淀S和水,2H2S+SO2=3S↓+2H2O;
(6)Na2S2O3中S为+2价,从氧化还原反应的角度分析,反应物中S元素化合价必须分别大于2和小于2,a中S化合价都小于2,c、d中S的化合价都大于2,b符合题意。


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】下列关于主族元素的说法正确的是( )
A.主族元素的原子核外电子最后填入的能级是s能级
B.主族元素的原子核外电子最后填入的能级是s能级或p能级
C.所有主族元素的最高正价都等于主族序数
D.主族元素的价电子数有可能超过最外层电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 若H2O2分解产生1molO2,理论上转移的电子数约为4×6.02×1023
B. 室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,溶液pH>7
C. 钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其腐蚀
D. 一定条件下反应N2+3H22NH3达到平衡时,3v正(H2)=2v逆(NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关溶液的说法正确的是( )
A. pH相等的①NH4Cl、②NH4Al(SO4)2、③NH4HSO4溶液:浓度的大小顺序为①>②>③
B. HA的电离常数Ka =4.93×1010,则等浓度的NaA、HA混合溶液中:c(Na+) >c(HA) >c(A)
C. NaHCO3溶液加水稀释,c(Na+)与c(HCO3)的比值将减小
D. 已知在相同条件下酸性HF >CH3COOH,则物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+) – c(F) >c(K+ ) c(CH3COO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是合成抗炎药洛索洛芬钠的关键中间体,它的一种合成路线如下:
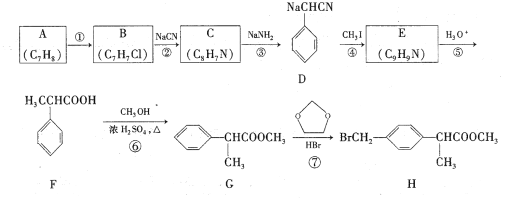
回答下列问题:
(1)A的名称是____,H中官能团名称是____;
(2)反应①的反应条件为____;
(3)反应⑥的化学方程式为________;反应类型为____。
(4)反应⑦除生成H外,还生成了另一种有机产物的结构简式为____。
(5)符合下列条件的G的同分异构体有____种。
I.能发生银镜反应 Ⅱ.苯环上一氯取代物只有一种 Ⅲ.核磁共振氢谱有4组峰
(6)仿照H的合成路线,设计一种由B合成![]() 的合成路线___。
的合成路线___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.电离时能生成H+的化合物是酸
B.水溶液显碱性的物质是碱
C.电解质电离时产生的阴离子全部是OH-的化合物是碱
D.能与碱发生反应生成水的化合物是酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“碳捕捉技术”常用于去除或分离气流中的二氧化碳。
Ⅰ.2017年,中国科学家在利用二氧化碳直接制备液体燃料领域取得了突破性进展,其中用二氧化碳制备甲醇(CH3OH)的反应如下图:
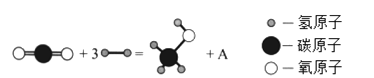
(1)A的化学式为_________。
(2)该反应说明CO2具有___________性(填“氧化”或“还原”)。若有1mol甲醇生成,转移电子的物质的量为_________________mol。
Ⅱ.利用NaOH溶液“捕提"CO2的基本过程如下图(部分条件及物质已略去):
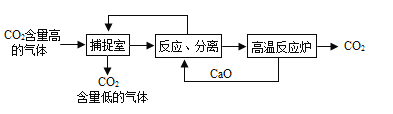
(1)反应分离室中,发生反应的化学方程式分别为CaO+H2O=Ca(OH)2和__________________
(2)高温反应炉中,涉及反应的化学反应类型为_______________________。
(3)整个过程中,可以循环利用物质的化学式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)有机物M的合成路线如下图:
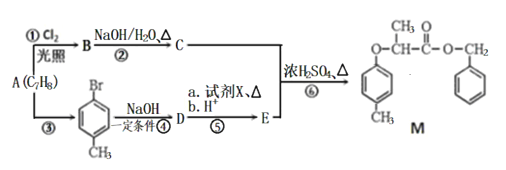
已知:i: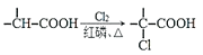 ii:
ii: 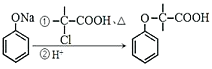
(1)M中含氧官能团的名称有醚键和___________,C的名称为___________,步骤⑥的反应类型为___________。
(2)步骤④反应的化学方程式为_________________________________。
(3)试剂X的结构简式为___________。
(4)同时满足下列条件,E的同分异构体有__________种。
I.能与FeCl3溶液发生显色反应;II.能发生水解反应和银镜反应;III.苯环上只有两个取代基。
其中核磁共振氢谱峰面积比为1:1:2:2:6的分子的结构简式为: ______________________。
(5)根据以上信息,写出以![]() 为原料制取
为原料制取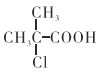 的合成路线图 (无机试剂一定要选银氨溶液,其它无机试剂任选)____________________________________________。合成路线图示例:CH2=CH2
的合成路线图 (无机试剂一定要选银氨溶液,其它无机试剂任选)____________________________________________。合成路线图示例:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
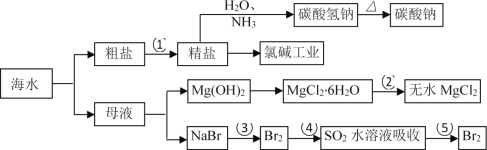
已知:MgCl2 · 6H2O 受热生成 Mg(OH)Cl 和 HCl 气体等。下列有关说法正确的是( )
A. 工业上将石灰水加入到海水中得到 Mg(OH)2 沉淀
B. 在过程②中将 MgCl2 · 6H2O 灼烧即可制得无水 MgCl2
C. 在第③、④、⑤步骤中,溴元素均被氧化
D. 制取 NaHCO3 的反应是利用其溶解度小于 NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com