
����Ŀ��һ���¶��£������Ϊ2L�ĺ������չ���������Ӧ��4A(g)+bB(s)cC(g) ��H=-QkJ��mol-1(Q��0)����Ӧ�����еIJ����������±���ʾ��
n/(mol) t/min | n(A) | n(B) | n(C) |
0 | 4.0 | 1.0 | 0 |
2 | 0.6 | 0.2 | |
4 | 0.4 | ||
6 | 2.8 | 0.3 |
����˵����ȷ���ǣ� ��
A.t=2minʱ��c(A)=3.2mol��L-1
B.��Ӧ��ʼ����tȡ��ֵ��A��B��ת���ʾ����������
C.��Ӧ�ﵽƽ��״̬ʱ����B��ʾ��ƽ����Ӧ����Ϊ0.075mol��L-1��min-1
D.t=6minʱ����Ӧ�ų�������Ϊ0.6Q
���𰸡�B
��������
A��t=2minʱ��n(B)=0.6mol��n(C)=0.2mol����n(B)=0.4mol��n(C)=0.2mol�����ʵ����仯��֮�ȵ��ڼ���ϵ��֮�ȣ�n(B)��n(C)=b��c=0.4��0.2=2��1���������������������ӦΪ��4A(g)+2B(s)C(g)���ɵã�n(A)=4��0.2mol=0.8mol����t=2minʱ��n(A)=4mol-0.8mol=3.2mol��c(A)=![]() mol��L-1����A����
mol��L-1����A����
B����ʼA��B�����ʵ���֮��Ϊ4��1������A�������A��B�����ĵ����ʵ���֮��Ϊ2��1����tȡ��ֵ��A��B��ת���ʾ���������ȣ���B��ȷ��
C�����ݷ�Ӧ4A(g)+2B(s) C(g)��BΪ���壬����������ʾ�÷�Ӧ�ķ�Ӧ���ʣ���C����
D�����ݷ�Ӧ��4A(g)+2B(s)C(g) ��H=-QkJ��mol-1��֪����Ӧ��ȫ��������1molCʱ�ų�������ΪQkJ��t=6minʱ���ÿ��淴Ӧ����C�����ʵ���Ϊ0.3mol����Ӧ�ų�������Ϊ0.3Q����D����
��ѡB��


 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵������ȷ����(����)
A. 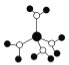 ˮ��ͭ���ӵ�ģ����ͼ��ʾ��1��ˮ��ͭ��������4����λ��
ˮ��ͭ���ӵ�ģ����ͼ��ʾ��1��ˮ��ͭ��������4����λ��
B. 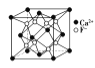 CaF2����ľ�����ͼ��ʾ��ÿ��CaF2����ƽ��ռ��4��Ca2��
CaF2����ľ�����ͼ��ʾ��ÿ��CaF2����ƽ��ռ��4��Ca2��
C.  Hԭ�ӵĵ�����ͼ��ͼ��ʾ��Hԭ�Ӻ���Ĵ����������ԭ�Ӻ˸����˶�
Hԭ�ӵĵ�����ͼ��ͼ��ʾ��Hԭ�Ӻ���Ĵ����������ԭ�Ӻ˸����˶�
D.  ����Cu��Cuԭ�Ӷѻ�ģ����ͼ��ʾ���ý�������Ϊ���ܶѻ���ÿ��Cuԭ�ӵ���λ����Ϊ12
����Cu��Cuԭ�Ӷѻ�ģ����ͼ��ʾ���ý�������Ϊ���ܶѻ���ÿ��Cuԭ�ӵ���λ����Ϊ12
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУѧ������ͼ��ʾװ�ý���ʵ�飬��̽�������巢����Ӧ��ԭ���������ᴿ��Ӧ�IJ����ش��������⣺

��1��װ��(��)�з�����Ӧ�Ļ�ѧ����ʽΪ 2Fe+3Br2 �T2FeBr3��________ ��
��2��ʵ�鿪ʼʱ���ر� K2������ K1�ͷ�Һ©���������μӱ���Һ��Ļ��Һ�� ����С�Թ��ڱ���������___________��
��3����˵������Һ�巢����ȡ����Ӧ��������___________��
��4����Ӧ������Ҫ��װ��I�е�ˮ������װ�����У�����������Ŀ����___________��������һ�����ķ�����___________ ��
��5���ĸ�ʵ��װ���������������õ�װ����___________��
��6����װ��(��)��Ӧ���Һ�����ν�������ʵ������Ϳɵõ��ϴ������屽��
��������ˮϴ�ӣ�����Һ�� ����5%��NaOH��Һϴ�ӣ�����Һ��
��������ˮϴ�ӣ�����Һ�� ��������ˮCaCl2��ĩ�����________����������ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ2L���ܱ������н������·�Ӧ��A(g)+2B(g)![]() 3C(g)+nD(g)����ʼʱAΪ4mol��BΪ6mol��5minĩʱ���C�����ʵ���Ϊ3mol����D��ʾ�Ļ�ѧ��Ӧ����v(D)Ϊ0.2mol/(L��min)������:
3C(g)+nD(g)����ʼʱAΪ4mol��BΪ6mol��5minĩʱ���C�����ʵ���Ϊ3mol����D��ʾ�Ļ�ѧ��Ӧ����v(D)Ϊ0.2mol/(L��min)������:
(1)5minĩA�����ʵ���Ũ��Ϊ________��
(2)ǰ5min����B��ʾ�Ļ�ѧ��Ӧ����v(B)Ϊ________��
(3)��ѧ����ʽ��nֵΪ________��
(4)�˷�Ӧ�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��
��v(A)=5mol/(L��min)
��v(B)=6mol/(L��min)
��v(C)=4.5mol/(L��min)
��v(D)=8mol/(L��min)
���з�Ӧ����������________�����ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ȣ�ClO2����һ�ֻ���ɫ���壬������ˮ���ڻ�������е������������10���Ϳ��ܷ�����ը���ڹ�ҵ�ϳ�����ˮ��������Ư�����ش��������⣺
(1)�ڴ�����ˮʱ��ClO2�ɽ���ˮ�е�CN��������CO2��N2���÷�Ӧ�����ӷ���ʽ��_______��
(2)ijС�鰴���������Ʊ�ClO2�ķ����������ͼ��ʾ��ʵ��װ�������Ʊ�ClO2��
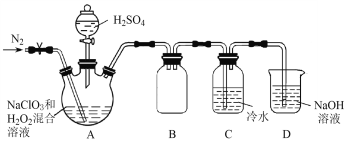
��ͨ�뵪������Ҫ������2����һ�ǿ����������ã�����____________________��
��װ��B��������__________________��
��װ��A��������ClO2���壬�÷�Ӧ�Ļ�ѧ����ʽ��_______________________________��
(3)�ⶨװ��C��ClO2��Һ��Ũ�ȣ�ȡ10.00 mL C����Һ����ƿ�У�����������KI��Һ��H2SO4�ữ��Ȼ�����___________________��ָʾ������0.100 0 mol![]() L��1��Na2S2O3��Һ�ζ���ƿ�е���Һ��I2 + 2S2O32����2I��+ S4O62���������ı���Һ�����Ϊ20.00 mL���ζ��յ��������______________________________��C��ClO2��Һ��Ũ����__________mol
L��1��Na2S2O3��Һ�ζ���ƿ�е���Һ��I2 + 2S2O32����2I��+ S4O62���������ı���Һ�����Ϊ20.00 mL���ζ��յ��������______________________________��C��ClO2��Һ��Ũ����__________mol![]() L��1��
L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҺX�п��ܺ���NO3-��Cl-��SO42-��CO32-��NH4+��Fe2+��Fe3+�еļ��֣������������ӵ����ʵ�����ȡ�Ϊȷ������Һ�ijɷ֣�ijѧϰС����������ʵ�飺

������˵����ȷ���ǣ� ��
A.�������ʹʪ�����ɫʯ����ֽ��죬��������ʹ����ʯ��ˮ�����
B.Fe2+��Fe3+���ܶ����ڣ�SO42-��NH4+һ������
C.������Fe3+����һ������Cl-
D.����Һ��ֻ�������������е�NO3-��SO42-��NH4+��Fe2+��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���һ��1L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ���д���пհף�

��1���ӿ�ʼ��2min��X��ƽ����Ӧ����Ϊ__________��
��2���÷�Ӧ�Ļ�ѧ����ʽΪ_______________________��
��3��1minʱ�����淴Ӧ���ʵĴ�С��ϵΪ��v������_____v���棩��2minʱ��v������_____v���棩�����>����<����=����
��4����X��Y��Z��Ϊ���壬��2minʱ����������ͨ�������������ϵѹǿ��X�Ļ�ѧ��Ӧ���ʽ�______���������ʺϵĴ�����Y�Ļ�ѧ��Ӧ���ʽ�______���������䡱��С����
��5����X��Y��Z��Ϊ���壬������˵����Ӧ�Ѵ�ƽ�����_____________��
a��X��Y��Z���������Ũ�����
b�������������ʵ������ٸı�
c����Ӧ�Ѿ�ֹͣ
d����Ӧ����v��X���Uv��Y��=2��1
e������λʱ��������X�����ʵ�����������λʱ��������Z�����ʵ�����=3:2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С�����ü״�ȼ�ϵ�ؽ������µ��ʵ�飬���м׳ص��ܷ�ӦʽΪ2CH3OH+3O2+4KOH=2K2CO3+6H2O������˵������ȷ����

A. �׳���ͨ��CH3OH�ĵ缫��Ӧ��CH3OH-6e-+8OH-=CO32-+6H2O
B. �׳�������560mLO2����״���£��������ҳ�Ag�缫����3.2g
C. ��Ӧһ��ʱ������ҳ��м���һ����Cu(OH)2���壬��ʹCuSO4��Һ�ָ���ԭŨ��
D. �����Ҳ�Pt�缫�ĵ缫��Ӧʽ��Mg2++2H2O+2e-=Mg(OH)2��+H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��B��[ʵ�黯ѧ]
��Ȳ�������![]() ����һ����Ҫ���л�����ԭ�ϣ��е�Ϊ103~105 �档ʵ�����Ʊ�������Ȳ������ķ�ӦΪ
����һ����Ҫ���л�����ԭ�ϣ��е�Ϊ103~105 �档ʵ�����Ʊ�������Ȳ������ķ�ӦΪ
![]()
ʵ�鲽�����£�
����1���ڷ�Ӧƿ�У�����14 g��Ȳ�ᡢ50 mL�״���2 mLŨ���ᣬ���裬���Ȼ���һ��ʱ�䡣
����2�����������ļ״���װ�ü���ͼ����
����3����ӦҺ��ȴ�������ñ���NaCl��Һ��5%Na2CO3��Һ��ˮϴ�ӡ�������л��ࡣ
����4���л��ྭ��ˮNa2SO4������ˡ����ñ�Ȳ�������

��1������1�У���������״���Ŀ����________��
��2������2�У���ͼ��ʾ��װ��������A��������______��������ƿ�м������Ƭ��Ŀ����______��
��3������3�У���5%Na2CO3��Һϴ�ӣ���Ҫ��ȥ��������____��������л���IJ�������Ϊ____��
��4������4�У�����ʱ������ˮԡ���ȵ�ԭ����________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com