
【题目】下列关于二氧化硅的说法中,错误的是
A. 二氧化硅和二氧化碳在物理性质上有很大的差别
B. 二氧化硅分子由一个硅原子和两个氧原子构成
C. 工业上用二氧化硅制粗硅
D. 二氧化硅既能与氢氟酸反应,又能与烧碱反应,但它不是两性氧化物
科目:高中化学 来源: 题型:
【题目】石墨炸弹爆炸时,能在方圆几百米范围内撒下大量的石墨纤维,造成输电线、电厂设备损坏。这是由于石墨
A. 有剧毒 B. 易燃、易爆 C. 能导电 D. 有放射性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液既能溶解Al(OH)3 , 又能溶解H2SiO3 , 在该溶液中可以大量共存的离子组是( )
A.K+、Na+、HCO ![]() 、NO
、NO ![]()
B.Na+、SO ![]() 、Cl﹣、ClO﹣
、Cl﹣、ClO﹣
C.H+、Mg2+、SO ![]() 、NO
、NO ![]()
D.Ag+、K+、NO ![]() 、Na+
、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某药物具有抗痉挛作用,制备该药物其中一步反应为: 
下列说法不正确的是( )
A.a中参加反应的官能团是羧基
B.生活中b可作燃料和溶剂
C.c极易溶于水
D.该反应类型为取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和CrO42-,浓度均为0.010mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
A. Br-、Cl-、CrO42- B. Cl-、Br-、CrO42-
C. CrO42-、Br-、Cl- D. Br-、CrO42-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含大量Fe2+、Al3+、Fe3+、Na+、Cl﹣、SO ![]() 离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是( )
离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是( )
A.Na+、Fe2+
B.Al3+、SO ![]()
C.Fe3+、SO ![]()
D.Al3+、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,发生下列几种反应:①16H++10Z一+2XO ![]() =2X2++5Z2+8H2O ②2A2++B2=2A3++2B一 ③2B一+Z2=B2+2Z根据上述反应,判断下列结论中错误的是( )
=2X2++5Z2+8H2O ②2A2++B2=2A3++2B一 ③2B一+Z2=B2+2Z根据上述反应,判断下列结论中错误的是( )
A.氧化性强弱的顺序为:XO ![]() >Z2>B2>A3+
>Z2>B2>A3+
B.Z2在①、③反应中为还原剂
C.溶液中可发生:Z2+2A2+=2A3++2Z一
D.X2十是XO ![]() 的氧化产物
的氧化产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1905年德国化学家哈伯发明了合成氨的方法,他因此获得了1918年度诺贝尔化学奖.氨的合成不仅解决了地球上因粮食不足而导致的饥饿与死亡问题,在国防、能源、轻工业方面也有广泛用途.
Ⅰ.以氨为原料,合成尿素的反应原理为:
2NH3(g)+CO2(g)═CO(NH2)2(l)+H2O(g)△H=a kJ/mol.
为研究平衡时CO2的转化率与反应物投料比( ![]() )及温度的关系,研究小组在10L恒容密闭容器中进行模拟反应,并绘出如图(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系).
)及温度的关系,研究小组在10L恒容密闭容器中进行模拟反应,并绘出如图(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系).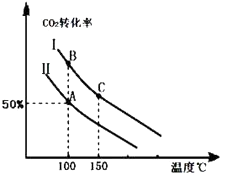
(1)a0 (填“>”或“<”),判断依据是 .
(2)①投料比:Ⅱ(填“>”或“<”).
②若n(CO2)起始=10mol,曲线Ⅱ的投料比为0.4,在100℃条件下发生反应,达平衡至A点,则A点与起始压强比为 .
③A点平衡常数与B点平衡常数间的关系:KAKB(填“>”或“<”或“=”).B点正反应速率与C点正反应速率间的关系为:v(B)v(C)(填“>”或“<”或“=”).
(3)若按曲线Ⅰ的投料比投料,在上述实验中压缩容器体积至5L,在图中画出反应达平衡时的二氧化碳的转化率与温度之间的关系曲线.
(4)为提高CO2转化率可以采取的措施是 .
a.使用催化剂 b.及时从体系中分离出部分CO(NH2)2c.将体系中的水蒸气液化分离
氨气可用于工业上生产硝酸,其尾气中的NO2可用氨水吸收生成硝酸铵,25℃时,将10molNH4NO3溶于水,溶液显酸性,向该溶液中滴加1L某浓度的氨水,溶液呈中性,则滴加氨水的过程中水的电离平衡将(填“正向”、“逆向”或“不”) 移动,此中性溶液中NH3H2O的物质的量为mol.(25℃时,NH3H2O的电离平衡常数Kb=2×10﹣5)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com