
| V |
| 22.4L/mol |
| m |
| n |
| 5.6L |
| 22.4L/mol |
| 6.5g |
| 0.25mol |
|
|


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、①③ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化碳中所含的氯化氢(NaOH溶液) |
| B、氢气中所含的硫化氢(硫酸铜溶液) |
| C、乙酸乙酯中所含的乙酸(乙醇) |
| D、氯化钠溶液中所含的氯化钡(硫酸) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Q1=Q2=92.4 |
| B、Q1=Q2<92.4 |
| C、Q1<Q2<92.4 |
| D、Q2<Q1<92.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
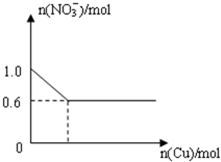 将28.8g铜投入100mL浓硝酸中,最后铜有剩余,其NO3-离子物质的量变化如图所示,请回答下列问题:
将28.8g铜投入100mL浓硝酸中,最后铜有剩余,其NO3-离子物质的量变化如图所示,请回答下列问题:| 2 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去混在氯化钠固体中的氯化铵或单质碘,均可用升华的方法 |
| B、若FeCl2溶液中含有I-杂质,可用过量的Cl2氧化后进行萃取分液 |
| C、CO2中含有HCl杂质:通入饱和NaHCO3溶液,洗气 |
| D、鉴别固体Na2CO3和NaHCO3,可以分别配成溶液,再加入澄清石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com