
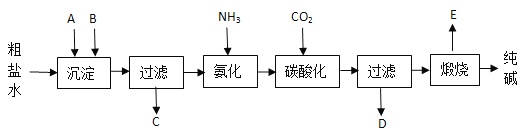
【题目】工业生产纯碱的工艺流程示意图如下:
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A_____________________ B_____________________。
(2)实验室提纯粗盐的实验操作依次为:_________
取样→________→ 沉淀 →________→______ → 冷却结晶 → _______ → 烘干 。
(3)工业生产纯碱的工艺流程中,先通氨气,再通二氧化碳的原因是________________。
(4)碳酸化时产生的现象是____________________________________,碳酸化后过滤,滤液D最主要的成分是____________(填写化学式)。
(5)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数(已知:样品质量为m1,加热后固体质量为m2),纯碱中碳酸氢钠的质量分数可表示为W(NaHCO3)=_______。
【答案】 Ca(OH)2或CaO Na2CO3 溶解, 过滤, 蒸发, 过滤 因为氨气在水中的溶解度非常大,在水中形成氨的水溶液,溶液的碱性比较强,易于吸收更多的二氧化碳,这样可以生成更多的HCO3,从而产生更多的纯碱 有晶体析出(或出现浑浊) NH4Cl 84(m1-m2)/31m1
【解析】(1)沉淀剂A来源于石灰窑厂,所以A是Ca(OH)2或CaO,A用来除去粗盐中的镁离子。而过量的钙离子,则需要碳酸钠来除去,故B为Na2CO3;(2)形成沉淀之前,应该先溶解。产生的沉淀通过过滤除去,所得溶液通过蒸发即得到氯化钠晶体。故实验室提纯粗盐的实验操作依次为:取样→溶解→ 沉淀 →过滤→蒸发→ 冷却结晶 →过滤→ 烘干;(3)因为氨气在水中的溶解度非常大,在水中形成氨的水溶液,溶液的碱性比较强,易于吸收更多的二氧化碳,这样可以生成更多的HCO3,从而产生更多的纯碱,故工业生产纯碱的工艺流程中,先通氨气,再通二氧化碳;(4)碳酸化时产生的现象是有晶体析出(或出现浑浊);根据操作过程,氨化后通入二氧化碳的溶液发生复分解反应,反应的化学方程式为:H2O+CO2+NH3+NaCl=NaHCO3+NH4Cl,最终得到NH4Cl还有碳酸氢钠等,碳酸氢钠溶解度很小而结晶,故酸化后滤液的主要成分是NH4Cl;(5)加热前纯碱的质量为m1,加热后的质量为m2,则加热损失的质量为:m1-m2,则纯碱中碳酸氢钠的质量为: ![]() ;故纯碱中含有的碳酸氢钠的质量分数为
;故纯碱中含有的碳酸氢钠的质量分数为![]() 。
。


科目:高中化学 来源: 题型:
【题目】一定质量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6g,若其中水的质量为10.8g,则CO的质量是( )
A.4.4g
B.1.4g
C.2.2g
D.在2.2g和4.4g之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如右图,则原混合溶液中MgCl2与FeCl3的物质的量之比为( ) 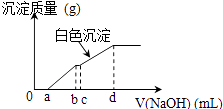
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备高纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)═Si(s)+4HCl(g)△H=+Q kJ/mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述中正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达平衡时,吸收热量为Q kJ
C.反应至4min时,若HCl浓度为0.12mol/L,则H2的反应速率为0.03mol/(Lmin)
D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL 1mol/L的NaOH溶液恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定石灰石样品中碳酸钙(合SiO2杂质)的含量。现利用如图所示装置进行实验,充分反应后,测定装置C中生成的BaCO3沉淀质量。下列说法正确的是

A. 装置A中药品应为浓硫酸
B. 在B~C之间应增添盛有饱和NaHCO3溶液的洗气装置,以除去氯化氢气体
C. 只要测定装置C在吸收CO2前后的质量差,也可以确定碳酸钙的质量分数
D. 为了测得C中生成的沉淀质量,需经过过滤、洗涤、干燥、称量等操作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室检验溶液中是否存在SO42-,可选用的化学试剂依次为
A. KCl(aq),HCl(aq) B. HNO3(aq),KNO3(aq)
C. HCl(aq),BaCl2(aq) D. NaNO3(aq),HNO3(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知C—C单键可以绕键轴旋转,其结构简式可表示为![]() 的烃,下列说法中正确的是( )
的烃,下列说法中正确的是( )
A. 分子中最多有4个碳原子处于同一直线上
B. 该烃的核磁共振氢谱图有四组峰
C. 分子中至少有10个碳原子处于同一平面上
D. 该烃是苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ksp(CaSO4)=9×10﹣6 , CaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( ) 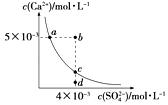
A.CaSO4在稀硫酸中的溶解性比在纯水中的溶解性强
B.a点对应的Ksp等于c点对应的Ksp
C.d点溶液通过蒸发可以变到c点
D.b点将有沉淀生成,平衡后溶液中c(SO42﹣)一定等于3×10﹣3mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com