
����Ŀ���������ó��ս��ì�ܼ�����Ҳ�����ǿ������й��뵼���ҵ���ڵ����㣬��˵�������Σ�Ϊʱδ�������ҳ����ڵIJ��㣬Ȼ����Ե�ȥ������⣬�����ð뵼���ҵ����չ׳�����������Ȼ�����(POCl3)��һ����Ҫ�Ļ���ԭ�ϣ��������뵼����Ӽ������άԭ�ϡ�һ�о�С����ʵ����ģ�ⷴӦ![]() �Ʊ�POCl3���ⶨ��Ʒ������
�Ʊ�POCl3���ⶨ��Ʒ������
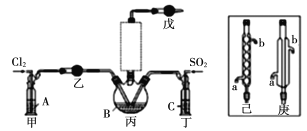
���Ͽ�Ƭ��
���� | �۵㣯�� | �е㣯�� | ��Է������� | ���� |
PCl3 | -93.6 | 76.1 | 137.5 | ��ˮ����ˮ�⣬����O2��Ӧ |
POCl3 | 1.25 | 105.8 | 153.5 | ��ˮ����ˮ�⣬������PCl3 |
SOCl2 | -105 | 78.8 | 119 | ��ˮ����ˮ�⣬�����ֽ� |
��1����ѡ��Na2SO3������70��ŨH2SO4��ȡSO2����Ӧ�Ļ�ѧ����ʽ�ǣ�____________��
��2����ҺAΪ����ʳ��ˮ����װ����Ӧ��ʢװ���Լ�Ϊ__________(����P2O5��������ʯ��������ŨH2SO4��������ˮ����ͭ��)����Ӧװ��ͼ�������δ�������������ѡ��______(����������������)��
��3���ס���װ�õ����ó�����������ľ��������⣬����________________��
��4��ˮԡ����������ƿ�����Ʒ�Ӧ�¶���60��65�棬��ԭ����___________��
��5��ͨ��������·��ɲⶨ�����ᴿ��IJ�Ʒ��POCl3�ĺ�����ȷ��ȡ1��600g��Ʒ��ˮ��ƿ��ҡ������ȫˮ�⣬��ˮ��Һ���100 mL��Һ��ȡ10��00 mL����ƿ�У�����0��2000 mol��L-1��AgNO3��Һ20��00 mL(Ag++C1- AgC1��)���ټ�������������������ʹ�������л��︲�ǡ�����NH4Fe(SO4)2��ָʾ������0��1000 mol��L-1KSCN����Һ�ζ�������AgNO3���յ�(Ag++SCN- AgSCN��)����ƽ��ʵ�飬ƽ������KSCN����Һ10��00 mL��
�ٴﵽ�ζ��յ��������____________��
��POCl3����������Ϊ___________��
����֪��KSP(AgC1)=3
���𰸡�Na2SO3+H2SO4 �TNa2SO4 +SO2��+H2O P2O5 �� ͨ���۲�������ݵ����ʿ���ͨ����������� �¶�̫�ͣ���Ӧ����̫�����¶�̫�ߣ�PCl3�����ʻӷ� �������һ��KSCN����Һ����Һ���ɫ���Ұ�����ڲ���ɫ 95.9�� ƫС
��������
��ʵ��װ��ͼ��ʵ��ԭ����֪��װ��A����ʢ�б���ʳ��ˮ����ȥ�����л��е��Ȼ��⣬װ������ʢ�����Թ����������������ף�����������װ�ö���ʢ��Ũ���ᣬ�����������װ�ñ�Ϊ���Ȼ������Ʊ�װ�ã�װ�������������ܵ������������������Ȼ����ף���ֹ���Ȼ��������Ȼӷ���ʢ�м�ʯ�ҵĸ���ܵ�����������δ��Ӧ�������Ͷ�������ֹ��Ⱦ������ͬʱ���տ�����ˮ��������ֹˮ��������������ƿ�е������Ȼ�����ˮ�⡣
��1��Na2SO3������70��ŨH2SO4��Ӧ���������ơ����������ˮ����Ӧ�Ļ�ѧ����ʽΪNa2SO3+H2SO4 �TNa2SO4 +SO2��+H2O���ʴ�Ϊ��Na2SO3+H2SO4 �TNa2SO4 +SO2��+H2O��
��2����ҺA�б���ʳ��ˮ�������dz�ȥ�����л��е��Ȼ��⣬װ������ʢ�����Թ����������������ף�������������ֹˮ��������������ƿ�е������Ȼ�����ˮ�⣻װ�������������ܵ������������������Ȼ��ף���ֹ���Ȼ��ס����Ȼ��������Ȼӷ����������Ȼ����IJ��ʣ�Ϊ��ǿ����Ч������ѡ��ֱ�������ܣ��ʴ�Ϊ��P2O5������
��3���ס���װ�õ����ó�����������ľ��������⣬�������۲�������ݵ����ʿ���ͨ����������٣������ڷ�Ӧ��ֽ��У��ʴ�Ϊ��ͨ���۲�������ݵ����ʿ���ͨ����������٣�
��4�������¶�̫�ͣ���Ӧ����̫�������¶�̫�ߣ�PCl3���������Ȼӷ����������Ȼ����IJ��ʣ�����ʵ��ʱ��ˮԡ����������ƿ�����Ʒ�Ӧ�¶���60��65�����ʴ�Ϊ���¶�̫�ͣ���Ӧ����̫�����¶�̫�ߣ�PCl3�����ʻӷ���
��5�����������֪���ⶨPOCl3��Ʒ����ʱ��NH4Fe(SO4)2��ҺΪָʾ������KSCN��Һ�ζ�������AgNO3��Һ���ﵽ�յ�ʱ�������ǵ������һ��KSCN����Һ����Һ���ɫ���Ұ�����ڲ���ɫ���ʴ�Ϊ���������һ��KSCN����Һ����Һ���ɫ���Ұ�����ڲ���ɫ��
��KSCN�����ʵ���Ϊ0.1mol/L��0.01L=0.001mol�����ݷ�ӦAg++SCN-=AgSCN������֪��Һ��ʣ��������ӵ����ʵ���Ϊ0.001mol������POCl3��ˮ��Ӧ�����Ȼ���������ӵ����ʵ���Ϊ��0.004mol ��0.001mol��=0.003mol��ˮ�����ɵ��Ȼ�������ʵ���Ϊ0.003mol���������֪1.600g��Ʒ��POCl3�����ʵ���Ϊ![]() ��10=0.01mol�����Բ�Ʒ��POCl3����������Ϊ
��10=0.01mol�����Բ�Ʒ��POCl3����������Ϊ![]() ��100%=95.9%���ʴ�Ϊ��95.9%��
��100%=95.9%���ʴ�Ϊ��95.9%��
��������������������ʹ���ɵ��Ȼ��������뿪��Һ�������������������ˮ��Һ�в����Ȼ�������ת����AgSCN����֪Ksp��AgCl��>Ksp��AgSCN����ʹ��ʵ�������ĵ�AgSCNƫ�࣬���ݣ�7���ļ���ԭ����֪����ʹ�ⶨ�����ƫ�ͣ��ʴ�Ϊ��ƫ�͡�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�������ճ��������й㷺Ӧ�á�
(1)д��Fe(OH)2ת��ΪFe(OH)3�Ļ�ѧ����ʽ��__________________��
(2)�̷�(FeSO4��7H2O)�Dz�Ѫ����ԭ�ϣ��ױ��ʡ������̷��Ƿ���ʵ��Լ���________�����ʵ������̷��Ƿ���ȫ���ʣ�________________��
(3)(I)�����̷��Ʊ���ԭ���۵Ĺ�ҵ�������£�
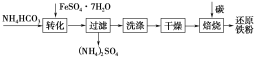
�����������Ҫ��Ϊ����ȥ����ˮ�ͽᾧˮ�������л�������FeCO3��nH2O�ڿ����б�����ΪFeOOH���÷�Ӧ�Ļ�ѧ����ʽΪ_____________________��
��ȡ������FeCO3��Ʒ12.49 g�����գ����յõ���ԭ����6.16 g��������Ʒ������FeOOH������Ϊ________g��(FeOOHҲ�ܱ�C��ԭ�õ�Fe)
(II)�����з������Ƶ�Fe(OH)2��ɫ�������ò���Fe3����FeSO4��Һ�벻��O2������ˮ���Ƶ�NaOH��Һ��Ӧ�Ʊ���
������������������������FeSO4��Һʱ�������________��
����ȥ����ˮ���ܽ��O2������________�ķ�����
�����ɰ�ɫ����Fe(OH)2�IJ������ó��ι���ȡ����O2��NaOH��Һ������FeSO4��ҺҺ���£��ټ���NaOH��Һ������������������_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧʵ��С���ͬѧΪ̽���ͱȽ�SO2����ˮ��Ư���ԣ��������ͼ��ʵ��װ�á�
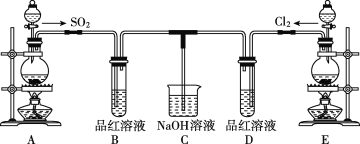
��1��ʵ������װ��E�Ʊ�Cl2���䷴Ӧ�Ļ�ѧ����ʽΪMnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O������6mol��HCl�μӷ�Ӧ����ת�Ƶĵ�������Ϊ____��
MnCl2+Cl2��+2H2O������6mol��HCl�μӷ�Ӧ����ת�Ƶĵ�������Ϊ____��
��2���ٷ�Ӧ��ʼһ��ʱ��۲쵽B��D�����Թ��е�Ʒ����Һ���ֵ������ǣ�B____��D____��
��ֹͣͨ�����ٸ�B��D�����Թֱܷ���ȣ������Թ��е�����ֱ�Ϊ��B____��D____��
��3����һ��ʵ��С���ͬѧ��ΪSO2����ˮ����Ư���ԣ�����Ϻ��Ư���Կ϶����ǿ�����ǽ��Ƶõ�SO2��Cl2��1��1ͬʱͨ�뵽Ʒ����Һ�У����������ɫЧ���������������������������������ԭ��(�û�ѧ����ʽ��ʾ)��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Z�Ǻϳ�ijҩ����м��壬��ϳ�ԭ������:
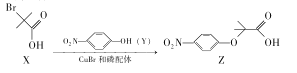
����˵����ȷ����.
A.��NaHCO3��Һ���Լ���X��ZB.X��Y��Z���ܷ���ȡ����Ӧ
C.X��������̼ԭ�ӿ��ܹ�ƽ��D.��X������ͬ�����ŵ�ͬ���칹�廹��5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ҵβ��SO2��NO2����Ⱦ�������γ������������ס���ش��������⣺������(��ѧʽ��HNCO��CΪ+4��)����������β���е�NO2���䷴Ӧԭ��Ϊ��HNCO+NO2��N2+CO2+![]() (δ��ƽ)��
(δ��ƽ)��
��������Ӧ����������____________��
����ƽ����Ӧ��д____________��
��ÿ����33.6LNO2(��״��)����Ӧ��ת�Ƶ��ӵ���ĿΪ____________��
����Ϊ�˼���CO�Դ�������Ⱦ��ij�о���ѧϰС�����о�����CO��H2O��Ӧת��Ϊ��ɫ��ԴH2����֪��2CO��g��+O2��g���T2CO2��g����H=��566.0kJ mol��1��2H2��g��+O2��g���T2H2O��g����H=��483.6kJ mol��1��2H2O��g���TH2O��l����H=��44.0kJ mol��1��
��1��д��CO��H2O��g����������CO2��H2���Ȼ�ѧ����ʽ��____________��
��2�������Ǻϳɰ�����Ҫԭ�ϣ��ϳɰ���Ӧ���Ȼ�ѧ����ʽ���£�N2��g��+3H2��g��![]() 2NH3��g����H=��92.4kJmoL��1��
2NH3��g����H=��92.4kJmoL��1��
�ٵ��ϳɰ���Ӧ�ﵽƽ��ı�ijһ������������ı�N2��H2��NH3����������Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��ͼ��t3ʱ����ƽ���ƶ�������������______�����б�ʾƽ��������NH3�ĺ�����ߵ�һ��ʱ����______��

���¶�ΪT��ʱ����1mol N2��2mol H2�����ݻ�Ϊ0.5L���ܱ������У���ַ�Ӧ����N2��ƽ��ת����Ϊ50%����Ӧ��T��ʱ��ƽ�ⳣ��Ϊ______mol��2L2��
��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2+3H2![]() 2NH3��ͼ��ʾ�������ı䣬ƽ����ϵ�а�����������ı仯���ƣ���������Ϊѹǿʱ���仯������ȷ���ǣ�����ţ���ͬ��___����������Ϊ�¶�ʱ���仯������ȷ����___��
2NH3��ͼ��ʾ�������ı䣬ƽ����ϵ�а�����������ı仯���ƣ���������Ϊѹǿʱ���仯������ȷ���ǣ�����ţ���ͬ��___����������Ϊ�¶�ʱ���仯������ȷ����___��

��3�������°�����HCl����������ˮ���ֽ���ͬ�������ͬ���ʵ���Ũ�ȵİ�ˮ�������ϣ�������Һ�и����ӵ����ʵ���Ũ�Ȱ����ɴ�С��˳����������Ϊ____��____��____��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڲ�ͬ�¶��£�ˮ��Һ��![]() ��
��![]() ����ͼ��ʾ��ϵ������˵����ȷ����
����ͼ��ʾ��ϵ������˵����ȷ����![]()
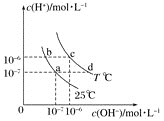
A.b����Һ�в����ܴ���![]()
B.b��c����pH��ͬ������Һ������Բ�ͬ
C.ͨ�����µķ�������ʹ��Һ��״̬��d���Ϊa��
D.a����Һ�п��ܴ�����������ӣ�![]() ��
��![]() ��
��![]() ��
��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳɰ���Ӧ�ڴ�������ķ�Ӧ���̼������仯��ͼ��ʾ������˵����ȷ����
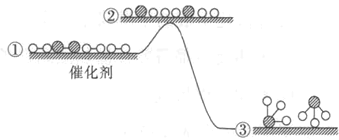
A.����ѹǿ��������֮���������ֵ������
B.�ϳɰ������淴Ӧ���ʱ���ͬ
C.�ϳɰ��Ĺ��������ȷ�Ӧ
D.��ʹ�ô��������ɵ�����NH3��Ҫ��ʱ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����Ĺ�ҵ�����η�ˮ�к��д�����Fe2+��Fe3+���϶��Cu2+��������Na+�������ƻ��Ӹ÷�ˮ�л������������ͽ���ͭ�������������ͼ��

�ش��������⣻
(1)A�Ļ�ѧʽΪ_________��D�Ļ�ѧʽΪ_______��
(2)�ڹ�ҵ��ˮ�м������Aʱ����Ӧ�����ӷ���ʽ�У�___________��__________��
(3)�õ�FeSO47H2O����IJ�����Ϊ������Ũ������ȴ�ᾧ��______��______�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й����ʵ����ļ�������ѧ��ѧ����Ҫ���֣���ش������й����ʵ����ļ������⡣
��1���ڱ�״���£�67.2 L CO2��__________mol������Ϊ_______g������__________��CO2���ӣ����к���__________mol��ԭ�ӡ�
��2���ڱ�״���£�1.7 g������ռ�����ԼΪ_________L������ͬ������_____mol H2S������ͬ����ԭ������
��3��ij��̬�����ﻯѧʽΪRO2���ڱ�״���£�1.28 g��������������448 mL�����������Ħ������Ϊ_______��R�����ԭ������Ϊ__________��
��4��ʵ���ҳ���Ũ�������������Ϊ98%���ܶ�Ϊ1.80 g��mL1�������ʵ���Ũ����_______��
��5����״���£���V L A���壨Ħ������ΪM g/mol����ȫ����0.1 Lˮ���ܶ�1 g/cm3���У�������Һ���ܶ�Ϊd g/mL�������Һ�����ʵ���Ũ��Ϊ_______mol/L��
A��![]() B��
B��![]() C��
C��![]() D��
D��![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com