
����Ŀ��ij��ѧ��ȤС��������ͼװ���Ʊ��������������۲�����ɫ���ṩ��ѧҩƷ�����ۡ�ϡ���ᡢ����������Һ��
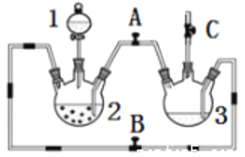
��1��ϡ����Ӧ����___________�У���д�������ƣ�.
��2����ʵ��ͨ������A��B��C�������أ��������еĿ����ž����ٹرտ���_________������______�Ϳɹ۲쵽��������������ɫ���Է���ʵ�鿪ʼʱ�ž�װ���п���������____________________________��
��3����ʵ��ʹ�����ۣ�����Ӧ���ʿ���̫���⣬�����ܻ���ɵIJ��������____________��
��4����FeSO4��Һ�м���(NH4)2SO4������Ʊ���������茶���[(NH4��2SO4�� FeSO46H2O] ��ʽ��Ϊ392�����þ����һ���������ȶ������ױ�������������ˮ���������Ҵ���
��Ϊϴ��(NH4��2SO4��FeSO4��6H2O�ֲ�Ʒ�����з���������ʵ���________________ ��
A������ˮϴ B��������ˮϴ��������ˮ�Ҵ�ϴ
C����30%���Ҵ���Һϴ D����90%���Ҵ���Һϴ
��Ϊ�˲ⶨ��Ʒ�Ĵ��ȣ���ȡa g��Ʒ����ˮ�����Ƴ�500mL��Һ����Ũ��Ϊc mol��L-1������KMnO4��Һ�ζ���ÿ����ȡ����Һ�����Ϊ25.00mL��ʵ������¼���£�
ʵ����� | ��һ�� | �ڶ��� | ������ |
���ĸ��������Һ���/mL | 25.52 | 25.02 | 24.98 |
�ζ������з�����Ӧ�����ӷ���ʽΪ_______________________________________.
���𰸡� ��Һ©�� B A����AC���� ��ֹ���ɵ����������������� ���۽��뵼�ܴӶ��������ܣ������������𰸣� D MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
��������������Ҫ�������ʵ�����Ʊ�����������ʵ������ۡ�
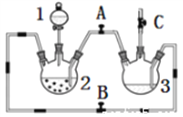
��1��ϡ����Ӧ���ڷ�Һ©���С�
��2����ʵ��ͨ������A��B��C�������أ��������еĿ����ž����ٹرտ���B������A��C�Ϳɹ۲쵽��������������ɫ��ʵ�鿪ʼʱ�ž�װ���п��������ɣ���ֹ���ɵ�������������������
��3����ʵ��ʹ�����ۣ�����Ӧ���ʿ���̫���⣬�����ܻ���ɵIJ�����������۽��뵼�ܴӶ��������ܣ������������𰸣���
��4������������茶��岻�����Ҵ�����ˣ�Ϊϴ��(NH4��2SO4��FeSO4��6H2O�ֲ�Ʒ�����з���������ʵ���D��
�ڵζ������з�����Ӧ�����ӷ���ʽΪMnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. Na2O2�����ĩ���뵽���͵�NaCl��Һ�в�������������
B. �Ʊ�NO2ʱ������ˮ��NaOH��Һ����β��
C. ������KMnO4��Һ����FeCl3��Һ��FeCl2��Һ
D. �����£�56g Fe��������Ũ���ᷴӦ��ת�Ƶ�����Ϊ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ǻ�ѧѧϰ�о����õ��ķ���,���ж�һЩ���ʻ�ѧ��Ӧ�ķ����Լ�������ȷ����( )
A. H2SO4���ᣬ��ΪH2SO4�к�����Ԫ��
B. �����ǽ��壬��Ϊ�����еķ�ɢ������ֱ����1nm��100nm֮��
C. Na��H2O�ķ�Ӧ�������ӷ�Ӧ����Ϊ��Ӧ��û�����Ӳμ�
D. Na��Cl2��ȼ�ղ���������ԭ��Ӧ����Ϊû�е�����ʧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ�����ʴ�������˵����ȷ����( )
A. �����������ڿ�������绯ѧ��ʴ�����䰵
B. �ں����������п�鱣����Dz��ܸ�ʴ�Dz�������������������������
C. ����������Ʒ�ĶƲ�����ʱ���Ʋ����ܶ�����Ʒ�𱣻�����
D. �ɽ��������ֹ������ֱ����Դ�����������Ա��������ܸ�ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A(C2H2)�ǻ����л�����ԭ�ϣ���A�Ʊ�����ϩ������ȩ��˳ʽ�������ϩ�ĺϳ�·��(���ַ�Ӧ������ȥ)��ͼ��ʾ��

�ش��������⣺
��1��A��������____________��B���еĹ�������____________��
��2���ٵķ�Ӧ������____________���ߵķ�Ӧ������____________��
��3��C��D�Ľṹ��ʽ�ֱ�Ϊ____________��____________��
��4�������ϩ�����������__________��ԭ�ӹ�ƽ�棬˳ʽ�������ϩ�Ľṹ��ʽΪ____________��
��5��д����A������ͬ�����ŵ������ϩ������ͬ���칹��(д�ṹ��ʽ)________________________________________________��
��6�����������ϩ�������ϳ�·�ߣ����һ����A����ȩΪ��ʼԭ���Ʊ�1��3-����ϩ�ĺϳ�·��____________________________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Cl2����ͨ��ˮ�������ͣ�Ȼ�������еμ�0.1mol/LNaOH��Һ������ʵ���������Һ��pH�仯������ͼ��ʾ�������Ǵ�����ֽ⣬����������ȷ����

A. ʵ���������pH��ֽ�ⶨ��Һ��pH
B. a��b�Σ���Һ�� C��H+��/C��OH-�� ��С
C. b���Ӧ��Һ�У�c��Cl������c��H+����c��HClO����c��ClO������c��OH����
D. c���Ӧ��Һ�У�c��Na+��=c��Cl-��+c��ClO-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ʊ��谱�����ƵĻ�ѧ����ʽΪCaCO3��2HCN===CaCN2��CO����H2����CO2�����ڷ�Ӧ��(����)
A. ��Ԫ�ر�������̼Ԫ�ر���ԭ B. HCN����������CaCO3�ǻ�ԭ��
C. CaCN2���������H2�ǻ�ԭ���� D. COΪ�������H2Ϊ��ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A��������ķ�Ӧһ�����Է���Ӧ B��������ķ�Ӧһ�����Է���Ӧ
C���ء��ʶ�Ϊ��ֵ�ķ�Ӧ���Է���Ӧ D����HT��S<0�ķ�Ӧһ�����Է���Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���屽��һ�ֻ���ԭ�ϣ�ʵ���Һϳ��屽��װ��ʾ��ͼ���й��������£�

�� | �� | �屽 | |
�ܶ�/(g��cm��3) | 0.88 | 3.10 | 1.50 |
�е�/�� | 80 | 59 | 156 |
ˮ���ܽ�� | �� | �� | �� |
�����кϳɲ���ش����⣺
(1)��a�м���15 mL��ˮ����������м����b��С�ļ���4.0 mLҺ̬�塣��a�е��뼸���壬�а�ɫ��������������Ϊ������ ���塣�����μ���Һ����ꡣװ��d�������� ��
(2)Һ�����������в�������ᴿ��
����a�м���10 mLˮ��Ȼ����˳�ȥδ��Ӧ����м��
����Һ������10 mLˮ��8 mL 10%��NaOH��Һ��10 mLˮϴ�ӡ�NaOH��Һϴ�ӵ������� ��
����ֳ��Ĵ��屽�м�����������ˮ�Ȼ��ƣ����á����ˡ������Ȼ��Ƶ�Ŀ���� ��
(3)�����Ϸ���������屽�л����е���Ҫ����Ϊ ��Ҫ��һ���ᴿ�����в����б������ (������ȷѡ��ǰ����ĸ)��
A���ؽᾧ B������ C������ D����ȡ
(4)�ڸ�ʵ���У�a���ݻ����ʺϵ��� (������ȷѡ��ǰ����ĸ)��
A��25 mL B��50 mL C��250 mL D��500 mL
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com