
【题目】化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷(P4)和六氧化四磷(P4O6)的分子结构如图所示。现提供以下化学键的键能(单位:kJ/mol):P—P:198;P—O:360;O=O:498。则1 mol P4(白磷)燃烧P4( 白磷)+3O2(g)![]() P4O6(g)时的能量变化为( )
P4O6(g)时的能量变化为( )
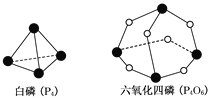
A.吸热1638 kJB.放热1638 kJC.吸热126 kJD.放热126 kJ
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】
铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe3+基态核外电子排布式为____________________。
(2)丙酮(![]() )分子中碳原子轨道的杂化类型是_______________,1 mol 丙酮分子中含有σ键的数目为______________。
)分子中碳原子轨道的杂化类型是_______________,1 mol 丙酮分子中含有σ键的数目为______________。
(3)C、H、O 三种元素的电负性由小到大的顺序为________________。
(4)乙醇的沸点高于丙酮,这是因为____________________。
(5)某FexNy的晶胞如题21图-1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如题21图-2 所示,其中更稳定的Cu替代型产物的化学式为___________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着电子科技水平的进步,液晶电视、电脑、仪表等电子产品已进入我们的日常生活。下面是工业上用丙烯(A)和有机物 C(C7H6O3)为原料合成液晶显示器材料(F)的主要流程:
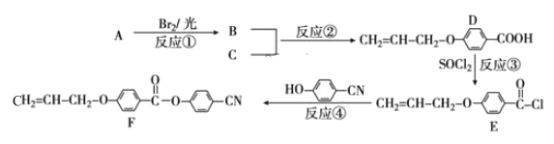
(1)化合物C的名称为_____;反应④的反应类型是 _____。
(2)D 中含氧官能团的名称为____;B的结构简式为 ______。
(3)写出C与足量 NaOH 水溶液反应的离子方程式______。
(4)写出所有符合下列条件下的化合物C的同分异构体的结构简式 ____。
①苯环上一溴代物只有 2 种 ②能发生银镜反应 ③苯环上有3个取代基
(5)化合物D是用于合成一种质子交换膜材料的重要原料。我国科研人员研发的一种质子交换膜材料的结构片段如下,它由三种单体缩聚而成。
已知:R1OH + R2Cl → R1—O—R2+ HCl,
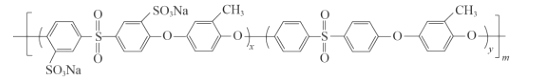
其单体的结构简式是: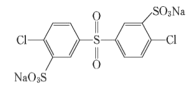 、________、________。
、________、________。
(6)请参照上述制备流程,写出以有机物C、乙烯、![]() 为原料制备
为原料制备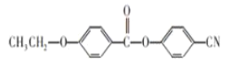 的合成路线流程图(无机试剂任用)__
的合成路线流程图(无机试剂任用)__
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式,并分别用双线桥法和单线桥法表示电子转移的方向和数目。
(1)用氢气还原氧化铜。__、__。
(2)加热氯酸钾分解制取氧气。__、__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲烷燃烧生成二氧化碳和液态水放出的热量为55.625 kJ·g-1。下列热化学方程式中不正确的是( )
A.CH4(g)+2O2(g)CO2(g)+2H2O(l) ΔH =-890 kJ/mol
B.![]() CH4(g)+O2(g)
CH4(g)+O2(g)![]() CO2(g)+H2O(l) ΔH=-445 kJ/mol
CO2(g)+H2O(l) ΔH=-445 kJ/mol
C.![]() CO2(g)+H2O(l)
CO2(g)+H2O(l)![]() CH4(g)+O2(g) ΔH=+445 kJ/mol
CH4(g)+O2(g) ΔH=+445 kJ/mol
D.CH4(g)+2O2(g)CO2(g)+2H2O(l) ΔH=-55.625 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+离子由H、C、N三种元素组成,结构如图所示。回答下列问题:
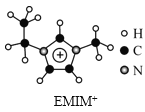
(1)碳原子价层电子的轨道表达式为__,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为__形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是__。NH3比PH3的沸点高,原因是__。
(3)氮元素的第一电离能比同周期相邻元素都大的原因是__。
(4)EMIM+离子中,碳原子的杂化轨道类型为__。分子中的大π键可用符号Π![]() 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为Π![]() ),则EMIM+离子中的大π键应表示为__。
),则EMIM+离子中的大π键应表示为__。
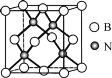
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于__晶体,其中硼原子的配位数为__。已知:立方氮化硼密度为dg/cm3,B原子半径为xpm,N原子半径为ypm,阿伏加德罗常数的值为NA,则该晶胞中原子的空间利用率为__(列出化简后的计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器的接触室(见右图)。下列说法错误的是
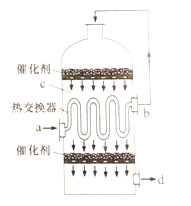
A. a、b两处的混合气体成分含量相同,温度不同
B. c、d两处的混合气体成分含量相同,温度不同
C. 热交换器的作用是预热待反应的气体,冷却反应后的气体
D. c处气体经热交换后再次催化氧化的目的是提高SO2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1 L含有0.4 mol Cu(NO3)2和0.4 mol KCl的水溶液,用惰性电极电解一段时间后,在一电极上析出19.2 g Cu。此时,在另一电极上放出气体的体积在标准状况下为(不考虑产生的气体在水中的溶解)( )
A.6.72 LB.13.44 LC.3.36 LD.5.6 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】均由两种短周期元素组成的A、B、C、D化合物分子,都含有18个电子,它们分子中所含原予的数目依次为2、3、4、6。A和C分子中的原子个数比为1∶1,B和D分子中的原子个数比为1∶2。D可作为火箭推进剂的燃料。请回答下列问题:
(1) A、B、C、D分子中相对原子质量较大的四种元素第一电离能由大到小排列的顺序为_________(用元素符号表示)。
(2) A与HF相比,其熔、沸点较低,原因是___________。
(3) B分子属于________(填“极性”或“非极性”)分子。
(4) D分子中心原子的杂化方式是________,由该原子组成的单质分子中包含________个π键,与该单质分子互为等电子体的常见分子的分子式为________。
(5) [Fe(H2O)6]2+与NO反应生成的[Fe(NO)(H2O)5]2+中,NO以N原子与Fe2+形成配位键。请画出[Fe(NO)(H2O)5]2+结构示意图:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com