
【题目】随着电子科技水平的进步,液晶电视、电脑、仪表等电子产品已进入我们的日常生活。下面是工业上用丙烯(A)和有机物 C(C7H6O3)为原料合成液晶显示器材料(F)的主要流程:
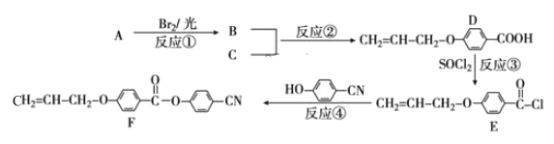
(1)化合物C的名称为_____;反应④的反应类型是 _____。
(2)D 中含氧官能团的名称为____;B的结构简式为 ______。
(3)写出C与足量 NaOH 水溶液反应的离子方程式______。
(4)写出所有符合下列条件下的化合物C的同分异构体的结构简式 ____。
①苯环上一溴代物只有 2 种 ②能发生银镜反应 ③苯环上有3个取代基
(5)化合物D是用于合成一种质子交换膜材料的重要原料。我国科研人员研发的一种质子交换膜材料的结构片段如下,它由三种单体缩聚而成。
已知:R1OH + R2Cl → R1—O—R2+ HCl,
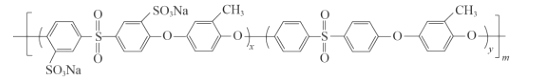
其单体的结构简式是: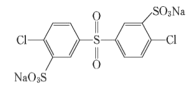 、________、________。
、________、________。
(6)请参照上述制备流程,写出以有机物C、乙烯、![]() 为原料制备
为原料制备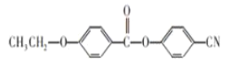 的合成路线流程图(无机试剂任用)__
的合成路线流程图(无机试剂任用)__
【答案】对羟基苯甲酸(或 4-羟基苯甲酸) 取代反应 醚键、羧基 CH2=CH-CH2Br 
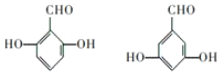

 CH2=CH2
CH2=CH2![]() CH3CH2Br
CH3CH2Br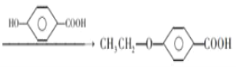


【解析】
丙烯(A)与溴在光照条件下,甲基上发生取代生成B,有机物C(C7H6O3)结合D的结构![]() ,可推知C为
,可推知C为![]() ,故丙烯与溴在光照条件下生成B为CH2=CHCH2Br,D中羧基与SOCl2发生取代反应生成E
,故丙烯与溴在光照条件下生成B为CH2=CHCH2Br,D中羧基与SOCl2发生取代反应生成E![]() ,E与
,E与![]() 发生取代生成F
发生取代生成F![]() 。
。
(1)化合物C![]() 的名称为对羟基苯甲酸(或 4-羟基苯甲酸);E与
的名称为对羟基苯甲酸(或 4-羟基苯甲酸);E与![]() 发生取代生成F,反应④的反应类型是取代反应。故答案为:对羟基苯甲酸(或 4-羟基苯甲酸);取代反应;
发生取代生成F,反应④的反应类型是取代反应。故答案为:对羟基苯甲酸(或 4-羟基苯甲酸);取代反应;
(2)D( ![]() )分子中含氧官能团的名称为醚键、羧基;由丙烯与溴在光照条件下生成B,B的结构简式为CH2=CH-CH2Br。故答案为:醚键、羧基;CH2=CH-CH2Br;
)分子中含氧官能团的名称为醚键、羧基;由丙烯与溴在光照条件下生成B,B的结构简式为CH2=CH-CH2Br。故答案为:醚键、羧基;CH2=CH-CH2Br;
(3)![]() 中酚羟基、羧基均能与NaOH反应,C与足量 NaOH 水溶液反应的离子方程式
中酚羟基、羧基均能与NaOH反应,C与足量 NaOH 水溶液反应的离子方程式 。故答案为:
。故答案为: ;
;
(4)所有符合下列条件下的化合物C的同分异构体①苯环上一溴代物只有2种,说明苯环上有2种氢,②能发生银镜反应,说明含有醛基,③苯环上有3个取代基,取代基为-CHO、2个-OH且存在对称结构,符合条件的同分异构体结构简式为: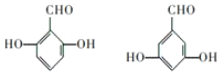 ;故答案为:
;故答案为: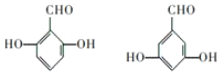 ;
;
(5)质子交换膜材料的结构片段 由三种单体缩聚而成,由信息R1OH + R2Cl → R1—O—R2+ HCl,脱去HCl形成化学键的部位如图,
由三种单体缩聚而成,由信息R1OH + R2Cl → R1—O—R2+ HCl,脱去HCl形成化学键的部位如图, 将失去的H和Cl补上,其单体的结构简式是:
将失去的H和Cl补上,其单体的结构简式是: 、
、 、
、 。故答案为:
。故答案为: ;
; ;
;
(6)乙烯与HBr发生加成反应生成CH3CH2Br,再类比路线图中合成F的流程可得目标物,以有机物C、乙烯、![]() 为原料制备
为原料制备![]() 的合成路线流程图(无机试剂任用):CH2=CH2
的合成路线流程图(无机试剂任用):CH2=CH2![]() CH3CH2Br
CH3CH2Br
![]()
![]() ;故答案为:CH2=CH2
;故答案为:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]()
![]()
![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】氯化亚铜是有机合成工业中应用较广的催化剂。
(1)CuCl用作制备碳酸二甲酯的催化剂:4CH3OH+2CO+O2![]() 2(CH3O)2CO+2H2O,请填写化学方程式将催化原理补充完整:i.4CuCl+4CH3OH+O2=4Cu(CH3O)Cl+2H2O;ii.________________________。
2(CH3O)2CO+2H2O,请填写化学方程式将催化原理补充完整:i.4CuCl+4CH3OH+O2=4Cu(CH3O)Cl+2H2O;ii.________________________。
(2)一种用废铜制备氯化亚铜的过程如下:
Cu(s)+Cl2(g)=CuCl2(s) △H=-a kJ·mol-1
CuCl2(s) +Cu(s) +4HCl(aq)=2H2[CuCl3] (aq) △H=+b kJ·mol-1
CuCl(s) + 2HCl(aq)H2[CuCl3] (aq) △H=-c kJ·mol-1
①反应 2Cu(s)+Cl2(g)=2CuCl(s) △H=_______________ kJ·mol-1(用含 a、b、c 的式子表示)
②向CuCl2 溶液中加入过量铜粉,发生反应生成CuC1。但在实验过程中要加入浓盐酸反应才能持续进行,反应结束后将溶液倒入蒸馏水中稀释获得CuCl。加入浓盐酸的目的是___________________。
(3)在电解槽中电解氨性含铜蚀刻废液,电解后向阴极液中加入盐酸酸化,再倒入蒸馏水稀释,得到氯化亚铜沉淀。
①电解装置如图所示,阴极区电极方程式为___________________________ 。
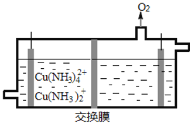
②稀释过程中溶液的温度不同,得到沉淀质量和氯化亚铜百分含量变化如图所示。
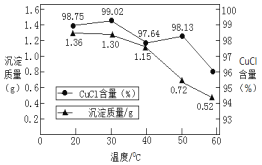
从氯化亚铜产率角度分析,最佳稀释温度为__________________;温度越高得到氯化亚铜沉淀质量越小,其原因可能是:i.加热过程中部分氯化亚铜被氧化;ii.___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年2月,国家卫生健康委办公厅、国家中医药管理局办公室联合发出《关于印发新型冠状病毒肺炎诊疗方案(试行第六版)的通知》。此次诊疗方案抗病毒治疗中增加了磷酸氯喹和阿比多尔两个药物。其中阿比多尔中间体I的合成路线如下:
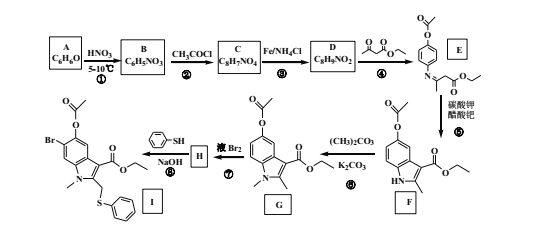
(1)A的结构简式是 _____。描述检验 A的方法及现象______________。
(2)I中含氧官能团名称是_____。
(3)③、⑦的反应类型分别是 ____ 、 __________ 。
(4)②的化学方程式为 ____。
(5)D的同分异构体中,满足下列条件的有_______种
a. 含有苯环 b.含有—NO2
其中核磁共振氢谱为3组峰,且峰面积之比为1∶2∶6的为__________________(任写一种结构简式)。
(6)已知:①当苯环有RCOO-、烃基时,新导入的基团进入原有基团的邻位或对位;原有基团为—COOH时,新导入的基团进入原有基团的邻位。②苯酚、苯胺(![]() )易氧化。设计以
)易氧化。设计以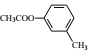 为原料制备
为原料制备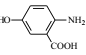 的合成路线 __________(无机试剂任用)。
的合成路线 __________(无机试剂任用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在 20 mL 0.1 molL-1 一元弱酸HA溶液中滴加0. 1mol L-1 NaOH溶液,溶液中1g[c(A-)/c(HA)]与 pH 关系如图所示。下列说法正确的是
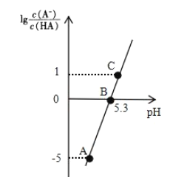
A.A点对应溶液中:c(OH-)>c(H+)
B.25℃时,HA电离常数的数量级为10-5
C.B点对应的 NaOH 溶液体积小于 10 mL
D.对C点溶液加热(不考虑挥发),则![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温条件下,可逆反应:2NO(g)+O2(g)![]() 2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
①单位时间内生成n mol O2的同时生成2n mol NO2②单位时间内生成n mol O2的同时生成2n mol NO③用NO2、NO、O2表示的反应速率的比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的压强不再改变的状态⑦混合气体的平均相对分子质量不再改变的状态.
A. ①④⑥⑦ B. ②③⑤⑦ C. ①③④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
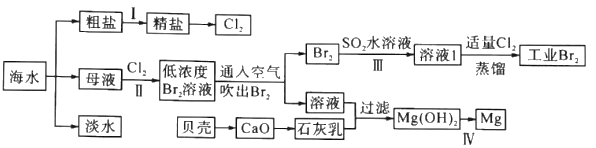
请回答下列问题:
(1)步骤I中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是______(填字母)。
A.①②③④ B.②③④① C.②④③① D.③④②①
请写出加入Na2CO3溶液后相关化学反应的离子方程式:_________、_________。
(2)步骤Ⅱ中已获得Br2,步骤Ⅲ中又将Br2还原为Br-,其目的是_________。步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_________。
(3)为了从工业Br2中提纯溴,除去产物中残留的少量Cl2.可向其中加入_________溶液。
(4)步骤Ⅳ由Mg(OH)2得到单质Mg,以下方法最合适的是_________(填序号)。
A. ![]()
B.![]()
C.![]()
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以葡萄糖为原料制得的山梨醇(A)和异山梨醇(B)都是重要的生物质转化平台化合物。E是一种治疗心绞痛的药物,由葡萄糖为原料合成E的过程如下:

回答下列问题:
(1)葡萄糖的分子式为__________。
(2)A中含有的官能团的名称为__________。
(3)由B到C的反应类型为__________。
(4)C的结构简式为__________。
(5)由D到E的反应方程式为______________。
(6)F是B的同分异构体,7.30 g的F与足量饱和碳酸氢钠反应可释放出2.24 L二氧化碳(标准状况),F的可能结构共有________种(不考虑立体异构),其中核磁共振氢谱为三组峰,峰面积比为3∶1∶1的结构简式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷(P4)和六氧化四磷(P4O6)的分子结构如图所示。现提供以下化学键的键能(单位:kJ/mol):P—P:198;P—O:360;O=O:498。则1 mol P4(白磷)燃烧P4( 白磷)+3O2(g)![]() P4O6(g)时的能量变化为( )
P4O6(g)时的能量变化为( )
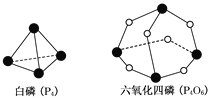
A.吸热1638 kJB.放热1638 kJC.吸热126 kJD.放热126 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一处于平衡状态的可逆反应:X(s)+3Y(g)![]() 2Z(g) ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是
2Z(g) ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z
A.①③⑤B.②③⑤C.②③⑥D.②④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com