
����Ŀ��̼�ǵ���������������������Ԫ��֮һ������Ҫ��ش���������:
��1��̼ԭ�ӵļ۵����Ų�ͼ:_________��������_________�ֲ�ͬ�˶�״̬�ĵ��ӡ�
��2��̼�����γɶ����л��������ͼ��ʾ��һ�����ʺ�һ����वĽṹ�����ַ���������ԭ�Ӷ���һ��ƽ���ϡ�
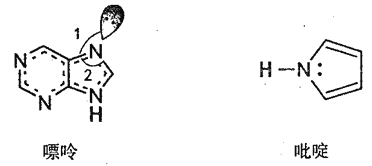
������������Ԫ�صĵ縺���ɴ�С��˳��__________��
�������й��֮��ļнǡ�1�ȡ�2����ԭ��_____________��
����ऽṹ��N ԭ�ӵ��ӻ���ʽ___________��
�ܷ����еĴ����������÷���![]() ��ʾ������m���������γɴ�������ԭ������n���������γɴ������ĵ�����(�籽�����еĴ������ɱ�ʾΪ
��ʾ������m���������γɴ�������ԭ������n���������γɴ������ĵ�����(�籽�����еĴ������ɱ�ʾΪ![]() )�������ʺ�����ж����д�����,���ʸ�����еĴ�������ʾΪ__________��
)�������ʺ�����ж����д�����,���ʸ�����еĴ�������ʾΪ__________��
��3��̼���γ�CO��CO2��H2CO3�ȶ����������
���ڷ�ӦCO ת����CO2 �Ĺ����У�����˵����ȷ����______��
A.ÿ�������й¶Ե��������� B.���Ӽ��Ա仯
C.ԭ�Ӽ�ɼ���ʽ�ı� D.���ӵ��۷е���
���ɱ��ͱ������ֳ����ķ��Ӿ��壬�����еĿռ�������: �ɱ�___����(����>���� ��<������=��)
��H2CO3��H3PO4 ����1�����ǻ�����H3PO4Ϊ��ǿ�ᣬH2CO3Ϊ�����ԭ��______��
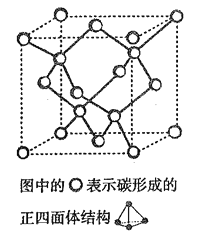
��4����2017 �꣬�����ѧ���Ŷӹ�ͬ�ϳ���̼��һ������ͬ��������: T- ̼��T- ̼�Ľṹ��: ���������ʯ�е�ÿ��̼ԭ����һ����4 ��̼ԭ����ɵ���������ṹ��Ԫȡ�����γ�̼��һ��������ά��������ṹ������ͼ����֪T- ̼��������Ϊa pm������٤������ΪNA����T- ̼���ܶȵı���ʽΪ______g/cm3��
���𰸡� ![]() 6 N > C > H ����N C H�� �µ��Ӷ�����ϵ��Ӷ�֮��ij������ڼ��ϵ��Ӷ�֮��ij������������Ǵ� sp3
6 N > C > H ����N C H�� �µ��Ӷ�����ϵ��Ӷ�֮��ij������ڼ��ϵ��Ӷ�֮��ij������������Ǵ� sp3 ![]() BCD > ��������ˮ�Ķ�����̼����ֻ��Լ���ٷ�֮һ��ˮ��ϳ�̼�ᣬ�밴������̼ȫ��ת��Ϊ̼��������������ǿ����ȣ���Ȼ��С�˽��ٱ���
BCD > ��������ˮ�Ķ�����̼����ֻ��Լ���ٷ�֮һ��ˮ��ϳ�̼�ᣬ�밴������̼ȫ��ת��Ϊ̼��������������ǿ����ȣ���Ȼ��С�˽��ٱ��� ![]()
��������(1)̼Ϊ6��Ԫ�أ�̼ԭ�ӵļ۵����Ų�ͼΪ![]() ��������6�ֲ�ͬ�˶�״̬�ĵ��ӣ��ʴ�Ϊ��
��������6�ֲ�ͬ�˶�״̬�ĵ��ӣ��ʴ�Ϊ��![]() ��6��
��6��
(2)��Ԫ�صķǽ�����Խǿ���縺����ֵԽ������������Ԫ�صĵ縺���ɴ�С��˳��ΪN > C > H���ʴ�Ϊ��N > C > H��
�ڹµ��Ӷ�����ϵ��Ӷ�֮��ij������ڼ��ϵ��Ӷ�֮��ij���������Խ����Խ����������й��֮��ļнǡ�1�ȡ�2�ʴ�Ϊ���µ��Ӷ�����ϵ��Ӷ�֮��ij������ڼ��ϵ��Ӷ�֮��ij������������Ǵ�
����ऽṹ��Nԭ��������3��ԭ�ӣ�����1���¶Ե��ӣ�����sp3�ӻ����ʴ�Ϊ��sp3��
�ܷ����еĴ����������÷���![]() ��ʾ������m���������γɴ�������ԭ������n���������γɴ������ĵ�������������वĽṹ�����еĴ�������5��ԭ��6�������γɵģ���ʾΪ
��ʾ������m���������γɴ�������ԭ������n���������γɴ������ĵ�������������वĽṹ�����еĴ�������5��ԭ��6�������γɵģ���ʾΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(3)��A. CO������̼�����ϸ���1���¶Ե��ӣ�CO2������̼�����ϸ���2���¶Ե��ӣ���A����B.COΪ���Է��ӣ�������̼Ϊ�Ǽ��Է��ӣ���B��ȷ��C.CO�д���̼��������CO2�д���̼��˫�������Ӽ�ɼ���ʽ�ı䣬��C��ȷ��D.��Ӧ���е�һ����̼����������Է�������С�������������̼�����ӵ��۷е���D��ȷ����ѡBCD��
��ˮ���Ӽ���������������з����ԣ�����ˮ�����γɱ�ʱ���ڽϴ�Ŀ�϶���ɱ�����֮��ֻ���ڷ��»������γɵķ��Ӿ������ܶѻ��������еĿռ������ʣ��ɱ��������ʴ�Ϊ������
����������ˮ�Ķ�����̼����ֻ��Լ���ٷ�֮һ��ˮ��ϳ�̼�ᣬ�밴������̼ȫ��ת��Ϊ̼��������������ǿ����ȣ���Ȼ��С�˽��ٱ��ˣ�������ˮ���������������ܹ���ȫ��Ӧ�������ᣬ�ʴ�Ϊ����������ˮ�Ķ�����̼����ֻ��Լ���ٷ�֮һ��ˮ��ϳ�̼�ᣬ�밴������̼ȫ��ת��Ϊ̼��������������ǿ����ȣ���Ȼ��С�˽��ٱ��ˣ�
(4)���ݾ����ṹͼ�������к��е���������ṹ����Ŀ=8��![]() +6��
+6��![]() +4=8��ÿ����������ṹ����4��̼ԭ�ӣ�����������=
+4=8��ÿ����������ṹ����4��̼ԭ�ӣ�����������=![]() ����������Ϊapm�������ܶ�=
����������Ϊapm�������ܶ�= =
=![]() g/cm3���ʴ�Ϊ��
g/cm3���ʴ�Ϊ��![]() ��
��


 ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д�
ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д� â���̸����������������ϵ�д�
â���̸����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ɳ����˶�Ա�ڽ����̽�ʱ�����������˶�Ա��֫���ⷢ���鴤�������������Ŵ����ź��������ų��˹�����
A. ˮ B. ���� C. ���� D. ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӽṹ�������ʵĹ۵���ƶ�  ���������ʣ�
���������ʣ�
��1���������ֿɷ�����Ӧ����Ӧ��
��2����CH�TCH2���ֿɷ�����Ӧ����Ӧ��
��3�����л��������ˮ�����ɲ���Ľṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ú��������Ҫ����Դ��Ҳ�ǻ�ѧ��ҵ����Ҫԭ�ϡ���ͼΪ��úΪԭ�Ϻϳ�TNT�߾���F��·�ߡ�
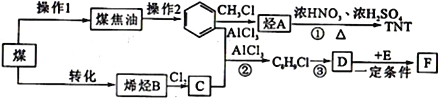
��ش��������⣺
��1������˵����ȷ����_______��
A.����1��ú�ĸ���
B.ú�������ǻ�ѧ�仯��ú��Һ���������仯
C.ú�к��б��Ͷ��ױ�������ú����ɵõ����Ͷ��ױ�
��2����![]() ������A�ķ�Ӧ������_______________��TNT�ĺ˴Ź���������________��塣
������A�ķ�Ӧ������_______________��TNT�ĺ˴Ź���������________��塣
��3��C�Ľṹ��ʽ��________________��
��4�����б������л������ʽΪC8H9Cl����������3��ȡ������ͬ���칹�����ĿΪ________�֡�
��5��E��1,3-����ϩ��F�Ǹ߷��ӻ����D��E��Ӧ�ķ���ʽ��_____________________________��
��6����д���������![]() Ϊԭ���Ʊ�������Ʒ
Ϊԭ���Ʊ�������Ʒ![]() �ĺϳ�·��_____________________________________________��
�ĺϳ�·��_____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ϵ�ؿɾ�����ˮ��ͬʱ���ܻ����Դ���м�ֵ�Ļ�ѧ��Ʒ��ͼ1Ϊ�乤��ԭ����ͼ2Ϊ��ˮ��Cr2O72-����Ũ����ȥ���ʵĹ�ϵ������˵����ȷ����
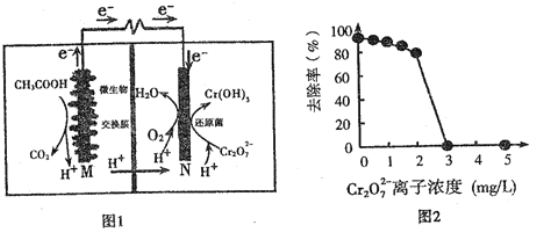
A. MΪ���������CH3COOH����ԭ
B. ���·ת��4mol����ʱ��M ������22.4LCO2
C. ��Ӧһ��ʱ���N����������ҺpH�½�
D. Cr2O72-����Ũ�Ƚϴ�ʱ�����ܻ���ɻ�ԭ��ʧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ������ȡSO2����֤SO2��ijЩ���ʵ�װ�ã���ش�

��1�������з�����Ӧ�Ļ�ѧ����ʽΪ______________________________________��
��2�����е�ʵ������Ϊʯ����Һ____________����ʵ��֤��SO2����____________�����ʡ�
��3�����е�Ʒ����Һ________��֤��SO2��________�ԡ�
��4�����е�ʵ��������________________________��֤��SO2��____________�ԡ�
��5�����е�ʵ��������______��֤��SO2��______�ԡ�
��6������������____________����Ӧ�Ļ�ѧ����ʽΪ____________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵������ȷ����
A. ��⾫��ͭʱ����ת����NA�����ӣ�������������С32g
B. 14g���ڿ��Ų����14Cԭ���к�������Ϊ8NA
C. ����������Ӧ����1molNa2O2ʱ��ת�Ƶ�����ĿΪ2NA
D. 28g��ϩ�к��еĹ��ۼ���ĿΪ6NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������100�������Ṳ����116���Ȼ���106����������Щ���������ϳ�6��������ʱ��������NH2������(����)
A. 6 B. 12 C. 22 D. 100
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������в�����̼̼������̼̼˫������Ľṹ��������Ϊ֤�ݵ���ʵ��( )
�ٱ�����ɫ�ӷ���Һ�壻
�ڱ�����ʹ���Ը��������Һ��ɫ��
��![]() ��
�� ��ͬһ�����ʡ�
��ͬһ�����ʡ�
A. �٢ڢ� B. �ٺ͢� C. �ٺ͢� D. �ں͢�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com