
【题目】下列化学方程式中,正确的是
A.甲烷的燃烧热△H =-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H =-890.3 kJ·mol-1
B.一定条件下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3放热akJ,其热化学方程式为:N2(g)+3H2(g) ![]() 2NH3(g) △H =-2a kJ·mol-1
2NH3(g) △H =-2a kJ·mol-1
C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,则水分解的热化学方程式表示为:2H2O(l) =2H2(g)+O2(g) △H =-571.6 kJ·mol-1
D.HCl和NaOH反应中和热△H =-57.3 kJ·mol-1,则CH3COOH和NaOH反应生成1mol水时放出的热量小于57.3KJ
【答案】D
【解析】
A.燃烧热中生成液态水;
B.合成氨为可逆反应,热化学方程式中为完全转化时的能量变化,且为放热反应;
C.2gH2完全燃烧生成液态水,放出285.8kJ热量,即1molH2完全燃烧生成液态水,放出285.8kJ热量,物质的量与热量成正比,且互为逆反应时焓变的符号相反、数值相同;
D.稀的强酸与强碱生成1mol时放热为57.3KJ,而醋酸电离吸热。
A. 甲烷的燃烧热△H=890.3kJmol1,则甲烷燃烧的热化学方程式可表示为![]() ,故A错误;
,故A错误;
B. 合成氨为可逆反应,热化学方程式中为完全转化时的能量变化,且为放热反应,则一定条件下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3放热akJ,可知1molN2完全反应放热大于2akJ,其热化学方程式为:![]() ,故B错误;
,故B错误;
C.2gH2完全燃烧生成液态水,放出285.8kJ热量,即1molH2完全燃烧生成液态水,放出285.8kJ热量,物质的量与热量成正比,且互为逆反应时焓变的符号相反、数值相同,则水分解的热化学方程式表示为:![]() ,故C错误;
,故C错误;
D. 稀的强酸与强碱生成1mol时放热为57.3KJ,而醋酸电离吸热,则CH3COOH和NaOH反应生成1mol水时放出的热量小于57.3KJ,故D正确;
故答案选:D。


 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案科目:高中化学 来源: 题型:
【题目】X、Y两种有机物的分子式不同,但均含有C、H或C、H、O,将X、Y以任意比例混合,只要物质的量之和不变,完全燃烧时所消耗的氧气量和生成水的物质的量也分别不变。则下列有关判断正确的是 ( )
A. X、Y分子式中氢原子数一定要相同,碳原子数必定相同
B. 若X为CH4,则相对分子质量最小的Y是甲醇
C. 若X为CH4,则相对分子质量最小的Y是乙二醇
D. X、Y的化学式应含有相同的氢原子数,且相差n个碳原子,同时相差2n个氧原子(n为正整数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学通过下列实验探究了物质的溶解度大小、反应物浓度与沉淀转化方向之间的关系。
已知:
物质 | BaSO4 | BaCO3 | AgI | AgCl |
溶解度/g(20℃) |
|
|
|
|
(1)探究BaCO3和BaSO4之间的转化
实验操作:
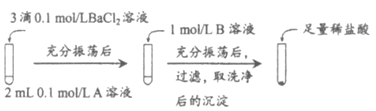
试剂A | 试剂B | 加入盐酸后的现象 | |
实验Ⅰ | Na2CO3 | Na2SO4 | 无明显现象 |
实验Ⅱ | Na2SO4 | Na2CO3 | 有少量气泡产生,沉淀部分溶解 |
①实验Ⅰ中加入A溶液后生成沉淀的离子方程式为_____________。
②实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因________。
(2)探究AgCl和AgI之间的转化
实验Ⅲ:
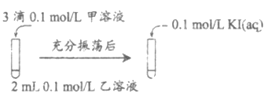
实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。
| p>装置 | 步骤 | 电压表读数 |
| i. 如图连接装置并加入试剂,闭合K | a |
ii. 向B中滴入AgNO3(aq),至沉淀完全 | b | |
iii. 再向B中投入一定量NaCl(s) | c | |
iv. 重复i,再向B中加入与iii等量NaCl(s) | a |
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
①实验Ⅲ证明了AgCl转化为AgI,甲溶液是_____________(填序号)。
a. AgNO3溶液 b. NaCl溶液 c. KI溶液
②实验Ⅳ中结合信息,解释电压b<a的原因:_____________。
③实验Ⅳ的现象能说明AgI转化为AgCl,理由是_____________。
(3)综合实验Ⅰ~Ⅳ,下列说法正确的是_____________(填序号)。
a. 溶解度小的沉淀只能转化成溶解度更小的沉淀
b. 电化学是研究物质性质和转化的重要手段之一
c. 某些沉淀转化反应可通过对反应物浓度的调节,实现逆向转化
d. 溶解度差别越大,由溶解度小的沉淀转化为溶解度较大的沉淀越难实现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[Zn(CN)4]2-在水溶液中可与HCHO发生反应生成[Zn(H2O)4]2+和HOCH2CN,下列说法错误的是( )
A.Zn2+基态核外电子排布式为[Ar]3d10
B.1molHCHO分子中含有σ键的数目为3mol
C.HOCH2CN分子中碳原子轨道的杂化类型是sp3
D.[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,结构可表示为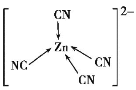
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.恒温恒容密闭容器中反应:H2NCOONH4(s) ![]() 2NH3(g)+CO2(g),混合气体的压强不再改变时说明反应已达平衡
2NH3(g)+CO2(g),混合气体的压强不再改变时说明反应已达平衡
B.汽车尾气催化净化时的反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) ΔH < 0 ,平衡常数为K1;若反应在绝热容器中进行,平衡常数为K2;则K1 < K2
N2(g)+2CO2(g) ΔH < 0 ,平衡常数为K1;若反应在绝热容器中进行,平衡常数为K2;则K1 < K2
C.某恒容密闭容器中反应:nA(g)+mB(g)![]() pC(g)+qD(g) ΔH > 0已达平衡,则降温时c(B)/c(C)的值增大
pC(g)+qD(g) ΔH > 0已达平衡,则降温时c(B)/c(C)的值增大
D.2NO2(g) ![]() N2O4(g)在常温下即可进行,说明正反应是放热反应
N2O4(g)在常温下即可进行,说明正反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现对冶金硅进行电解精炼提纯可降低高纯硅制备成本。相关电解装置如图所示,用Cu-Si合金作硅源,在950℃利用三层液熔盐进行电解精炼,有关说法正确的是
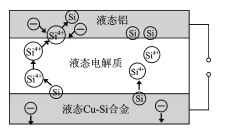
A.在该液相熔体中Cu优先于Si被氧化,Si4+优先于Cu2+被还原
B.液态Cu-Si合金作阳极,固体硅作阴极
C.电流强度的大小不会影响硅提纯速率
D.三层液熔盐的作用是增大电解反应接触面积,提高硅沉积效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有学生将铜与稀硝酸反应实验及NO、NO2性质实验进行改进、整合,装置如图(洗耳球:一种橡胶为材质的工具仪器)。

实验步骤如下:
(一)组装仪器:按照如图装置连接好仪器,关闭所有止水夹;
(二)加入药品:在装置A中的烧杯中加入30%的氢氧化钠溶液,连接好铜丝,在装置C的U型管中加入4.0 mol/L的硝酸,排除U型管左端管内空气;
(三)发生反应:将铜丝向下移动,在硝酸与铜丝接触时可以看到螺旋状铜丝与稀硝酸反应产生气泡,此时打开止水夹①,U型管左端有无色气体产生,硝酸左边液面下降与铜丝脱离接触,反应停止;进行适当的操作,使装置C中产生的气体进入装置B的广口瓶中,气体变为红棕色;
(四)尾气处理:气体进入烧杯中与氢氧化钠溶液反应;
(五)实验再重复进行。
回答下列问题:
(1)实验中要保证装置气密性良好,检验其气密性操作应该在____。
a.步骤(一)(二)之间 b.步骤(二)(三)之间
(2)装置A的烧杯中玻璃仪器的名称是____。
(3)加入稀硝酸,排除U型管左端管内空气的操作是________。
(4)步骤(三)中“进行适当的操作”是打开止水夹____(填写序号),并用洗耳球在U型管右端导管口挤压空气进入。
(5)在尾气处理阶段,使B中广口瓶内气体进入烧杯中的操作是____。尾气中主要含有NO2和空气,与NaOH溶液反应只生成一种盐,则离子方程式为 ___。
(6)某同学发现,本实验结束后硝酸还有很多剩余,请你改进实验,使能达到预期实验目的,反应结束后硝酸的剩余量尽可能较少,你的改进是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积固定的密闭容器中加入反应物N2、H2,发生反应:N2(g)+3H2(g)![]() 2NH3(g)。反应过程中的部分数据如表所示:
2NH3(g)。反应过程中的部分数据如表所示:

下列说法正确的是
A.0~2min内,H2的反应速率为0.1 mol/(L·min)
B.2min时,NH3的物质的量浓度为0.2 mol/L
C.4min时,反应已达到平衡状态,此时正、逆反应的速率都为0
D.4~6min内,容器内气体分子的总物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据研究报道,药物瑞德西韦(Remdesivir)对2019年新型冠状病毒(COVID-19)有明显抑制作用。F为药物合成的中间体,其合成路线如下:
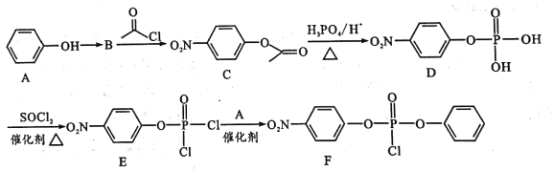
已知:R-OH![]() R-Cl
R-Cl
(1)A中官能团名称是________;C的分子式为_____
(2)A到B为硝化反应,则B的结构简式为___,A到B的反应条件是_____。
(3)B到C、D到E的反应类型 ________(填“相同”或“不相同”);E→F的化学方程式为________ 。
(4)H是C的同分异构体,满足下列条件的同分异构体有_____种。
①硝基直接连在苯环上
②核磁共振氢谱峰面积之比为2:2:2:1
③遇FeCl3溶液显紫色
(5)参照F的合成路线图,设计由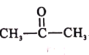 、SOCl2为原料制备
、SOCl2为原料制备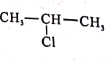 的合成路线_______(无机试剂任选)。
的合成路线_______(无机试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com