
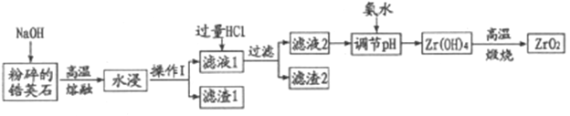
【题目】氧化材料具有高硬度、高强度、高韧性、极高的耐磨性及耐化学腐蚀性等优良的物化性能。以锆英石(主要成分为 ZrSiO4,含有少量Al2O3、SiO2、Fe2O3等杂质)为原料通过碱熔法制备氧化锆(ZrO2)的流程如下:
25℃时,有关离子在水溶液中沉淀时的pH数据:
Fe(OH)3 | Zr(OH)4 | Al(OH)3 | |
开始沉淀时pH | 1.9 | 2.2 | 3.4 |
沉淀完全时pH | 3.2 | 3.2 | 4.7 |
请回答下列问题:
(1)流程中旨在提高化学反应速率的措施有___________。
(2)操作I的名称是___________滤渣2的成分为___________。
(3)锆英石经“高温熔融”转化为Na2ZrO3,写出该反应的化学方程式:___________。
(4)“调节pH”时,合适的pH范围是___________。为了得到纯的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是___________。
(5)写出“高温煅烧”过程的化学方程式___________。根据ZrO2的性质,推测其两种用途___________。
【答案】粉碎、高温 过滤 硅酸(H2SiO3或H4SiO4) ZrSiO4+4NaOH![]() Na2ZrO3+Na2SiO3+2H2O 3.2<pH<3.4 取最后一次洗涤液,向其中滴加稀硝酸,再滴加硝酸银溶液,若无沉淀生成,则Zr(OH)4洗涤干净,否则未洗涤干净 Zr(OH)4
Na2ZrO3+Na2SiO3+2H2O 3.2<pH<3.4 取最后一次洗涤液,向其中滴加稀硝酸,再滴加硝酸银溶液,若无沉淀生成,则Zr(OH)4洗涤干净,否则未洗涤干净 Zr(OH)4![]() ZrO2+2H2O 耐火材料、磨料等
ZrO2+2H2O 耐火材料、磨料等
【解析】
(1)从物质的存在状态、接触面积及反应温度分析影响反应速率的因素;(2)根据混合物成分的不同状态分析分离混合物的方法;结合锆英石的成分中哪些能反应,哪些不能反应,再结合它们的水溶性分析滤渣的成分;(3)根据图示反应物、已知生成物,结合元素守恒,就可得到相应的反应方程式;(4)用氨水调节溶液pH时,要使Zr4+形成Zr(OH)4沉淀,而杂质铝离子存在于溶液中;(5)结合反应物、生成物及反应条件,得到分解反应的方程式,并结合产生该物质的条件分析产物的性质,根据性质决定用途分析产物的用途,据此解答。
(1) 锆英石状态为固态,为提高反应速率,可以通过将矿石粉碎,以增大接触面积;或者通过加热升高反应温度的方法加快反应速率;
(2)操作I是分离难溶于水的固体与可溶性液体物质的方法,名称是过滤;
(3)将粉碎的锆英石与NaOH在高温下发生反应:ZrSiO4+4NaOH![]() Na2ZrO3+Na2SiO3 +2H2O;Al2O3+2NaOH=2NaAlO2+H2O;SiO2+2NaOH=2Na2SiO3+H2O;Fe2O3是碱性氧化物,不能与碱发生反应,所以水浸后过滤进入滤渣1中,Na2ZrO3、Na2SiO3、NaAlO2能溶于水,水浸、过滤进入滤液1中;
Na2ZrO3+Na2SiO3 +2H2O;Al2O3+2NaOH=2NaAlO2+H2O;SiO2+2NaOH=2Na2SiO3+H2O;Fe2O3是碱性氧化物,不能与碱发生反应,所以水浸后过滤进入滤渣1中,Na2ZrO3、Na2SiO3、NaAlO2能溶于水,水浸、过滤进入滤液1中;
(4)向滤液中加入足量盐酸,HCl会与Na2ZrO3、Na2SiO3、NaAlO2发生反应,生成NaCl、H2SiO3(或H4SiO4)、AlCl3、ZrCl4,其中H2SiO3(或H4SiO4)难溶于水,过滤时进入滤渣2中,其余进入滤液2中,因此滤渣2的成分为H2SiO3(或H4SiO4);向滤液2中加入氨水,发生复分解反应,调节溶液的pH至大于Zr(OH)4,而低于开始形成Al(OH)3沉淀的pH,即3.2<pH<3.4,就可以形成Zr(OH)4沉淀,而Al元素仍以Al3+形式存在于溶液中;Zr(OH)4沉淀是从氨水和金属氯化物的混合液中过滤出来的,所以要检验Zr(OH)4是否洗涤干净的方法可通过检验洗涤液中是否含有Cl-离子判断,方法是取最后一次洗涤液,向其中滴加稀硝酸酸化,再滴加硝酸银溶液,若无沉淀生成,则Zr(OH)4洗涤干净,否则未洗涤干净;
(5)将Zr(OH)4沉淀过滤、洗涤,然后高温灼烧,发生分解反应:Zr(OH)4![]() ZrO2+2H2O就得到ZrO2;由于ZrO2是高温分解产生的物质,说明ZrO2熔点高,微粒之间作用力强,物质的硬度大,因此根据ZrO2的这种性质,它可用作制耐火材料、磨料等。
ZrO2+2H2O就得到ZrO2;由于ZrO2是高温分解产生的物质,说明ZrO2熔点高,微粒之间作用力强,物质的硬度大,因此根据ZrO2的这种性质,它可用作制耐火材料、磨料等。


科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d第一电离能大小关系为___________________,e的外围电子排布图为_____________________。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为_________;分子中既含有极性共价键,又含有非极性共价键的化合物是_____________(填化学式,写两种)。
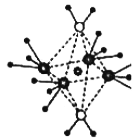
(3)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如下图所示)。该化合物中阴离子为__________,阳离子中存在的化学键类型有________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中符合离子反应 H++OH-=H2O 的是
A. 稀硫酸与稀氨水 B. 稀硫酸与氢氧化钡溶液
C. 浓硝酸与氢氧化钡溶液 D. 盐酸与氢氧化铁胶体反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工生产中含Cu2+的废水常用MnS(s)作沉淀剂,其反应原理为Cu2+(aq)+MnS(s)![]() CuS(s)+Mn2+(aq)。下列有关该反应的推理不正确的是
CuS(s)+Mn2+(aq)。下列有关该反应的推理不正确的是
A. CuS的溶解度比MnS的溶解度小
B. 该反应达到平衡时:c(Cu2+)=c(Mn2+)
C. 往平衡体系中加入少量Cu(NO3)2(s)后,c(Mn2+)变大
D. 该反应平衡常数:K=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向10mL0.1mol/L的HR溶液中逐滴加入0.1mol/L的氨水,所得溶液pH及导电性变化如图。下列分析正确的是

A. a~c点,溶液中离子数目先增大后减小
B. b点溶液pH=7说明c(NH4+)=c(R-)
C. c点溶液存在c(NH4+)>c(R-)>c(H+)>c(OH-)
D. b、c两点对应溶液中,水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关电化学知识的描述正确的是
A. 由于CaO+H2O![]() Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池
Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池
B. 当马口铁(镀锡铁)的镀层破损后,马口铁腐蚀会加快
C. 原电池的电极附近溶液pH的变化可以用电池总反应式来判断
D. 铅蓄电池放电时的正极反应式为PbO2 +4H+ +2e-![]() Pb2+ +2H2O
Pb2+ +2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生反应NO2(g)+SO2(g)![]() SO3(g)+NO(g),下列能说明反应达到平衡状态的是
SO3(g)+NO(g),下列能说明反应达到平衡状态的是
A. 体系压强保持不变B. 混合气体颜色保持不变
C. 混合气体的密度保持不变D. 每消耗1 mol SO3的同时生成1 molNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、铵盐和纯碱的原料,也是一种常用的制冷剂。
(1)某化学研究性学习小组模拟工业合成氨的反应。在容积固定为2L 的密闭容器内充入1mol N2和3mol H2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
反应时间 /min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
则从反应开始到25 min 时,以N2 表示的平均反应速率=__________。
(2)工业合成氨的反应方程式为: N2(g)+3H2(g)![]() 2NH3(g) ΔH 下图Ⅰ是合成氨反应的能量与反应过程相关图(未使用催化剂);图Ⅱ是合成氨反应在2L 容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图。
2NH3(g) ΔH 下图Ⅰ是合成氨反应的能量与反应过程相关图(未使用催化剂);图Ⅱ是合成氨反应在2L 容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图。
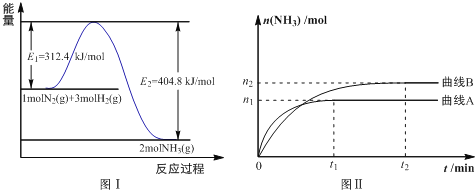
下列说法正确的是________________。
A.ΔH=-92.4kJ/mol
B.使用催化剂会使E1的数值增大
C.为了提高转化率,工业生产中反应的浓度越低越好
D.图Ⅱ是不同温度下反应体系中氨的物质的量与反应时间关系图,且TA>TB;
E.在曲线A条件下,反应从开始到平衡,消耗N2的平均速率为![]() mol·L-1·min-1
mol·L-1·min-1
(3)一定温度下,向一个容积为2 L的密闭容器中通入2 mol N2和7 mol H2,达到平衡时测得容器的压强为起始时的7/9倍,在同一温度,同一容器中,将起始物质改为amol N2 ,b molH2,c mol NH3 (a,b,c均不为零)欲使平衡混合物中各物质的质量与原平衡相同,则a,b,c满足的关系为_____________(用含a,b,c的表达式表示),且欲使反应在起始时向逆反应方向进行,c的取值范围是_______
(二) 在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
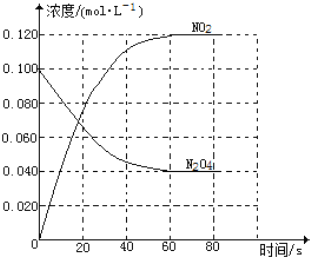
(1)反应的△H______0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为________mol·L-1·s-1
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。T_______100℃(填“大于”“小于”),判断理由是________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向_______(填“正反应”或“逆反应”)方向移动,判断理由是__________________。
(4)已知:
甲醇脱水反应2CH3OH(g)=CH3OCH3(g)+H2O(g) △H1=-23.9kJ·mol-1
甲醇制烯烃反应2CH3OH(g)=C2H4 (g)+H2O(g) △H2=-29.1kJ·mol-1
乙醇异构化反应2CH3OH(g)=CH3OCH3(g)) △H3=+50.7kJ·mol-1
则乙烯气相直接水合反应C2H4 (g)+H2O(g)=C2H5OH(g)的△H=____________ kJ·mol-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com