
【题目】加入0.1 mol MnO2粉末于50 mL过氧化氢溶液(ρ=1.1 g·mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示。

(1)实验时放出气体的总体积是_______________________________________。
(2)放出一半气体所需的时间为_________________________________________。
(3)反应放出3/4气体所需时间为_________________________________________________。
(4)A、B、C、D各点反应速率快慢的顺序为________________________________________。
(5)解释反应速率变化的原因是_______________________________________________。
(6)计算H2O2的初始物质的量的浓度________________________________________。
(7)求反应到2 min时,H2O2的质量分数_______________________________________。
【答案】 60 mL 1 min 2 min D>C>B>A 随着反应的进行,c(H2O2)逐渐降低,反应速率逐渐变慢 0.108 mol·L-1 0.086%
【解析】根据V-t图像知,反应进行到1min时,放出O2的体积为30mL,反应进行至2 min时,放出O2体积为45mL,反应进行至4 min时,放出O2的体积达最大值60mL;由V-t曲线的斜率变化可知:D、C、B、A的反应速率逐渐减小,这是因为随着反应的进行,c(H2O2)逐渐减小,反应速率逐渐变慢;根据2H2O2![]() 2H2O+O2↑,n(H2O2)=0.06×2/22.4mol,所以H2O2的起始物质的量浓度为[0.06×2/22.4]÷0.05=0.108 mol·L-1;反应进行至2 min时,消耗H2O2的物质的量为n′(H2O2)=0.045×2/22.4=0.004 mol,剩余H2O2的物质的量为0.06×2/22.4-0.045×2/22.4=1.34×10-3mol,所以w(H2O2)=
2H2O+O2↑,n(H2O2)=0.06×2/22.4mol,所以H2O2的起始物质的量浓度为[0.06×2/22.4]÷0.05=0.108 mol·L-1;反应进行至2 min时,消耗H2O2的物质的量为n′(H2O2)=0.045×2/22.4=0.004 mol,剩余H2O2的物质的量为0.06×2/22.4-0.045×2/22.4=1.34×10-3mol,所以w(H2O2)= ;根据以上分析解答。
;根据以上分析解答。
(1)由反应方程式为: 2H2O2![]() 2H2O+O2↑,该反应为不可逆反应,最后阶段,收集到的气体体积不再增加,说明过氧化氢完全分解,由图象可以知道,生成氧气的体积为60 mL;正确答案: 60 mL 。
2H2O+O2↑,该反应为不可逆反应,最后阶段,收集到的气体体积不再增加,说明过氧化氢完全分解,由图象可以知道,生成氧气的体积为60 mL;正确答案: 60 mL 。
(2)由图象可以知道,当放出一半气体30 mL时,所需的时间为1 min;正确答案:1 min。
(3)由图象可以知道, 反应放出3/4气体的体积为45mL,所需时间为2 min ;正确答案:2 min。
(4)由曲线的变化特点可以看出,曲线的斜率逐渐变小,说明反应逐渐减慢,则反应速率D>C>B>A;正确答案是: D>C>B>A。
(5)根据图像可以知道,随着反应的进行,c(H2O2)逐渐降低,反应速率逐渐变慢;正确答案:随着反应的进行,c(H2O2)逐渐降低,反应速率逐渐变慢。
(6)根据2H2O2![]() 2H2O+O2↑,n(H2O2)=0.06×2/22.4mol,所以H2O2的起始物质的量浓度为[0.06×2/22.4]÷0.05=0.108 mol·L-1;正确答案:0.108 mol·L-1 。
2H2O+O2↑,n(H2O2)=0.06×2/22.4mol,所以H2O2的起始物质的量浓度为[0.06×2/22.4]÷0.05=0.108 mol·L-1;正确答案:0.108 mol·L-1 。
(7)反应进行至2 min时,消耗H2O2的物质的量为n′(H2O2)=0.045×2/22.4=0.004 mol,剩余H2O2的物质的量为0.06×2/22.4-0.045×2/22.4=1.34×10-3mol,所以w(H2O2)=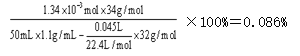 ;正确答案:0.086%。
;正确答案:0.086%。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】根据题意填空:
(1)碳酸钠溶液中各离子按照浓度从大到小的顺序依次为: .
(2)下表是几种常见弱酸的电离平衡常数(25℃)
酸 | H2CO3 | CH3COOH | HClO |
K | K1=4.4×10﹣7;K 2=4.7×10﹣11 | K=1.76×10﹣5 | K=2.95×10﹣8 |
根据分析表格中数据可知,H2CO3、CH3COOH、HClO 三种酸的酸性从强到弱依次是;25℃时,等浓度的Na2CO3、NaAc 和NaClO三种溶液的pH从小到大依次是 .
(3)常温下,将0.02molL﹣1 的 Ba(OH)2溶液100mL和0.02molL﹣1的NaHSO4溶液100mL混合,若忽略溶液体积变化,则混合后的溶液的 pH 为 .
(4)25℃时,Ksp[Mg(OH)2]=5.61×10﹣12 , Ksp[MgF2]=7.42×10﹣11 . 该温度下饱和Mg(OH)2溶液与饱和 MgF2溶液相比,(填化学式)溶液中的 c(Mg2+)大.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于“观察DNA和RNA在细胞中的分布”的实验,下列说法中正确的是( )
A. 染色时先用甲基绿染液,再用吡罗红染液
B. 用质量分数为8%的盐酸的目的之一是使DNA与蛋白质分离,并使DNA水解
C. 酒精灯烘干载玻片,可将细胞固定在载玻片上
D. 用高倍显微镜可以比较清楚地看到呈现绿色的染色体和呈现红的RNA分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联合国卫生组织认为我国使用的铁锅是有益于人类健康的理想炊具。其主要原因是( )
A. 价格便宜,不易生锈 B. 铁具有银白色光泽,导电性好
C. 烹调的食物中留有人体需要的铁元素 D. 传热慢,保温性能好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.1mol/L的醋酸溶液中存在CH3COOHCH3COO﹣+H+ . 要使溶液中 ![]() 值增大,可以采取的措施是( )
值增大,可以采取的措施是( )
A.加少量烧碱固体
B.升高温度
C.加少量冰醋酸
D.加少量醋酸钠固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,既属于吸热反应又属于氧化还原反应的是
A.Al与盐酸的反应B.灼热的碳与二氧化碳的反应
C.碳酸氢钠与盐酸的反应D.Ba(OH)2·8H2O与NH4Cl的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是氢氧燃料电池的示意图,按图中提示,下列叙述不正确的是( )

A. a电极是负极,b电极是正极
B. a电极的电极反应式为H2-2e-===2H+
C. b电极的电极反应式为4OH--4e-===2H2O+O2↑
D. 氢氧燃料电池不需要将还原剂和氧化剂全部储藏在电池内
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() U是重要的核工业原料,下列有关
U是重要的核工业原料,下列有关 ![]() U的说法正确的是( )
U的说法正确的是( )
A.![]() U与
U与 ![]() U互为同素异形体
U互为同素异形体
B.![]() U与
U与 ![]() U互为同位素
U互为同位素
C.![]() U原子核中含有92个中子
U原子核中含有92个中子
D.![]() U原子核外有143个电子
U原子核外有143个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选考(13分)(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、![]() (PAN)等二次污染物。
(PAN)等二次污染物。
①1mol PAN中含有的σ键数目为____。PAN中四种元素的第一电离能由大到小的顺序为__________。
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中中心离子的配位数为________,
心离子的核外电子排布式为_______________。
③相同压强下,HCOOH的沸点比CH3OCH3____(填“高”或“低”),其原因是___________________。
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
①(NH4)2SO4晶体中各种微粒间的作用力不涉及___________(填序号)。
a.离子键
b.共价键
c.配位键
d.范德华力
e.氢键
②NH4NO3中阳离子的空间构型为_____,阴离子的中心原子轨道采用_______杂化。
(3)测定大气中PM2.5的浓度方法之一是β—射线吸收法,β—射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则m/n=_____(填数字)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com