
ЁОЬтФПЁПNH4Al(SO4)2ЁЄ12H2OЫзГЦяЇУїЗЏЃЌЦфаджЪЮШЖЈЃЌЪЧЛЏбЇЪЕбщГЃгУЕФЛљзМЪдМСЁЃгУЬМЫсЧтяЇгыСђЫсФЦПЩвджЦБИДПОЛЕФяЇУїЗЏЃЌжЦБИЙ§ГЬШчЭМЃЌЯТУцЫЕЗЈВЛе§ШЗЕФЪЧ
A.МгШыNH4HCO3БЅКЭШмвКЗЂЩњЗДгІЕФРызгЗНГЬЪНЃКNa++HCO3-=NaHCO3Ё§
B.ЕїНкpHЪБЃЌЮЊСЫМѕЩйЫ№КФЃЌЬсИпВњТЪЃЌПЩНЋpHЪджНжБНгНўШыТЫвКaжа
C.ВйзїЂђЕФЛљБОЙ§ГЬЮЊеєЗЂХЈЫѕЁЂРфШДНсОЇЁЂЙ§ТЫЁЂЯДЕгЁЂИЩдя
D.ШєЙ§СПЕФЦјЬхaЭЈШыЕНБЅКЭЕФДПМюШмвКжаЛсгаОЇЬхЮіГіЃЌИУОЇЬхгыЙЬЬхaЯрЭЌ
ЁОД№АИЁПB
ЁОНтЮіЁП
A. ЬМЫсЧтФЦШмНтЖШаЁгкNH4HCO3ЃЌМгШыNH4HCO3БЅКЭШмвКЗЂЩњЗДгІЯДГіЬМЫсЧтФЦОЇЬхЃЌРызгЗНГЬЪНЃКNa++HCO3-=NaHCO3Ё§ЃЌЙЪAе§ШЗЃЛ
B. ВЛФмНЋpHЪджНжБНгНўШыТЫвКaжаЃЌЛсЖдЪдМСдьГЩЮлШОЃЌЙЪBДэЮѓЃЛ
C. ВйзїЂђЪЧДгяЇУїЗЏШмвКЕУЕНЕУЕНяЇУїЗЏЙЬЬхЃЌгЩгкяЇУїЗЏДјНсОЇЫЎЃЌЫљвдВЩШЁеєЗЂХЈЫѕЁЂРфШДНсОЇЁЂЙ§ТЫЁЂЯДЕгЁЂИЩдяЕФЗНЗЈЛёЕУЃЌЙЪCе§ШЗЃЛ
D. ЦјЬхaЮЊЖўбѕЛЏЬМЃЌЭЈШыЕНБЅКЭЕФДПМюШмвКжаЃЌвВЛсВњЩњЬМЫсЧтФЦОЇЬхЮіГіЃЌгыЙЬЬхaГЩЗжЯрЭЌЃЌЙЪDе§ШЗЁЃ
Д№АИбЁBЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
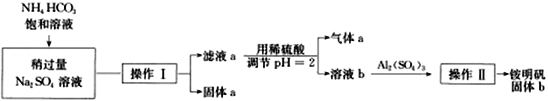
ЁОЬтФПЁПЯТБэЫљСаИїзщЮяжЪжаЃЌЮяжЪжЎМфЭЈЙ§вЛВНЗДгІФмЪЕЯжШчЭМЫљЪОзЊЛЏЙиЯЕЕФЪЧ
X | Y | Z | ЮяжЪзЊЛЏЙиЯЕ | |
A | Cu | CuO | Cu(OH)2 |
|
B | S | SO3 | H2SO4 | |
C | NaHCO3 | Na2CO3 | NaOH | |
D | FeCl2 | FeO | FeCl3 |
A.AB.BC.CD.D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПАДвЊЧѓЛиД№ЯТСаЮЪЬтЃК
(1)ЭщЬўAдкЭЌЮТЁЂЭЌбЙЯТеєЦјЕФУмЖШЪЧH2ЕФ36БЖЃЌЦфЗжзгЪНЮЊ___________ЁЃ
(2)аДГіЬьШЛЯ№НКЕЅЬх(2-МзЛљ-1ЃЌ3-ЖЁЖўЯЉ)ЕФНсЙЙМђЪН_________ЁЃ
(3)СЂЗНЭщ![]() ЕФвЛТШДњЮяга_________жжЃЌЫќЕФСљТШДњЮяга_________жжЁЃ
ЕФвЛТШДњЮяга_________жжЃЌЫќЕФСљТШДњЮяга_________жжЁЃ
(4)ЯТСаЮяжЪЕФЗаЕуАДгЩИпЕНЕЭЕФЫГађХХСае§ШЗЕФЪЧ___________ЁЃ
ЂйCH3(CH2)2CH3 ЂкCH3(CH2)3CH3 Ђл (CH3)3CH Ђм (CH3)2CHCH2CH3
A.ЂкЂмЂйЂл B. ЂмЂкЂйЂл C.ЂмЂлЂкЂй D.ЂкЂмЂлЂй
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯђNaOHКЭNa2CO3ЛьКЯШмвКжаЕЮМг0.1 molЁЄL1ЯЁбЮЫсЃЌCO2ЕФЩњГЩСПгыМгШыбЮЫсЕФЬхЛ§ЕФЙиЯЕШчЭМЁЃЯТСаХаЖЯе§ШЗЕФЪЧ
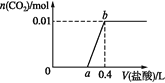
A. дк0~aЗЖЮЇФкЃЌжЛЗЂЩњжаКЭЗДгІ
B. abЖЮЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊЃК![]()
C. a=0.3
D. дЛьКЯШмвКжаNaOHгыNa2CO3ЕФЮяжЪЕФСПжЎБШЮЊ1ЁУ2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЭЕЅжЪМАЦфЛЏКЯЮядкКмЖрСьгђгаживЊгУЭОЃЌШчН№ЪєЭгУРДжЦдьЕчЯпЕчРТЃЌЮхЫЎСђЫсЭПЩгУзїЩБОњМСЁЃ
(1)ЯђCuSO4ШмвКжаМгШыЙ§СПNaOHШмвКПЩЩњГЩ[Cu(OH)4]2-ЁЃВЛПМТЧПеМфЙЙаЭЃЌ[Cu(OH)4]2-ЕФНсЙЙПЩгУЪОвтЭМБэЪОЮЊ_____________________________ЃЌCuЮЛгкдЊЫижмЦкБэЕкЂёBзхЁЃCu 2ЃЋЕФКЫЭтЕчзгХХВМЪНЮЊ____________________ЁЃ
(2)ЕЈЗЏCuSO4ЁЄ5H2OПЩаДГЩ[Cu(H2O) 4 ]SO4 ЁЄH2OЃЌЦфНсЙЙЪОвтЭМШчЯТЃК
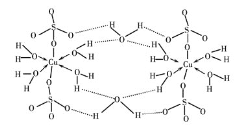
ЯТСаЫЕЗЈе§ШЗЕФЪЧ________(ЬюзжФИ)ЁЃ
AЃЎЫЎжаЕФбѕдзгВЩгУsp3 дгЛЏ
BЃЎбѕдзгВЮгыаЮГЩХфЮЛМќКЭЧтМќСНжжЛЏбЇМќ
CЃЎCu2+ЕФМлЕчзгХХВМЪНЮЊ3d84s1
DЃЎЕЈЗЏжаЕФЫЎдкВЛЭЌЮТЖШЯТЛсЗжВНЪЇШЅ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПFe2(SO4)3ШмвКПЩгУгкИЏЪДОјдЕАхЩЯЕФЭВЃЌжЦдьгЁЫЂЕчТЗАхЁЃЯжЩшМЦСЫвЛИіЗНАИШчЯТЃЌДгИЏЪДКѓЕФЗЯвК(жївЊКЌFe3+ЁЂFe2+ЁЂCu2+)жаЛиЪеЭЃЌВЂжиаТЛёЕУFe2(SO4)3ШмвКЁЃ
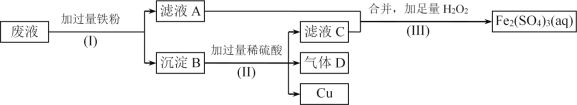
(1)ВНжш(I)жаЗжРыВйзїУћГЦЮЊ____________________ЁЃ
(2)ГСЕэBЕФжївЊГЩЗжга____________________ЃЌЦјЬхDЕФЕчзгЪНЮЊ__________ЁЃ
(3)аДГіВНжш(III)жаЗЂЩњЗДгІЕФРызгЗНГЬЪН______________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЬМЫсФЦКЭЬМЫсЧтФЦЖМЪЧжабЇГЃМћЛЏбЇвЉЦЗЁЃ
Ђё.ЯТУцЪЧдкЪЕбщЪвжаФЃФтЁАКюЪЯжЦМюЗЈЁБжЦШЁNaHCO3ЕФзАжУЃК
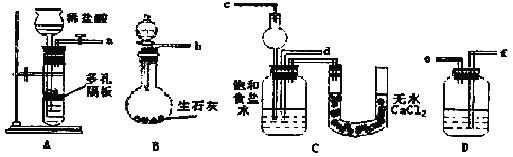
ЧыЛиД№ЯТСаЮЪЬтЃЈЬсЪОBЗжвКТЉЖЗжаЮЊХЈАБЫЎЃЌЕЮШыЩеЦППЩВњЩњАБЦјЃЉЃК
ЃЈ1ЃЉзАжУЕФСЌНгЫГађЪЧЃКaНг___ЃЌ___Нг___ЃЛbНг___ЁЃ
ЃЈ2ЃЉМьВщзАжУЦјУмадКѓЃЌБиаыЯШШУ___ЃЈЬюAЛђBЃЉзАжУЯШЗЂЩњЗДгІЁЃCжагУЧђаЮИЩдяЙмЖјВЛгУжБЕМЙмЃЌЦфзїгУЪЧ___ЁЃ
ЃЈ3ЃЉCжаЙуПкЦПФкВњЩњЙЬЬхЕФзмЛЏбЇЗНГЬЪНЮЊ___ЁЃ
Ђђ.ЭЈЙ§МгШШЗжНтЕФЗНЗЈПЩвдВтЖЈЬМЫсФЦКЭЬМЫсЧтФЦЕФКЌСПЁЃШЁ13.08gЬМЫсФЦКЭЬМЫсЧтФЦЕФЛьКЯЮяГфЗжМгШШЃЌНЋЩњГЩЕФCO2ЦјЬхЭЈШызуСПЕФГЮЧхЪЏЛвЫЎжаЃЌВтЕУЩњГЩГСЕэЕФжЪСПЮЊ4.0gЁЃ
ЃЈ4ЃЉМгШШЪБЗЂЩњЕФЛЏбЇЗДгІЗНГЬЪНЮЊ___ЁЃ
ЃЈ5ЃЉдЛьКЯЮяжаЬМЫсФЦКЭЬМЫсЧтФЦЕФЮяжЪЕФСПжЎБШЮЊ___ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЬњПѓЪЏЃЈШєжЛКЌЬњЕФбѕЛЏЮяКЭSiO2ЃЉШЁ36gШмгкЙ§СПЕФЯЁбЮЫсжаЃЌЙ§ТЫЁЂЯДЕгЁЂИЩдяКѓЕУ5.6gВЛШмЮяЃЌЯђЕУЕНЕФТЫвКжаМгШызуСПЕФNaOHШмвКЃЌЙ§ТЫЁЂЯДЕгКѓНЋГСЕэзЦЩеЃЌЕУ32gКьзиЩЋЙЬЬхЃЎИљОнЬтвтЯТСаНсТлВЛе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
A. гЩЬњПѓЪЏзЊЛЏЮЊКьзиЩЋЙЬЬхЕФЙ§ГЬжаЗЂЩњСЫбѕЛЏЛЙдЗДгІ
B. ШмгкбЮЫсКѓЕУЕНЕФТЫвКжаnЃЈFe2+ЃЉЃКnЃЈFe3+ЃЉ=1ЃК1
C. ЬњПѓЪЏжаЕФЬњЕФбѕЛЏЮяЕФЛЏбЇЪНвЛЖЈЪЧFe3O4
D. ШєЯЁбЮЫсЮЊ3.0molLЉ1 400mLЃЌЗДгІЧАКѓЬхЛ§БфЛЏКіТдВЛМЦЃЌдђТЫвКжаЪЃгрH+ЕФЮяжЪЕФСПХЈЖШЪЧ0.5molLЉ1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПТСЪЧживЊЕФН№ЪєВФСЯЃЌТСЭСПѓ(жївЊГЩЗжЪЧAl2O3КЭЩйСПЕФSiO2ЁЂFe2O3дгжЪ)ЪЧЙЄвЕЩЯжЦШЁТСЕФдСЯЁЃЪЕбщЪвФЃФтЙЄвЕЩЯвдТСЭСПѓЮЊдСЯжЦяЇУїЗЏОЇЬх[NH4Al(SO4)2]ЕФЙЄвеСїГЬШчЭМЫљЪОЃК
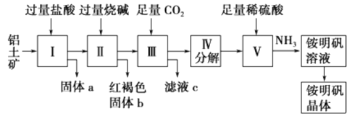
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)ЙЬЬхaЕФЛЏбЇЪНЮЊ________ЃЌЙЬЬхbЛЏбЇЪНЮЊ________ЃЌЂѓжаЭЈШызуСПCO2ЦјЬхЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ________________ЁЃ
(2)гЩЂѕжЦШЁяЇУїЗЏШмвКЕФЛЏбЇЗНГЬЪНЮЊ__________________ЁЃ
(3)гЩЂёЁњЂђЁњЂѓЁњЂєЖМвЊгУЕНЕФЗжРыЗНЗЈЪЧ__________________ЃЌгЩяЇУїЗЏШмвКжажЦяЇУїЗЏОЇЬхЕФВйзїЪЧ__________________ЁЃ
(4)ШчЙћЯШЯђТСЭСПѓМгШыЙ§СПЧтбѕЛЏФЦЃЌдйМгШыЙ§СПбЮЫсЃЌДЫЪБЪзЯШГіЯжЕФЙЬЬхaЪЧ__________ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com