
 ij�¶�ʱ����2L������X��Y��Z�����������ʵ����ʵ�����n������ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ�����
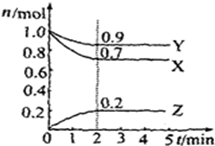
ij�¶�ʱ����2L������X��Y��Z�����������ʵ����ʵ�����n������ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ��������� ��1������ͼ����������ʵ�����������������С���Ƿ�Ӧ��ٸ��ݲμӷ�Ӧ�����ʵ���֮�ȵ����������֮�ȵü�������
��2�����г�����ʽ��������Ũ�ȹ�ʽ���㣻
��3����ѧ��Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�ɴ�������һЩ�������������仯��
��� ��1������ͼ����������ʵ�����������������С���Ƿ�Ӧ����Է�Ӧ����X��Y����������Z��X��Y��Z���ʵ����ı仯���ֱ�Ϊ��0.3 mol��0.1mol��0.2mol�����ݲμӷ�Ӧ�����ʵ���֮�ȵ����������֮�ȵü�����������X��Y��Z�ļ�����֮��Ϊ3��1��2���ʴ�Ϊ��3X+Y?2Z��
��2����Ӧ��ʼ��2min��Z���ʵ����ı仯��Ϊ0.2mol��
�� 3X+Y?2Z
��ʼ1.0 1.0 0
ת��0.3 0.1 0.2
ƽ��0.7 0.9 0.2
������X��ʾ��ƽ����Ӧ����Ϊv��X��=$\frac{��c}{��t}$=$\frac{\frac{0.3}{2}}{2}$=0.075mol/mol•L-1•mi-1��
ƽ��ʱ��Y��ת����Ϊ$\frac{0.1}{1.0}$��100%=10%��
ƽ��ʱ��Z��Ũ��Ϊ$\frac{0.2}{2}$=0.1mol/L��
�ʴ�Ϊ��0.075��10%��0.1��
��3��A��X��Y��Z�����ʵ���֮���뷴Ӧ��ʼʱ�����ʵ�����ƽ��ʱת���ij̶��йأ�����˵��������Ӧ�ﵽƽ��״̬����A����
B����Ӧǰ������ļ�����֮�Ͳ���ȣ���������ѹǿ����ʱ��ı仯���仯��˵��������Ӧ�ﵽƽ��״̬����B��ȷ��
C�����۷�Ӧ�Ƿ�ƽ�⣬��λʱ����ÿ����3molX��ͬʱ����2molZ����C����
D����Ӧ��ѭ�����غ㶨�ɣ������Ƿ�ƽ�⣬������������������ʱ��ı仯���仯������˵��������Ӧ�ﵽƽ��״̬����D����
E����ѧ��Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�������������ʵ�������ʱ��ı仯���仯������˵��������Ӧ�ﵽƽ��״̬����E��ȷ��
�ʴ�Ϊ��B��E��
���� ���⿼�����ʵ�����ʱ��ı仯���ߣ��Լ�ƽ��״̬���жϣ���Ŀ�ѶȲ���ע��ƽ��״̬���жϽǶȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 55.43% | B�� | 44.57% | C�� | 40% | D�� | 49% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��100�桢101 kPa�����£�1 molҺ̬ˮ����ʱ��Ҫ����40.69 kJ����������H2O��g���TH2O��l���ġ�H=+40.69 kJ•mol-1 | |
| B�� | ��֪CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-802.33 kJ•mol-1����CH4��ȼ����Ϊ802.33 kJ | |
| C�� | ϡ������0.1 mol•L-1NaOH��Һ��Ӧ���Ȼ�ѧ����ʽΪ��H+��aq��+OH-��aq��=H2O��l����H=-57.3 kJ•mol-1 | |
| D�� | ��֪S��g��+O2��g���TSO2��s����H1��S��g��+O2��g���TSO2��g����H2�����H2����H1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��֪��25�桢1.013��105Pa�£�1mol������ȫȼ������Һ̬ˮ�ų�285kJ����������ش��������⣺
��֪��25�桢1.013��105Pa�£�1mol������ȫȼ������Һ̬ˮ�ų�285kJ����������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƾ���ȼ����ΪQ3 kJ | |
| B�� | ��ʹ46 g�ƾ�Һ����ȫȼ�գ����ָ������£��ͷų�������Ϊ��3Q1-Q2+Q3��kJ | |
| C�� | H2O��g����H2O��l���ͷų������������Ըù���Ϊ��ѧ�仯 | |
| D�� | �ӷ�Ӧ�ۿ�֪1mol C2H5OH��g����������2 mol CO2��g����3 mol H2O��g���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ӧ���䰮��������ѧ���о����Ӵ��ж��к����ʣ�����Ӧ��Զ�뻯ѧ | |
| B�� | ��ѧѧ����Ҫ�����۲������о����ʵ�һ����ʵ��Ϊ��������Ȼ��ѧ | |
| C�� | ��ѧѧ�Ƽ縺�ſ������о��²��ϡ�����Դ���������Ҫ���� | |
| D�� | ��ѧѧ�Ƶķ�չ���������������Ľ���������Ҫ���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com