
【题目】某物质跨膜运输的方式如下图甲,则该过程与下图的哪条曲线最相符
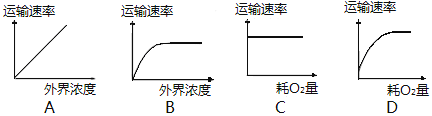
A. A B. B C. C D. D
【答案】D
【解析】
甲所示物质是逆浓度梯度跨膜运输,需载体蛋白协助且消耗能量,其方式为主动运输。A曲线显示:物质的运输速率随着外界浓度的增加而增加,说明只受物质浓度差的影响,可判断为自由扩散,A项错误;B曲线图显示,物质的运输速率,在一定范围内,随着外界浓度的增加而增加,超过该范围,不再随被转运分子浓度的增加而增加,说明受到载体数量的限制,可判断为协助扩散或主动运输,B项错误;C曲线显示:物质的运输速率不随O2浓度的增加而增加,说明不需要能量,可判断为自由扩散或协助扩散,C项错误;D曲线显示:物质的运输速率在一定范围内,随O2浓度的增加而增加,超过该范围,不再随O2浓度的增加而增加,说明受到能量和载体数量的限制,可判断为主动运输,D项正确。


科目:高中化学 来源: 题型:
【题目】氨和肼(N2H4)都是氮元素的重要氢化物,在工农业生产、生活中有广泛应用。
(1)工业中常用以下反应合成氨:N2+3H2![]() 2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.100mol/L,c(H2)=0.300mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示:
2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.100mol/L,c(H2)=0.300mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示:
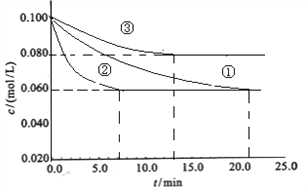
装罝③仅有一个反应条件与①不同,该条件为_______________,实验②平衡时H2的转化率为_____________;
(2)肼是一种具有强还原性的无色油状液体,可用作燃料。
①在火箭推进器中装有胼(N2H4)和液态H2O2,已知0.4mol液态N2H4和足量液态H2O2反应,生成气态N2和气态H2O,放出256.6kJ的热量。该反应的热化学方程式为_____________________________________________________。
②肼(N2H4)-空气燃料电池是一种环保型碱性燃料电池,电解质溶液是20%-30%的KOH溶液。已知肼在101kPa、25℃条件下的燃烧热为624kJ·mol-1,如果此燃料电池的能量转化率为50%,当消耗空气2.24L(已折算为标准状况下体积)时,则此电池产生的电能约为_________kJ。(假设空气中氧气的体积含量为20%,产物为液态水)

(3)肼又称“联氨”,为二元弱碱,在水中的电离方程式与氨相似,肼第一步电离反应的平衡常数值为____________.(已知:N2H4+H+![]() N2H5+ 的K=8.7×107;KW =1.0×10-14)
N2H5+ 的K=8.7×107;KW =1.0×10-14)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH标准溶液滴定未知浓度的盐酸,用酚酞为指示剂,造成测定结果偏高的原因可能是
A. 配制标准溶液的NaOH中混有Na2CO3 杂质
B. 盛装待测液的锥形瓶用燕馏水洗过,没有用待测液洗
C. 滴定到终点读数时,俯视刻度线
D. 滴定到终点读数时,滴定管尖嘴处有气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)①H2 + CuO ![]() Cu + H2O
Cu + H2O
②CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O
③3S + 6NaOH ![]() 2Na2S + Na2SO3 + 3H2O
2Na2S + Na2SO3 + 3H2O
④NH4NO3 + Zn = ZnO + N2↑+ 2H2O
⑤Cu2O + 4HCl = 2HCuCl2 + H2O
上述反应中,属于氧化还原反应的是__________________________(填序号)
(2)SeO2、KI和HNO3可发生反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O,配平该反应的化学方程式并用双线桥法标出电子转移的方向和数目:____________________________。
(3)在反应 KIO3 + 6HI = 3I2 + KI + 3H2O中,氧化剂与还原剂的物质的量之比为__________。
Ⅱ.已知:
① 2H2O + Cl2 + SO2 = H2SO4 + 2HCl ② 2KMnO4 + 16HCl = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
(4)根据以上两个反应可以得出氧化剂和还原剂的强弱顺序,请写出由KMnO4、K2SO4 、MnSO4 、SO2、H2O、H2SO4 这六种物质组成的氧化还原反应的方程式并配平:_______________________。
在反应②中,若有18.25g HCl被氧化,求:
(5)转移的电子数为:_______________。
(6)标况下生成Cl2的体积(请列式计算)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于加成反应的是( )
A.乙醇与钠反应生成乙醇钠和氢气
B.乙烯与氯化氢反应生成一氯乙烷
C.乙酸与乙醇反应生成乙酸乙酯和水
D.甲烷与氯气反应生成一氯甲烷和氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将V1mL1.00mol·L-1HCl溶液和V2mL未如浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是( )

A. 做该实验时环境温度为22℃ B. 该实验表明化学能可以转化为热能
C. NaOH溶液的浓度约为1.00mol·L-1 D. 该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋资源应用非常广泛,从中可提取氯化钠、碘等化工产品。回答下列问题:
I.实验室用氯化钠固体配制1.0molL-1的食盐水500mL。
(1)所需仪器为容量瓶(规格为____)、托盘天平、烧杯、玻璃棒和_____。
(2)配制时,下列操作对所配溶液的浓度有何影响?(填字母)无影响的有_____,偏大的有______,偏小的有_______。
A.称量时使用了生锈的砝码
B.往容量瓶中移液时,有少量液体溅出
C.容量瓶未干燥即用来配制溶液
(3)若加蒸馏水定容时不慎超过了刻度线,应如何处理?_______
II.海藻中含有丰富的碘元素,某课外活动小组欲从海藻中提取碘(已知过程②中反应的离子方程式为2I—+C12=2C1—+I2),设计如下的流程:

(4)指出提取碘的过程中有关实验操作的名称:①_______,③______。
(5)提取碘的过程中,可选择的有机溶剂是______。
A.酒精 B.醋酸 C.苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施或事实能用勒沙特列原理解释的是( )
A.在合成氨(正反应是放热)的反应中,升温有利于氨的合成
B.H2、I2、HI三者的平衡混合气,加压(缩小容器体积)后颜色变深
C.钢铁在潮湿的空气中更容易生锈
D.氯气可以用排饱和食盐水的方法收集
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com