
【题目】铁和钴是重要的过渡元素。
(1)钴位于元素周期表中第___族,基态钴原子中未成对电子的个数为_____。
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中中心离子Fe3+的核外价电子排布式为___;尿素分子中氮原子的杂化方式是___,尿素中所含非金属元素的电负性由大到小的顺序是___。
(3)Co(NH3)5BrSO4可形成两种结构的钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:
在第一种配合物溶液中加硝酸银溶液产生白色沉淀。
在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀,则第二种配合物的配体为_____。
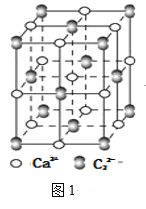
(4)离子化合物CaC2的一种晶体结构如图1所示,从钙离子看,属于____堆积,其配位数是_____;一个晶胞中平均含有的π键的个数为_____。
(5)科学研究结果表明。碳的氧化物CO2能够与H2O借助于太阳能制备HCOOH,其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中σ键和π键的个数比是____。
(6)奥氏体是碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为______,若晶体密度为ρg/cm3,则晶胞中最近的两个碳原子的距离为_____pm(阿伏加德罗常数的值用NA表示,写出计算式即可)。

【答案】Ⅷ 3 3d5 sp3 O>N>C>H SO42-、NH3 面心立方最密 6 4 4:1 FeC ![]()
【解析】
(1)Co是27号元素,处于周期表中第四周期第Ⅷ族,核外电子排布式为1s22s22p63s23p63d74s2;
(2)Fe的核外电子排布式为1s22s22p63s23p63d64s2,原子形成阳离子先失去高能层中电子,同一能层先失去高能级电子;分子中C原子形成3个σ键,没有孤电子对,杂化轨道数目为3;同周期主族元素随原子序数增大电负性增大,C、N、O在它们的氢化物中均表现负化合价,说明它们的电负性都比H元素的大;
(3)在第一种配合物溶液中加硝酸银溶液产生白色沉淀,说明外界为SO42-,Br-为配体,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀,说明Br-为外界,而SO42-为配体;
(4)钙离子处于顶点、面心位置,钙离子为心立方最密堆积;以顶点钙离子研究,与之最近的C22-处于棱中间,且关于顶点钙离子对称;均摊法计算晶胞中C22-数目,每个C22-含有1个σ键;
(5)HCOOH分子结构式为![]() ,单键为σ键,双键含有1个σ键、1个π键;
,单键为σ键,双键含有1个σ键、1个π键;
(6)Fe原子处于顶点、面心,碳原子处于体心、棱中心,均摊法计算Fe、C原子数目确定化学式;晶胞中最近的两个碳原子的距离为同一顶点的2条棱中心2个碳原子的距离。
(1)Co是27号元素,处于周期表中第四周期第Ⅷ族,核外电子排布式为1s22s22p63s23p63d74s2,基态钴原子中3d轨道有3个未成对电子;
(2)Fe的核外电子排布式为1s22s22p63s23p63d64s2,Fe3+的核外价电子排布式为3d5;分子中C原子形成3个σ键,没有孤电子对,杂化轨道数目为3,碳原子杂化方式为sp3;同周期主族元素随原子序数增大电负性增大,C、N、O在它们的氢化物中均表现负化合价,说明它们的电负性都比H元素的大,电负性为:O>N>C>H;
(3)在第一种配合物溶液中加硝酸银溶液产生白色沉淀,说明外界为SO42-,Br-为配体,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀,说明Br-为外界,而SO42-为配体,还有5个NH3为配体;
(4)钙离子处于顶点、面心位置,钙离子为心立方最密堆积;以顶点钙离子研究,与之最近的C22-处于棱中间,且关于顶点钙离子对称,钙离子的配位数为6;晶胞中C22-数目=1+12×![]() =4,每个C22-含有1个σ键,故一个晶胞含有的σ键平均有4个;
=4,每个C22-含有1个σ键,故一个晶胞含有的σ键平均有4个;
(5)HCOOH分子结构式为![]() ,单键为σ键,双键含有1个σ键、1个π键,分子中σ键和π键的个数比是4:1;
,单键为σ键,双键含有1个σ键、1个π键,分子中σ键和π键的个数比是4:1;
(6)Fe原子处于顶点、面心,碳原子处于体心、棱中心,晶胞中Fe原子数目=6×![]() +8×
+8×![]() =4、C原子数目=1+12×
=4、C原子数目=1+12×![]() =4,Fe、C原子数目之比为1:1,故该晶体的化学式为:FeC。在其晶胞中,最近的两个碳原子的距离为同一顶点的2条棱中心2个碳原子的距离,设晶胞中最近的两个碳原子的距离为rpm,则晶胞棱长=
=4,Fe、C原子数目之比为1:1,故该晶体的化学式为:FeC。在其晶胞中,最近的两个碳原子的距离为同一顶点的2条棱中心2个碳原子的距离,设晶胞中最近的两个碳原子的距离为rpm,则晶胞棱长=![]() rpm,晶胞质量=dg/cm3×(
rpm,晶胞质量=dg/cm3×(![]() r×10-10cm)3/span>=4×
r×10-10cm)3/span>=4×![]() g,解得r=
g,解得r=![]() 。
。


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
【题目】解热镇痛药贝诺酯的合成路线如下:

请回答下列问题:
(1)水杨酸的系统命名____;阿斯匹林所含官能团的名称____,水杨酸(C)→阿司匹林(D)的反应类型为_____。
(2)扑热息痛的同分异构体中含有苯环,苯环上有两个取代基,氨基直接连在苯环上且属于酯类的有____种,写出任意一种同分异构体的结构简式___(任写一种)。
(3)F的结构简式为_________。
(4)生成贝诺酯的化学方程式为_________。
(5)已知上述B物质为苯酚钠。水杨酸的制备也可以以甲苯为原料制取,由甲苯为原料结合上述流程图合成水杨酸的合理流程图如下:
![]()
请回答下列问题:
试剂I为_____,试剂II为_____,物质Y为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某溶液M中存在的离子有Na+、A2、HA、H+、OH,存在的分子有 H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式:_____________________________________;
(2)若溶液M是由10 mL 2 mol/L NaHA溶液与2 mol/L NaOH溶液等体积混合而得到 的,则溶液M的pH__________7(填“>”、“<”或“=”),溶液中离子浓度由大到小的顺序为_____________________________。已知Ksp(BaA)= 1.8×1010,向该混合溶液中加入10 mL 1 mol/L BaCl2溶液,混合后溶液中Ba2+ 浓度为________________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石嘴山市打造“山水园林城市”,因此研究NOx、SO2等大气污染物的妥善处理具有重要意义。
(1)SO2的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的SO2。
已知吸收过程中相关反应的热化学方程式如下:
①SO2(g)+NH3·H2O(aq)= NH4HSO3(aq) ΔH1=a kJ/mol;
②NH3·H2O(aq)+ NH4HSO3(aq)=(NH4)2SO3(ag)+H2O(l) ΔH2=b kJ/mol;
③2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq) ΔH3=c kJ/mol。
则反应2SO2(g)+4NH3·H2O(aq)+O2(g) =2(NH4)2SO4(aq)+2H2O(l)的ΔH=______kJ/mol。
(2)燃煤发电厂常利用反应2CaCO3(s)+2SO2(g)+O2(g)![]() 2CaSO4(s)+2CO2(g) ΔH =681.8 kJ/mol对煤进行脱硫处理来减少SO2的排放。对于该反应,在温度为TK时,借助传感器测得反应在不同时间点上各物质的浓度如下:
2CaSO4(s)+2CO2(g) ΔH =681.8 kJ/mol对煤进行脱硫处理来减少SO2的排放。对于该反应,在温度为TK时,借助传感器测得反应在不同时间点上各物质的浓度如下:
时间/min 浓度/mol·L1 | 0 | 10 | 20 | 30 | 40 | 50 |
O2 | 1.00 | 0.79 | 0.60 | 0.60 | 0.64 | 0.64 |
CO2 | 0 | 0.42 | 0.80 | 0.80 | 0.88 | 0.88 |
①0~10 min内,平均反应速率v(SO2)=_____mol/(L·min)。
②30min后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是_____(填字母)。
A.通入一定量的O2 B.加入一定量的粉状碳酸钙
C.适当缩小容器的体积 D.加入合适的催化剂
(3)NOx的排放主要来自于汽车尾气,有人利用反应C(s)+2NO(g)![]() N2(g)+CO2(g) ΔH=34.0 kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) ΔH=34.0 kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:

由图可知,1050K前反应中NO的转化率随温度升髙而增大,其原因为_______;在1100K时,CO2的体积分数为______。
(4)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106 Pa时,该反应的化学平衡常数Kp=____[已知:气体分压(P分)=气体总压(P)×体积分数]。
(5)汽车尾气还可利用反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH=746.8 kJ/mol,实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
N2(g)+2CO2(g) ΔH=746.8 kJ/mol,实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数____(填“>”“<”或“=”)k逆增大的倍数。
②若在1L的密闭容器中充入1 molCO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则k正︰k逆=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用如图装置制取氨气并探究氨气的有关性质:

(1)装置A中烧瓶内试剂可选用________(填序号)。
a.浓硫酸 b.碱石灰 c.五氧化二磷 d.NaOH固体
(2)若探究氨气的溶解性,标准状况下,装置D中收集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是________;完成喷泉实验后,装置D中充满液体,则装置D中溶液的物质的量浓度为__________。(保留两位有效数字)
(3)K2的导管末端需要连接氨气的吸收装置,则不能在K2的导管末端连接如图中的________装置(填序号Ⅰ、Ⅱ、Ⅲ)。
备选装置(其中水中含酚酞试液) | ||
|
|
|
Ⅰ | Ⅱ | Ⅲ |
(4)若探究氨气的还原性,需关闭K1、K3,K2处导管连接制取纯净、干燥氯气的装置。
①D中氨气与氯气反应产生白烟,同时生成一种化学性质稳定气体单质,该反应可用来检验氯气管道是否有泄漏,则该反应的化学方程式为______。
②尾气可用C装置处理,若尾气中含有少量Cl2,则C装置中吸收氯气发生的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚不仅是重要的化工原料,而且还是性能优良的能源和车用燃料。现代工业上可通过煤化工的产物CO和H2来合成二甲醚,其主要反应为:
(ⅰ)CO(g)+2H2(g)![]() CH3OH(g) △H= -90.1kJ·mol-1
CH3OH(g) △H= -90.1kJ·mol-1
(ⅱ)2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H= -24.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H= -24.5kJ·mol-1
(1)写出CO和H2来直接合成二甲醚的热化学方程式________。
(2)温度T时,在容积为2.00L的某密闭容器中进行上述反应(ⅰ),反应过程中相关数据如图1所示。
①下列说法能表明反应已达到平衡状态的是______。
a.容器中气体的压强不再变化 b.混合气体的密度不再变化
c.混合气体的平均相对分子质量不再变化 d.2υ正(H2)=υ逆(CH3OH)
②该化学反应0~10min的平均速率υ(H2)=_____。
③其他条件不变时,15mim时再向容器中加入等物质的量的CO和H2,则H2的转化率____(填增大、不变或减小)。

④对应气相反应,常用某组分(B)的平衡压强(pB)代替某物质的量浓度(cB)表示平衡常数(以Kp表示),其中,pB=p总×B的体积分数;若在T时平衡气体总压强为p总,则该反应Kp=_____。
⑤图2表示氢气转化率随温度变化的趋势,请解释T0后氢气转化率的变化原因__________。

(3)二甲醚燃料电池的工作原理如图所示,则X电极的电极反应式为__________。用该电池对铁制品镀铜,当铁制品质量增加12.8g时,理论上消耗二甲醚的质量为_________g。(精确到0.01)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、E的焰色反应均为黄色,其中B常用作食品的膨化剂,A与B按物质的量之比为1∶1混合并溶于足量水中,得到的溶液中只含有一种溶质。X为一种黑色固体单质,其氧化物参与大气循环,为温室气体。G为冶炼铁的原料,且为黑色晶体。G溶于盐酸中得到同种元素两种价态的化合物。A~H之间有如下的转化关系(部分物质未写出):

(1)写出下列物质的化学式:A___;C___;F___。
(2)在框图环境下,标准状况下得到11.2LD,则产生D的反应中,转移电子的物质的量为____mol。
(3)写出A+B→E的离子方程式:____。
(4)写出C和B混合加热过程中的全部化学方程式:___。
(5)写出D→G转化的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL稀盐酸。

回答下列问题:
(1)实验中观察到的现象是________________。
(2)产生上述现象的原因是________________。
(3)写出有关反应的离子方程式____________。
(4)由实验推知,MgCl2溶液和H2的总能量________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明反应A(s)+3B(g)![]() 2C(g)+D(g)已达平衡状态的是
2C(g)+D(g)已达平衡状态的是
A. B的物质的量浓度 B. 混合气体的密度
C. 混合气体的压强 D. v(B消耗)=3v(D消耗)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com