
下列叙述正确的是( )
| A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 |
| B.元素由化合态变成游离态时,它可能被氧化,也可能被还原 |
| C.元素的原子得失电子后,一定形成8电子的稳定结构 |
| D.有单质参加或生成的反应一定属于氧化还原反应 |
科目:高中化学 来源: 题型:单选题
氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应。用CuSO4溶液和“某物质”在40~50℃时反应可产生它。下列有关叙述中错误的是
| A.这“某物质”具有还原性 |
| B.CuH与盐酸反应,可能产生H2 |
| C.CuH与足量的稀硝酸反应:CuH + 3H+ + NO3—= Cu2++ NO↑+ 2H2O |
| D.CuH在氯气中燃烧:CuH + Cl2=" CuCl" + HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
工业上粗硅的生产原理为2C+SiO2 Si+2CO↑,下列说法正确的是
Si+2CO↑,下列说法正确的是
| A.SiO2是氧化剂 | B.SiO2发生氧化反应 |
| C.C表现出氧化性 | D.C被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用0.1 mol/L的Na2SO3溶液30 mL,恰好将2×10-3 mol XO4-还原,则元素X在还原产物
中的化合价是
| A.+4 | B.+3 | C.+2 | D.+1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3—→K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75 mol,则下列判断正确的是
| A.生成40.0 L N2(标准状况) |
| B.有0.250 mol KNO3被氧化 |
| C.转移电子的物质的量为1.25 mol |
| D.被还原的N原子的物质的量为3.75 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠
(Na2Cr2O7·2H2O),其主要反应:( )
①4FeO·Cr2O3+8Na2CO3+7O2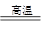 8Na2CrO4+2Fe2O3+8CO2 ②2Na2CrO4+H2SO4
8Na2CrO4+2Fe2O3+8CO2 ②2Na2CrO4+H2SO4 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法不正确的是( )
| A.反应①和②均为氧化还原反应 |
| B.Na2Cr2O7在碱性条件下可转化为Na2CrO4 |
| C.高温下,O2的氧化性大于Fe2O3和Na2CrO4的 |
| D.生成1 mol Na2Cr2O7时转移电子的物质的量大于7 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中能表明金属甲的活动性比金属乙的活动性强的是( )。
| A.在氧化还原反应中,甲失电子数比乙多 |
| B.同价态阳离子甲比乙氧化性强 |
| C.甲能跟盐酸反应放出H2而乙可与冷水反应产生H2 |
| D.甲、乙与H2SO4溶液形成原电池,乙上冒气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
200°C时,11.6克CO2和水蒸气的混合气体与足量的Na2O2充分反应后,固体的质量增加了3. 6克。从以上信息中,我们得出的下列结论中不正确的是( )
| A.可以计算出混合气体中CO2和水蒸气的质量 |
| B.可以判断出混合气体的平均摩尔质量 |
| C.可以计算出该反应中转移的电子数 |
| D.可以总结出Na2O2任何反应中既作氧化剂也作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一定条件下,分别以高锰酸钾、氯酸钾和过氧化氢为原料制取氧气,当制得同温同压下相同体积的氧气时,三个反应中转移的电子数之比为( )
| A.1:1:1 | B.2:2:1 | C.2:3:1 | D.4:3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com