
����Ŀ������������ˮ���۵�122.4�����е�248����ʵ�����üױ����������Һ��Ӧ������ʽΪC6H5��CH3+KMnO4![]() C6H5��COOK���Ƶñ�����أ�Ȼ�����ữ���Ƶñ����ᡣװ����ͼ��ʾ�����ּг�װ������ȥ����
C6H5��COOK���Ƶñ�����أ�Ȼ�����ữ���Ƶñ����ᡣװ����ͼ��ʾ�����ּг�װ������ȥ����

��1��ʵ��ʱ����1.84 g C6H5��CH3��4.5 g KMnO4����������ˮ��������ƿ���ý�����������Ŀ����________________________�����������ڣ��������е�ˮӦ��_____�������a����b������
��2������һ��ʱ���ֱ���ױ��㼸��������ʧ������Һ���ٳ������飬��ʱ��Ӧ���Һ��Ϊ��ɫ��ֹͣ���ȣ�����Һ©����������������������������Һ��ʵ������Ϊ________________________���÷�Ӧ��һ�ּһ���κͶ����������ɣ���ѧ����ʽΪ________________________���÷�Ӧ����������Ϊ__________���ѧʽ��������1 mol�����������ɣ�ת��_____mol���ӡ�
��3������Ӧ�������ȹ��ˣ�����Һ��ϴ��Һ��ϣ���ȴ����Ũ�����ữ��������Ӧ�Ļ�ѧ����ʽΪ��_____________________________��
��4����������ϴ�ӡ�������أ���1.71 g�����ᣬ��ʵ���б�����IJ���Ϊ_____%������һλС������
���𰸡���1��ʹ�����ܵļױ����������Һ��Ͼ��ȣ���߲��ʣ�2�֣� a��1�֣�
��2��ƿ����ɫ��ʧ��ͬʱ������ɫ������2�֣�
2KMnO4+3Na2SO3+H2O![]() 2MnO2��+3Na2SO4+2KOH��2�֣� Na2SO4��1�֣� 3��1�֣�
2MnO2��+3Na2SO4+2KOH��2�֣� Na2SO4��1�֣� 3��1�֣�
��3��C6H5��COOK+HCl(Ũ)![]() C6H5��COOH+KCl��2�֣�
C6H5��COOH+KCl��2�֣�
��4��70.1��3�֣�
����������1���ý����������Ŀ����ʹ�ױ����������Һ��Ͼ��ȣ���߲��ʣ�����ˮӦ�½��ϳ�����֤����Ч������2���������ƾ��л�ԭ�ԣ�����������������������Һ��Ϊ�˳�ȥ�����ĸ������������ʽΪ2KMnO4+3Na2SO3+H2O![]() 2MnO2��+3Na2SO4+2KOH�����ݻ��ϼ۱仯���÷�Ӧ����������ΪNa2SO4������1 mol�����������ɣ�ת��3 mol���ӡ���3������ǿ�������ᣬ�ɵ÷���ʽC6H5��COOK+HCl(Ũ)
2MnO2��+3Na2SO4+2KOH�����ݻ��ϼ۱仯���÷�Ӧ����������ΪNa2SO4������1 mol�����������ɣ�ת��3 mol���ӡ���3������ǿ�������ᣬ�ɵ÷���ʽC6H5��COOK+HCl(Ũ)![]() C6H5��COOH+KCl����4��1.84 g�ױ������ʵ���Ϊ0.02 mol��4.5 g KMnO4�����ʵ���Ϊ0.028 mol����KMnO4������Ӧ���ռױ��������м���������Ԫ���غ㣬1 mol�ױ���Ӧ1 mol�����ᣬ1.84 g�ױ���ȫ��ӦӦ����2.44 g�����ᣬ����1.71 g�����ᣬ��ʵ���б�����IJ���Ϊ
C6H5��COOH+KCl����4��1.84 g�ױ������ʵ���Ϊ0.02 mol��4.5 g KMnO4�����ʵ���Ϊ0.028 mol����KMnO4������Ӧ���ռױ��������м���������Ԫ���غ㣬1 mol�ױ���Ӧ1 mol�����ᣬ1.84 g�ױ���ȫ��ӦӦ����2.44 g�����ᣬ����1.71 g�����ᣬ��ʵ���б�����IJ���Ϊ![]() =70.1%��
=70.1%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪
Fe(s)��CO2(g)![]() FeO(s)��CO(g) K1 ��
FeO(s)��CO(g) K1 ��
Fe(s)��H2O(g)![]() FeO(s)��H2(g) K2 ��
FeO(s)��H2(g) K2 ��
H2(g)��CO2(g)![]() H2O(g)��CO(g)K3 ��
H2O(g)��CO(g)K3 ��
����֪��ͬ�¶��£�K1��K2ֵ���ұ���
�¶�/�� | K1 | K2 |
500 | 1.00 | 3.15 |
700 | 1.47 | 2.26 |
900 | 2.40 | 1.60 |
��1���жϷ�Ӧ���ﵽ��ѧƽ��״̬��������____________��
a����������ƽ��Ħ����������
b�����������c(CO)����
c��v(H2O)����v(H2)��
d������2 mol H��O����ͬʱ����1 mol H��H��
��2����500 ��ʱ���з�Ӧ����CO2��ʼŨ��Ϊ2 mol��L��1,2���Ӻ���ƽ�⣬��CO2ת����Ϊ________����CO��ʾ������Ϊ________________��
��3������ͼ���Ϸ�Ӧ������___________(�����)(ͼ��v�����ʣ���Ϊ�������H2������ٷֺ���)��

��4��900 �����з�Ӧ������ƽ�ⳣ��K3Ϊ____________(�������ֵ)���ʱ���H__________0(����>������������<��)�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ�������ﵽ�й�ʵ��Ŀ����
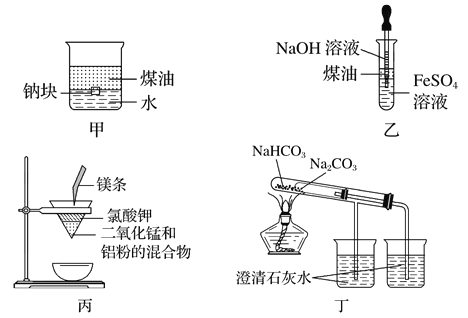
A. �ü�ͼװ��֤���ܶ���(ú��)����(��)����(ˮ)
B. ����ͼװ���Ʊ�Fe(OH)2
C. �ñ�ͼװ����ȡ������
D. �ö�ͼװ�ñȽ�NaHCO3��Na2CO3�����ȶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʢ����ˮ����֧�Թ��зֱ����ƾ������Ȼ�̼�ͱ������ã���������������ȷ�Ľ����ǣ�������

A. �ټ���CCl4 �ڼ��˱� �ۼ��˾ƾ�
B. �ټ��˱� �ڼ���CCl4 �ۼ��˾ƾ�
C. �ټ��˾ƾ� �ڼ���CCl4 �ۼ��˱�
D. �ټ��˱� �ڼ��˾ƾ� �ۼ���CCl4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ�������Ͻ��˵������ȷ���ǣ� ��
A. Ŀǰ�ҹ���ͨ��Ӳ�����ɺϽ���������
B. ���кϽ�����Ǿ��н�ǿ�Ŀ���ʴ����
C. þ�ڿ�����ȼ�շ���ҫ�۵İ⣬����������������
D. ��������Ʒ���渲��������Ĥ�����ڲ������𱣻�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ij��Һ����ˮ���������[H+]=1��10��5mol��L��1��������������ȷ����
A. һ���Ǽ���Һ
B. һ��������Һ
C. ��ˮ�������[OH��]=1��10��9mol��L��1
D. pHֵ����Ϊ9Ҳ����Ϊ5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���3�����ʵ��ܽ�ȣ�20�棩������˵���в���ȷ����
�� �� | MgCl2 | Mg��OH��2 | MgCO3 |
�ܽ�ȣ�g/100g�� | 74 | 0.00084 | 0.01 |
A. ����������������ˮ��ϣ����ȡ����գ����յĹ��������ͬ
B. ��ȥ�����к��е�MgCl2���ʣ���ѳ����Լ�ΪNaOH��Һ
C. ��֪MgCO3��Ksp=6.82��10��6mol2/L2�������к��й���MgCO3����Һ�У�����c��Mg2+��=c��CO32��������c��Mg2+����c��CO32����=6.82��10��6mol2/L2
D. ��ʯ��ˮ��������Mg2+��HCO3����Ӳˮ�����������ӷ�Ӧ����ʽΪ��
Mg2++2HCO3��+2Ca2++4OH��===2CaCO3��+Mg��OH��2��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ԭ�ӵ�������a g,12Cԭ�ӵ�������b g����NAֻ��ʾ�����ӵ���������ֵ��������˵������ȷ���ǣ�������
��1������ԭ�ӵ����ԭ������Ϊ![]() ��2��m g����ԭ�ӵ����ʵ���Ϊ
��2��m g����ԭ�ӵ����ʵ���Ϊ![]() mol
mol
��3������ԭ�ӵ�Ħ��������aNA g ��4��a g����ԭ�������ĵ�����Ϊ17NA
A. ��1����3�� B. ��1����2�� C. ��2����4�� D. ��2����3��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com