
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A. 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
B. 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
C. 18gD2O和H2O的混合物中含有的中子数为9NA
D. 12g石墨烯(单层石墨)中含有六元环个数为0.5NA
【答案】D
【解析】
A.室温下,1LpH=13的NaOH溶液中,c(OH-)=0.1mol/L,根据水的离子积常数可知,溶液中c(H+)=10-13mol/L。H+是由水电离产生,由于溶液的体积是1L,所以由水电离的OH-离子数目为10-13NA,A错误;
B.2molNO与1molO2充分反应会产生2molNO2,但NO2会又有一部分发生反应转化为N2O4,因此最后得到的气体分子数目小于2NA,B错误;
C.极端法求解。18g物质若全部是D2O,其物质的量是0.9mol,由于在1个D2O中含有10个中子,则0.9mol中含有中子数为9NA;若18g全为H2O,其物质的量是1mol,1个H2O中含有8个中子,则1molH2O中含有8 NA,故18gD2O和H2O的混合物中含有的中子数小于9NA,C错误;
D.在石墨的层状结构中,一个C原子形成3个六元环,每个六元环中含6个这种C原子,因此其中含有的C原子数为6×![]() =2,12g石墨烯含有1molC原子,则其中含有的六元环个数为0.5NA,D正确;
=2,12g石墨烯含有1molC原子,则其中含有的六元环个数为0.5NA,D正确;
故合理选项是D。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】把500 mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子的浓度为( )。
A.0.1(b-2a) mol·L-1B.10(2a-b) mol·L-1
C.10(b-a) mol·L-1D.10(b-2a) mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AlCl3溶液蒸干灼烧得不到无水AlCl3,而用SOCl2与AlCl3·6H2O混合共热可得到无水AlCl3,试用相关化学原理与必要的化学方程式进行解释。已知液态化合物SOCl2遇水剧烈反应,生成SO2和HCl两种气体。_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是化合反应,又是氧化还原反应的是( )
A.2CO+O2![]() 2CO2B.CaO+H2O=Ca(OH)2
2CO2B.CaO+H2O=Ca(OH)2
C.C+H2O![]() CO+H2D.CO2+Ca(OH)2=CaCO3↓+H2O
CO+H2D.CO2+Ca(OH)2=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Na+、NH4+、Fe3+、Al3+、SO42-等离子。向该溶液中滴加NaOH溶液,生成沉淀的物质的量变化曲线如图所示。下列有关判断正确的是 ( )
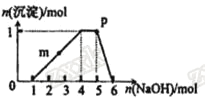
A.m点处反应:H++OH-=H2O
B.p点:c(OH-)>c(NH4+)>c(H+)
C.若取原溶液做焰色反应实验,焰色应为黄色
D.原溶液中存在的主要离子:n(H+)=2n(NH4+)=n(Al3+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L的密闭容器中,加入1molX和2molY发生反应:X(g)+2Y(g)![]() mZ(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入5molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是( )
mZ(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入5molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是( )
A. 两次平衡的平衡常数相同B. m=3
C. X与Y的平衡转化率之比为1:2D. 第二次平衡时,Z的浓度为0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从含溴化氢的废液中提取溴单质,下列说法中能达到实验目的的是( )
A.用装置 氧化废液中的溴化氢
氧化废液中的溴化氢
B.用装置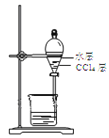 分离油层和水层
分离油层和水层
C.用装置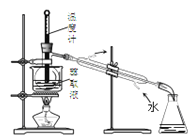 分离四氯化碳和液溴
分离四氯化碳和液溴
D.用仪器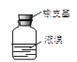 密封存放单质溴
密封存放单质溴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所示物质的制备方法合理的是
A.实验室从海帶中提取单质碘取样→灼烧→溶解→过滤→萃取→蒸馏
B.金红石(主要成分TiO2)为原料生产金属Ti:金红石、焦炭![]() TiCl4
TiCl4![]() Ti
Ti
C.从卤水中(溶质主要是MgCl2)提取Mg:卤水![]() Mg(OH)2
Mg(OH)2![]() MgCl2(aq)
MgCl2(aq) ![]() MgCl2(s)
MgCl2(s) ![]() Mg
Mg
D.由食盐制取漂粉精NaCl(ag) ![]() Cl2
Cl2![]() 漂粉精
漂粉精
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的“氧化物”样品,用5mol·L-1盐酸140mL恰好完全溶解,所得溶液还能吸收标准状况下0.56L氯气,使其中Fe2+全部转化为Fe3+,该样品可能的化学式是( )
A.Fe5O7B.Fe2O3C.Fe3O4D.Fe4O5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com