
【题目】下列过程属于物理变化的是
A.油脂酸败 B.空气液化 C.白酒变酸 D.粉尘爆炸
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】四种易溶于水的强电解质A、B、C、D由以下7种离子组成(电解质中阴离子各不相同)。
阴离子 | Na+ Ba2+ NH4+ |
阳离子 | CH3COO- Cl- OH- SO42- |
已知:①A、C溶液显碱性,A、B的溶液中水的电离程度相同;②C和D的溶液混合反应的现象只是有白色沉淀生成,B和C的溶液混合反应的现象只是有刺激性气味的气体生成,A和D的溶液混合无明显现象。
(1)A是__________,B是_____________。
(2)写出C与D的溶液反应的离子方程式_______________________。
(3)25℃时,0.1mol/LB溶液的pH=a,则B溶液中c(H+)—c(NH3·H2O)=_______________(用含有a的关系式表示)。
(4)将等体积、等物质的量浓度的B溶液和C溶液混合反应后溶液中各种离子浓度由大到小的顺序是______________________。
(5)向用盐酸中和后的C溶液中加入AgNO3和KBr,当两种沉淀共存时,c(Br—)/c(Cl—) =_________。(已知Ksp(AgCl) =2.0×10-10,Ksp(AgBr) =5.4×10-13)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用MnO2催化KClO3分解制取氧气要分离提纯回收其中的MnO2,正确的操作步骤是
A.溶解、过滤、蒸发 B. 溶解、过滤、结晶
C. 溶解、过滤、洗涤、干燥 D.溶解、结晶、干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家分获,以表彰他们在分子机器设计与合成领域方面的成就,其中一种光驱分子马达结构如右图所示。有关该分子的说法不正确的是

A. 光驱分子马达的分子式是C34H46O2,属于烃的含氧衍生物
B. 分子机器设计与合成的研究成果为未来新材料的研发开启了广阔前景
C. 三位科学家通过研究质子和中子重新合成了新的元素
D. 光驱分子马达能与NaHCO3和酸性KMnO4溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从化工厂铬渣中提取硫酸钠的工艺如下:
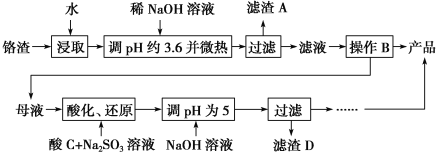
已知:①铬渣含有Na2SO4及少量Cr2O![]() 、Fe3+;
、Fe3+;
②Fe3+、Cr3+完全沉淀(c≤1.0×10-5mol·L-1)时pH分别为3.6和5。
(1)“微热”除能加快反应速率外,同时还可以________________________,滤渣A为________(填化学式)。
(2)根据溶解度(S)~温度(T)曲线,操作B的最佳方法为________(填字母序号)。
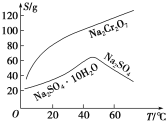
A.蒸发浓缩,趁热过滤
B.蒸发浓缩,降温结晶,过滤
(3)酸化后Cr2O![]() 可被SO
可被SO![]() 还原成Cr3+,离子方程式为_____________________;
还原成Cr3+,离子方程式为_____________________;
酸C为______________,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=____________。
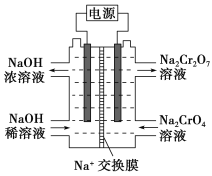
(4)根据2CrO![]() +2H+
+2H+![]() Cr2O
Cr2O![]() +H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的________极,其电极反应式为____________________________。
+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的________极,其电极反应式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)肼(N2H4)是火箭推进器中常用的高能燃料,已知0.4 mol液态肼和足量H2O2反应,生成N2和水蒸气,放出256. 65kJ的热量,请写出该反应的热化学方程式:__________。
(2)工业上制氢气的一个重要反应是:CO(g) +H2O(g)=CO2(g)+H2(g)
已知在25℃时:C(石墨)+![]() O2(g)=CO(g) △H1=-111kJ·mol-1
O2(g)=CO(g) △H1=-111kJ·mol-1
H2(g)+![]() O2(g)=H2O(g) △H2=-242 kJ·mol-1
O2(g)=H2O(g) △H2=-242 kJ·mol-1
C(石墨)+O2(g)=CO2(g) △H3=-394kJ·mol-1
试计算25℃时一氧化碳与水作用转化为氢气和二氧化碳反应的反应热△H=______kJ·mol-1
(3)CO2再在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与NaCO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol / L ,则生成沉淀所需CaCl2溶液的最小浓度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知碳单质的燃烧热为-393.5 kJmol-1,CO的燃烧热为-283kJmol-1,写出碳不完全燃烧生成CO的热化学方程式______________________________________。
(2)以CO为燃料,可以制成燃料电池。以CO为燃料,熔融碳酸盐为电解质的燃料电池正极通入的气体是_____________,负极的电极反应式____________________________。
(3)CO是汽车尾气之一,严重污染空气,在汽车上安装尾气处理器,发生反应:
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。
N2(g)+2CO2(g)。
现在固定容积为2L的密闭容器中通入NO和CO各2mol发生上述反应,随温度(T)、压强(P)和时间(t)的变化曲线如图所示。请回答下列问题:
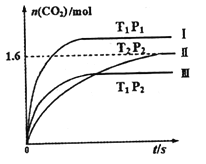
①曲线I、II、III对应反应从开始到平衡时用CO2表示的平均反应速率分别为V(I)、V(II)、V(III),则三者大小关系为______________。
②该反应△H__________0(填“>”、“=”或“<”);曲线II对应平衡常数K=_________;
曲线II对应的反应达平衡后,再通入2molNO和2molCO并保持温度不变,则再达平衡时NO的转化率将_______(填“增大”、“减小”或“不变”)。
③若维持温度为T2压强为P2的条件下,按下列四种方法改变起始物质的用量,达到平衡后,CO2的浓度为0.8 mol·L-1的是______________________________。
A.4mol NO+4 mol CO B.2 mol N2+2 mol CO2
C.1mol NO+1mol CO+1 mol N2+2 mol CO2 D.1mol NO+2mol N2+2 mol CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.HClO是弱酸,所以NaClO是弱电解质
B.CCl4可用于鉴别溴水和碘水
C.漂白粉在空气中不稳定,因此可用于漂白纸张
D.用乙醇萃取的方法可以分离溶于水的碘,是因为碘在乙醇中的溶解度较大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用铝片与稀硫酸反应制取氢气,以下能够加快该反应速率的是
①用浓硫酸代替稀硫酸②加热③改用铝粉④增大稀硫酸的体积⑤加水⑥加入少量硫酸铜
A.全部 B.②③⑥ C.①②③⑥ D.②③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com