
| A.硝基苯、苯、乙醇三种液体 |
B.硫酸 钠、硝酸钾、氯化钡三种固体 钠、硝酸钾、氯化钡三种固体 |
| C.硫磺、过氧化钠、氯化钙三种固体 |
| D.氯化铝、偏铝酸钠、烧碱三种固体 |
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源:不详 题型:实验题
 、乙两个充满氧气的密闭容器中各加入一定量的碳粉,在高温条件下使其充分反应,待反应结束后,两个容器中的碳粉都已完全消失。该小组成员对反应后两容器内气体进行如下探究:
、乙两个充满氧气的密闭容器中各加入一定量的碳粉,在高温条件下使其充分反应,待反应结束后,两个容器中的碳粉都已完全消失。该小组成员对反应后两容器内气体进行如下探究: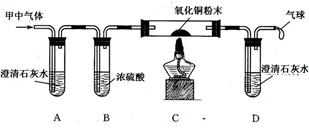
 行步骤2的实验,其理由是 。
行步骤2的实验,其理由是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
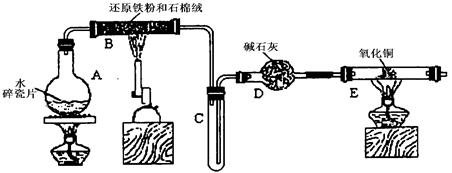
 Cu+Cu2++H2O,则可用来检验反应后E中的红色固体中除Cu外是否含Cu2O,可用的试剂是________(填序号)
Cu+Cu2++H2O,则可用来检验反应后E中的红色固体中除Cu外是否含Cu2O,可用的试剂是________(填序号)查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 骤,请排出正确的操作顺序:
骤,请排出正确的操作顺序:| A.NaOH放在纸上称量,且出现潮解现象 |
| B.配制前容量瓶内已有少量蒸馏水 |
| C.定容时仰视 |
| D.NaOH溶液未经冷却就转移到容量瓶中去 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 、转移、洗涤 ⑤定容、摇匀
、转移、洗涤 ⑤定容、摇匀| A.10ml | B.25ml | C.50ml | D.100ml) |

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。 |
| B.量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。 |
C.将酸式滴定管和碱式滴定管 用蒸馏水洗涤干净,并用各待盛溶液润洗。 用蒸馏水洗涤干净,并用各待盛溶液润洗。 |
| D.将物质的量浓度为1.50mol·L-1标准NaOH溶液装入碱式滴定管,调节液面记下读数V1。 |
| 滴定 序号 | 待测稀硫酸 的体积(mL) | 所消耗NaOH标准溶液液的体积(mL) | |
| V1 | V2 | ||
| ① | 20.00 | 0.50 | 22.60 |
| ② | 20.00 | 6.00 | 27.90 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 甲 | 100 mL 2.0 mol/L碳酸钠的溶液 200 mL 1.5 mol/L稀盐酸 | 盐酸逐滴加入到碳酸钠溶液中 |
| 乙 | 碳酸钠溶液逐滴加入盐酸到中 | |
| 丙 | 50ml 1.0mol/L氯化铝溶液 75ml 2.5mol/L氢氧化钠溶液 | 氯化铝溶液逐滴加入到氢氧化钠溶液中 |
| 丁 | 氢氧化钠 溶液逐滴加入到氯化铝溶液中 溶液逐滴加入到氯化铝溶液中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2CO3、BaCl2 | B.BaCl2、Na2CO3、H2SO4 |
| C.BaCl2、Na2CO3、HCl | D.Ba(NO3)2、Na2CO3、HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com