
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)该“84消毒液”的物质的量浓度约______mol·L-1(小数点后保留一位)。
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=______mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制80mL含NaClO质量分数为25%的消毒液。需要称量NaClO固体的质量为_______g。下列为打乱了的操作示意图,其正确排序为_______________________。
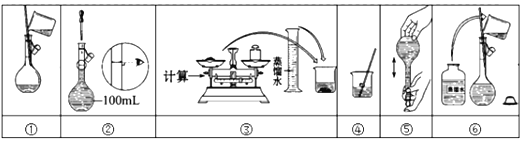
(4)配制过程中下列各项操作对消毒液物质的量浓度有和影响(填“偏小”、“偏大”或“无影响”)
A.用托盘天平称量 NaClO固体时,砝码生锈__________________。
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水____________________。
C.定容时,俯视容量瓶刻度线进行定容 ___________________。
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处___________。
【答案】4.0 0.04 29.8 ③④①⑥②⑤ 偏大 无影响 偏大 偏小
【解析】
(1)c=1000ρω/M=1000×1.19×25%/74.5mol·L-1≈4.0mol·L-1;
(2)稀释前后溶质的物质的量的不变,100×10-3×4=10000×10-3×c(Na+),解得c(Na+)=0.04mol·L-1;
(3)配制80mL溶液,需要用100mL的容量瓶,需要m(NaClO)=100×1.19×25%g=29.75g,因此需要称量NaClO固体的质量为29.8g;配制一定物质的量浓度的溶液的步骤是计算→称量→溶解→冷却→移液→洗涤→定容→摇匀,因此顺序是③④①⑥②⑤;
(4)A、称量时砝码生锈,药品的质量增大,所配溶液的浓度偏大;
B、容量瓶中有无水,对实验不产生影响,应填“无影响”;
C、定容时,俯视刻度线造成容量瓶中溶液的体积减小,浓度偏大;
D、定容摇匀后,发现低于刻度线,加入水补充,对原溶液稀释,浓度偏小;


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】实验室用氯酸钾和二氧化锰制取氧气的反应方程式为:2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
回答下列问题:
(1)该反应中被氧化的元素名称为______,生成1mol![]() 时转移电子的数目是______。
时转移电子的数目是______。
(2)从反应后的固体混合物中分离出难溶于水的![]() 的具体实验操作步骤:______。
的具体实验操作步骤:______。
(3)分离出的![]() 可用于实验室制取
可用于实验室制取![]() ,化学方程式为:MnO2+4HCl(浓)
,化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,其离子方程式为____。
MnCl2+Cl2↑+2H2O,其离子方程式为____。
(4)若两个反应中转移的电子的物质的量相同,则生成的![]() 和
和![]() 在相同状况下的体积比为____。
在相同状况下的体积比为____。
(5)以上两个反应都用到![]() ,其作用分别是 ______、_________。
,其作用分别是 ______、_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将潮湿的Cl2通过甲装置后,再通过放有干燥红色布条的 乙装置,红色布条不褪色,则甲装置中所盛试剂可能是

①浓硫酸 ②饱和食盐水 ③水 ④NaOH溶液
A. ①② B. ②③ C. ①④ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.100molL-1的盐酸滴定10ml0.100molL-1的Na2CO3溶液.溶液pH值与加入盐酸的体积的关系如图所示,已知室温时饱和CO2的pH为3.9,0.05molL-1NaHCO3的pH约为8.3,下列说法不正确的是
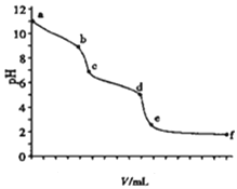
A. 以酚酞为指示剂,溶液颜色发生突变时(b点),Na2CO3转化为NaHCO3
B. 以甲基橙为指示剂,溶液颜色发生突变时,共消耗盐酸20.00ml
C. 溶液pH=7(c点),碳酸钠完全转化为NaCl
D. ce段对应溶液中CO2与NaHCO3共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。

(1)加入的试剂①为______(填化学式),加入试剂①的目的是______。
(2)操作a的名称为过滤、洗涤,所需要的玻璃仪器为______。洗涤固体B的操作是________。
(3)固体E的成分为_____,加入的试剂④为_____,发生的化学方程式为_________。
(4)从溶液D和溶液G中得到FeSO47H2O晶体的操作为______、______、______、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用锌粒与盐酸反应制取H2,下列措施不能提高该反应反应速率的是
A.用水将盐酸稀释B.用锌粉代替锌粒
C.适当提高盐酸浓度D.向反应液中滴入少量CuCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物(G)的合成路线如下:

已知:CH3(CH2)4Br![]() CH3(CH2)3CH2MgBr
CH3(CH2)3CH2MgBr
(1)G中所含的含氧官能团有________、__________(写官能团名称)。可以用________
仪器检测G中的官能团。
(2)A→B的过程中需加入K2CO3粉末,其主要作用是____________________。
(3)C→D的反应类型是______;在空气中久置,A可由白色转变为橙黄色,其原因是______。
(4)写出符合下列条件的A的一种同分异构体的结构简式:__________(只写一种)。
①能发生银镜反应,与FeCl3溶液能发生显色反应;
②除苯环外,含有3种不同的官能团;
③该分子核磁共振氢谱有5种不同的峰,且峰值比为1∶1∶2∶2∶2。
(5)写出以苯、乙醇为原料制备苯丙酮(![]() )的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:H2C=CH2
)的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH______。
CH3CH2OH______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实。2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g) 下列叙述错误的是
CH3CH2OH(g)+3H2O(g) 下列叙述错误的是
A. 使用Cu-Zn-Fe催化剂可大大提高生产效率
B. 反应需在300℃进行可推测该反应是吸热反应
C. 充入大量CO2气体可提高H2的转化率
D. 从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com