
【题目】某兴趣小组利用电解装置,探究“铁作阳极”时发生反应的多样性,实验过程如下。
I.KCl作电解质
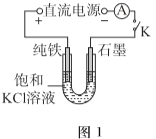
(1)一定电压下,按图-1装置电解,现象如下:
石墨电极上迅速产生无色气体,铁电极上无气体生成,铁逐渐溶解。
5min后U型管下部出现灰绿色固体,之后铁电极附近也出现灰绿色固体,10min后断开K。按图-2进行实验。
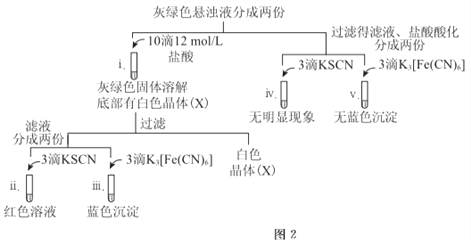
①石墨电极上的电极反应式是________。
②确认灰绿色固体中含有Fe2+的实验现象是_______。
③灼烧晶体X,透过蓝色钴玻璃观察到火焰呈紫色。结合平衡移动原理,解释“试管i中析出白色晶体”的原因是_______。
(2)其他条件不变时,用图-3装置重复实验,10min后铁电极附近溶液依然澄清,断开K。按图-4进行实验
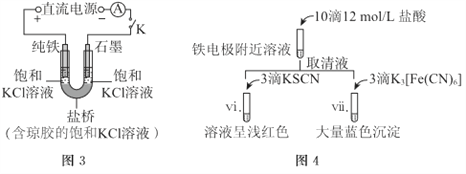
①盐桥的作用是_______。
②与实验I中vi、vii与ii~v中的现象比较,可以得出的结论是(答两点):_______。
II.KOH作电解质
(3)用图-1装置电解浓KOH溶液,观察到铁电极上立即有气体生成,附近溶液逐渐变为淡紫色(![]() ),没有沉淀产生。
),没有沉淀产生。
①铁电极上OH-能够放电的原因是______。
②阳极生成![]() 的总电极反应式是______。
的总电极反应式是______。
③某同学推测生成![]() 的必要条件是浓碱环境,将图-5中的实验方案补充完整,证实推测成立。
的必要条件是浓碱环境,将图-5中的实验方案补充完整,证实推测成立。
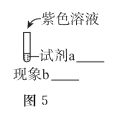 ______
______
【答案】 2H+ + 2e-= H2↑(或2H2O + 2e- = 2OH- + H2↑) 试管iii中生成蓝色沉淀,试管v中没有蓝色沉淀 试管i中存在溶解平衡:KCl(s) ![]() K+ (aq)+ Cl-(aq),滴加12 mol/L的盐酸, 增大c(Cl-),平衡逆向移动,析出KCl晶体 阻碍OH-向阳极迁移,避免灰绿色固体生成 本实验条件下铁在阳极区的产物主要为Fe2+ ,Fe2+在碱性条件下更容易被氧化为Fe3+ c(OH-)增大,反应速率加快(更容易放电) Fe -6e- + 8OH- = FeO42- +4H2O 水;生成红褐色沉淀和无色气体
K+ (aq)+ Cl-(aq),滴加12 mol/L的盐酸, 增大c(Cl-),平衡逆向移动,析出KCl晶体 阻碍OH-向阳极迁移,避免灰绿色固体生成 本实验条件下铁在阳极区的产物主要为Fe2+ ,Fe2+在碱性条件下更容易被氧化为Fe3+ c(OH-)增大,反应速率加快(更容易放电) Fe -6e- + 8OH- = FeO42- +4H2O 水;生成红褐色沉淀和无色气体
【解析】(1)①石墨电极为阴极,溶液中的氢离子放电生成氢气,电极反应式为2H+ + 2e-= H2↑(或2H2O + 2e- = 2OH- + H2↑),故答案为:2H+ + 2e-= H2↑(或2H2O + 2e- = 2OH- + H2↑);
②灰绿色固体用盐酸溶解后的溶液中加入铁氰化钾溶液,生成蓝色沉淀,灰绿色悬浊液过滤后的溶液中加入铁氰化钾溶液,无蓝色沉淀生成,说明灰绿色悬浊液中含有Fe2+,故答案为:试管iii中生成蓝色沉淀,试管v中没有蓝色沉淀;
③灼烧晶体X,透过蓝色钴玻璃观察到火焰呈紫色,说明含有钾元素,是因为试管i中存在溶解平衡:KCl(s) ![]() K+ (aq)+ Cl-(aq),滴加12 mol/L的盐酸, 增大c(Cl-),平衡逆向移动,析出KCl晶体,白色晶体为氯化钾晶体,故答案为:试管i中存在溶解平衡:KCl(s)
K+ (aq)+ Cl-(aq),滴加12 mol/L的盐酸, 增大c(Cl-),平衡逆向移动,析出KCl晶体,白色晶体为氯化钾晶体,故答案为:试管i中存在溶解平衡:KCl(s) ![]() K+ (aq)+ Cl-(aq),滴加12 mol/L的盐酸, 增大c(Cl-),平衡逆向移动,析出KCl晶体;
K+ (aq)+ Cl-(aq),滴加12 mol/L的盐酸, 增大c(Cl-),平衡逆向移动,析出KCl晶体;
(2)①盐桥中的氯离子代替氢氧根离子向阳极移动,避免灰绿色固体生成,故答案为:阻碍OH-向阳极迁移,避免灰绿色固体生成;
②根据实验I中vi、vii与ii~v中的现象比较可知,①vii中加入铁氰化钾溶液后生成大量蓝色沉淀,说明在使用盐桥的实验条件下铁在阳极区的产物主要为Fe2+ ,vi中溶液在加入KSCN溶液后呈浅红色,说明Fe2+在碱性条件下更容易被氧化为Fe3+,故答案为:本实验条件下铁在阳极区的产物主要为Fe2+ ;Fe2+在碱性条件下更容易被氧化为Fe3+;
(3)①c(OH-)增大,反应速率加快,使得铁电极上OH-能够放电,故答案为:c(OH-)增大,反应速率加快(更容易放电);
②阳极上生成的氧气能够将亚铁离子氧化生成FeO42-,反应的总电极反应式为Fe -6e- + 8OH- = FeO42- +4H2O,故答案为:Fe -6e- + 8OH- = FeO42- +4H2O;
③要推测生成FeO42-的必要条件是浓碱环境,只需要改变溶液的碱性,看是否仍然生成FeO42-即可,实验方案为:将淡紫色(FeO42-)溶液加入水中稀释,使溶液的碱性减弱,4FeO42-+10H2O4Fe(OH)3↓+8OH-+3O2↑,看到生成红褐色沉淀和无色气体,即可说明生成FeO42-的必要条件是浓碱环境,故答案为:水;生成红褐色沉淀和无色气体。


科目:高中化学 来源: 题型:
【题目】汽车的启动电源常用铅蓄电池,该电池在放电时的反应如下:Pb (s)+ PbO2(s) +2H2SO4(aq)![]() 2PbSO4(s) +2H2O(l),根据此反应判断下列叙述中正确的是
2PbSO4(s) +2H2O(l),根据此反应判断下列叙述中正确的是
A. PbO2是电池的负极 B. 铅蓄电池属于一次电池
C. 负极的电极反应式为:Pb(s)+SO42-(aq)–2e – = PbSO4(s) D. 电池放电时,溶液酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应在一定条件下的平衡转化率为25.3%,当使用了催化剂时,其转化率为( )
A. 大于25.3% B. 小于25.3% C. 等于25.3% D. 约等于25.3%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应发生在同种元素之间的是( )
A. Zn+2HCl![]() ZnCl2+H2↑
ZnCl2+H2↑
B. 2H2S+SO2![]() 3S↓+2H2O
3S↓+2H2O
C. H2+CuO![]() Cu+H2O
Cu+H2O
D. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备乙炔的电石渣对环境污染极为严重,因此需要对水体进行净化处理。现取500mL电石渣废水(阳离子主要为Ca2+),测定水质的数据如下表所示。

注:SS表示固体悬浮物
模拟工业处理流程如下:
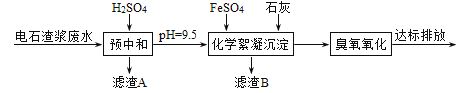
已知:i.常温时CaSO4微溶于水; ii.溶解度: CaSO4>Fe(OH)2>FeS。
(1)①采用20%的硫酸对废水进行预中和处理,pH变化如下图所示。硫酸的用量和废水中固体悬浮物(SS)含量的关系是_______。

②废水中SS含量随时间变化如下表所示。
静置时间(h) | 1 | 2 | 3 | 4 | 5 | 6 | 24 |
SS含量(mg/L) | 2500 | 1800 | 1300 | 900 | 820 | 800 | 780 |
为降低成本,减少硫酸投加量的最好办法是_______。
③滤渣A的主要成分有SS和_______。
(2)根据表中数据,回答下列问题。

①化学絮凝沉淀过程中,加入FeSO4发生反应的离子方程式是______。
②熟石灰能促进沉淀的生成,结合离子方程式,从平衡角度分析其原因是_______。
(3)用臭氧进一步处理废水中的氰化物和残留硫化物,若将500mL废水中的CN-完全氧化成N2和CO2,转移______mol e-。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成药物中间体M的流程如下。
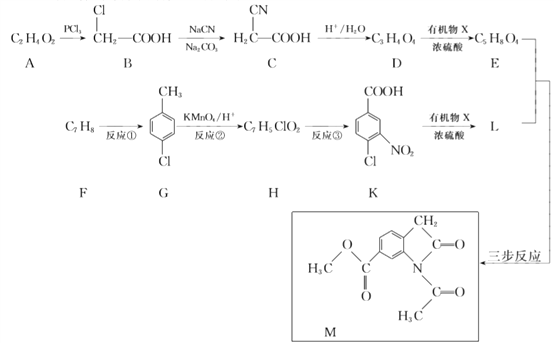
已知:
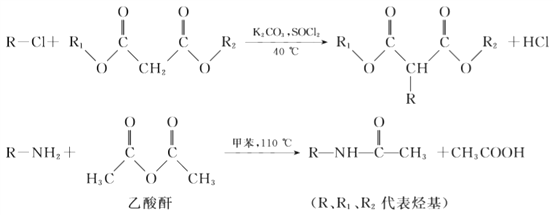
(1)A的名称是________。
(2)B中含有的官能团是________。
(3)D的结构简式是________。
(4)反应①的化学方程式是________。
(5)反应②的反应类型是________。
(6)反应③的试剂和条件是________。
(7)由K生成L反应的化学方程式是________
(8)
写出中间产物的结构简式: 中间产物Ⅰ ______ , 中间产物Ⅱ ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述中,不正确的是( )
A. 淀粉![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
B. 纤维素![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
C. 油脂![]() 甘油和高级脂肪酸
甘油和高级脂肪酸![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
D. 蛋白质![]() 氨基酸
氨基酸![]() 人体所需的蛋白质(人体生长发育)
人体所需的蛋白质(人体生长发育)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属及其合金的说法正确的是
A.在化学反应中,金属失电子,被还原
B.合金与各组分金属相比一般具有更低的熔点
C.生铁、普通钢和不锈钢中的碳含量依次增加
D.Fe2O3是磁铁矿的主要成分,属于碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: ①亚硝酸钠(NaNO2)是一种食品添加剂,为无色、无气味的同体,具有防腐和抗氧化作用。②AgNO2是一种微溶于水、易溶于酸的浅黄色固体。
I.问题探究
(1)人体正常的血红蛋白中应含Fe2+,误食亚硝酸盐(如NaNO2)会致使机体组织缺氧,出现青紫而中毒,原因是___________。若发生中毒时,你认为下列物质有助于解毒的是____(填字母)。
A.牛奶 B.Mg(OH)2 C.维生素C D.小苏打
(2)由于亚硝酸钠和食盐性状相似,曾多次发生过将NaNO2误当食盐食用的事件。要区别NaNO2和NaCl两种固体,你需用的试剂是_______________。
II.实验测定
为了测定某样品中NaNO2的含量,某同学进行如下实验:
①称取样品ag,加水溶解,配制成100mL溶液。
②取25.00mL溶液于锥形瓶中,用0.0200mol/LKMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液VmL。
(1)上述实验①所需玻璃仪器除玻璃棒、胶头滴管之外还有________。
(2)在进行滴定操作时,KMnO4溶液盛装在______(填“酸式”或“碱式”)滴定管中。当滴入最后一滴溶液,________时达到滴定终点。
(3)滴定过程中发生反应的离子方程式是________;测得该样品中NaNO2的质量分数为_____。
(4)若滴定管未用KMnO4标准溶液润洗就直接注入,则测定结果______(填“偏大”、“偏小”或“无影响”,下同);若滴定过程中刚出现颜色变化就停止滴定,则测定结果________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com