
【题目】焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生反应的体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和H2O。
(1)写出并配平该反应的方程式____;
(2)发生氧化反应的物质是___,反应中4mol的氧化剂能得到___mol电子;
(3)反应中产生了11.2L(标准状况)的气体时,被还原的物质的质量为___g;
(4)向NH4Cl溶液中滴加NaOH溶液并加热会放出气体,发生反应的离子方程式为_____。
【答案】4Fe2O3 +6NH4Cl![]() 2FeCl3+6Fe+3N2↑+12H2O NH4Cl 18 80 NH4++OH—
2FeCl3+6Fe+3N2↑+12H2O NH4Cl 18 80 NH4++OH—![]() NH3↑+H2O
NH3↑+H2O
【解析】
根据信息,用氯化铵除去铁锈,即氯化铵和Fe2O3为反应物,根据元素守恒,则N2、Fe、FeCl3、H2O为产物,NH4Cl中N的化合价由-3价→0价,Fe2O3中铁元素的化合价由+3价→0价,根据化合价升降法进行配平,据此分析;
(1)根据信息,用氯化铵除去铁锈,即氯化铵和Fe2O3为反应物,根据元素守恒,则N2、Fe、FeCl3、H2O为产物,得出Fe2O3+NH4Cl→N2+Fe+FeCl3+H2O,NH4Cl中N的化合价由-3价→0价,Fe2O3中铁元素的化合价由+3价→0价,根据化合价升降法进行配平,得出4Fe2O3+6NH4Cl ![]() 2FeCl3+6Fe+3N2↑+12H2O;
2FeCl3+6Fe+3N2↑+12H2O;
答案为4Fe2O3+6NH4Cl ![]() 2FeCl3+6Fe+3N2↑+12H2O;
2FeCl3+6Fe+3N2↑+12H2O;
(2)根据(1)的分析,N的化合价升高,NH4Cl为还原剂,发生氧化反应,该反应中Fe2O3为氧化剂,根据反应方程式,4molFe2O3参加反应时,其中有1molFe2O3没有参与氧化还原反应,3molFe2O3作氧化剂时,得到电子物质的量为3mol×2×3=18mol;
答案为NH4Cl;18;
(3)生成气体的物质的量为![]() =0.5mol,被还原的物质是Fe2O3,根据反应方程式,3molFe2O3被还原的同时有3molN2生成,即被还原的物质的量为0.5mol×160g·mol-1=80g;
=0.5mol,被还原的物质是Fe2O3,根据反应方程式,3molFe2O3被还原的同时有3molN2生成,即被还原的物质的量为0.5mol×160g·mol-1=80g;
答案为80g;
(4)向NH4Cl溶液中滴加NaOH溶液并加热,发生NH4++OH-![]() NH3↑+H2O;
NH3↑+H2O;
答案为NH4++OH-![]() NH3↑+H2O。
NH3↑+H2O。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】颠茄酸酯(H)有解除胃肠道痉挛、抑制胃酸分泌作用,常用于胃肠道平滑肌痉挛及溃疡病的辅助治疗,其合成路线如下:
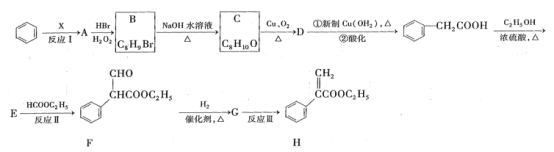
试回答下列问题:
(1)反应I所涉及的物质均为烃,氢的质量分数均为7.69%,A的相对分子量小于110,则A分子中最多有_______个碳原子在一条直线上。
(2)B的结构简式是_________________________。
(3)F中含有的官能团名称是____________________________。
(4)由C→D反应的化学方程式为___________________________________________。
(5)化合物G有多种同分异构体,同时满足下列条件的有________________种。
①能发生水解反应和银镜反应; ②能与FeCl3发生显色反应;
③苯环上有四个取代基,且苯环上一氯代物只有一种。
(6)参照上述合成路线,设计由 ![]() 制备
制备 ![]() 的合成路线为:___________
的合成路线为:___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50 s的平均速率为v(PCl3)=0.0032mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0mol PCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,近年来发现了一种新的星际分子,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键、三键等,颜色相同的球表示同一种原子)。
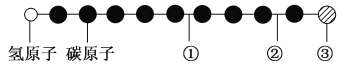
下列对该物质的说法中正确的是
A. ①处的化学键表示碳碳双键 B. ②处的化学键表示碳碳单键
C. ③处的原子可能是氯原子或氟原子 D. 此星际分子属于烃类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在容积为1L的密闭容器中充入![]() 和
和![]() 发生
发生![]() 测得
测得![]() 的物质的量随时间的变化如图所示,(已知,此温度下,该反应的平衡常数
的物质的量随时间的变化如图所示,(已知,此温度下,该反应的平衡常数![]() )下列说法正确的是 ( )
)下列说法正确的是 ( )
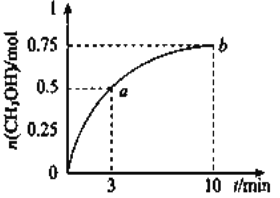
A. ![]()
B. 点b所对应的状态为化学平衡状态
C. ![]() 的生成速率,点a低于点b
的生成速率,点a低于点b
D. 欲增大平衡状态时![]() ,可保持其他条件不变,升高温度
,可保持其他条件不变,升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在氧化还原反应中,氧化剂__电子,发生的反应是__反应;还原剂__电子,发生的反应是__反应。铁与氯气反应的方程式为2Fe+3Cl2![]() 2FeCl3,生成物中铁是__价,铁与盐酸的反应式为___,生成物中铁是__价,这一事实证明,氯气的氧化性比盐酸的氧化性(填“强”“弱”)___。
2FeCl3,生成物中铁是__价,铁与盐酸的反应式为___,生成物中铁是__价,这一事实证明,氯气的氧化性比盐酸的氧化性(填“强”“弱”)___。
(2)0.6mol的氧气与0.4mol臭氧O3质量之比为___,分子个数之比为___,氧原子个数之比为___。
(3)现有一瓶A和B的混合液,已知它们的性质如下表。
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水 |
B | 17.9 | 290 | 1.26 |
据此分析,将A和B相互分离的常用方法是:___。
(4)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-按可能大量共存于同一溶液的情况,把他们分成A.B两组,而且每组中均含两种阳离子和两种阴离子。
A组:___;B组:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒酚是植物挥发油中的一种成分。关于胡椒酚的下列说法:
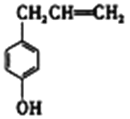
①该化合物属于芳香烃;
②分子中至少有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④1 mol该化合物最多可与2 mol Br2发生反应。
其中正确的是( )
A. ②③ B. ①②④ C. ①③ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组气体,不论以何种比例混合,其密度(同温同压)都不等于N2密度的是( )
A.O2和H2B.C2H4和COC.H2和Cl2D.CH4和C2H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com