
【题目】颠茄酸酯(H)有解除胃肠道痉挛、抑制胃酸分泌作用,常用于胃肠道平滑肌痉挛及溃疡病的辅助治疗,其合成路线如下:
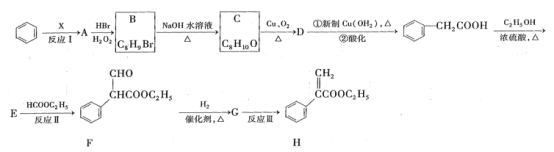
试回答下列问题:
(1)反应I所涉及的物质均为烃,氢的质量分数均为7.69%,A的相对分子量小于110,则A分子中最多有_______个碳原子在一条直线上。
(2)B的结构简式是_________________________。
(3)F中含有的官能团名称是____________________________。
(4)由C→D反应的化学方程式为___________________________________________。
(5)化合物G有多种同分异构体,同时满足下列条件的有________________种。
①能发生水解反应和银镜反应; ②能与FeCl3发生显色反应;
③苯环上有四个取代基,且苯环上一氯代物只有一种。
(6)参照上述合成路线,设计由 ![]() 制备
制备 ![]() 的合成路线为:___________
的合成路线为:___________
【答案】3 ![]() 醛基、酯基
醛基、酯基 ![]() 6
6 
【解析】
反应I所涉及的物质均为烃,氢的质量分数均为7.69%,烃A中含氢的质量分数为7.69%,当A的相对分子质量为110时,含有H原子数为:![]() =8.46,而烃A的相对分子质量小于110,故烃A分子中含H原子个数应大于6而小于8.46,只能为8,A的相对分子量为:
=8.46,而烃A的相对分子质量小于110,故烃A分子中含H原子个数应大于6而小于8.46,只能为8,A的相对分子量为:![]() ≈104,B分子中含有C原子数为:
≈104,B分子中含有C原子数为:![]() =8,所以A的分子式为C8H8,则X为C2H2,X结构简式为CH≡CH,A为
=8,所以A的分子式为C8H8,则X为C2H2,X结构简式为CH≡CH,A为![]() ,A与HBr发生加成反应生成B,根据D与新制Cu(OH)2加热条件下反应,酸化后得苯乙酸,D中含有醛基,则D的结构简式为:
,A与HBr发生加成反应生成B,根据D与新制Cu(OH)2加热条件下反应,酸化后得苯乙酸,D中含有醛基,则D的结构简式为:![]() ;C催化氧化生成E,则C的结构简式为:
;C催化氧化生成E,则C的结构简式为:![]() ;B水解生成C,则B的结构简式为:
;B水解生成C,则B的结构简式为:![]() ;苯乙酸与CH3CH2OH在浓硫酸加热条件下,发生酯化反应生成的E,则E的结构简式为
;苯乙酸与CH3CH2OH在浓硫酸加热条件下,发生酯化反应生成的E,则E的结构简式为![]() ,F与H2加成,醛基转化为羟基,则G的结构简式为:
,F与H2加成,醛基转化为羟基,则G的结构简式为:![]() ,G发生消去反应生成H。
,G发生消去反应生成H。
(1)A为![]() ,A分子中最多有3个碳原子在一条直线上;
,A分子中最多有3个碳原子在一条直线上;
(2)B的结构简式是![]() ;
;
(3)F为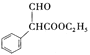 ,含有的官能团名称是醛基、酯基;
,含有的官能团名称是醛基、酯基;
(4)由C→D是苯乙醇在铜的催化下与氧气发生氧化反应生成苯乙醛和水,反应的化学方程式为![]() ;
;
(5)化合物G(![]() )有多种同分异构体.同时满足下列条件:与FeCl3溶液发生显色反应,含有酚羟基;能发生水解反应和银镜反应,含有甲酸形成的酯基;.苯环上有四个取代基,且苯环上一氯代物只有1种,符合条件的同分异构体有:
)有多种同分异构体.同时满足下列条件:与FeCl3溶液发生显色反应,含有酚羟基;能发生水解反应和银镜反应,含有甲酸形成的酯基;.苯环上有四个取代基,且苯环上一氯代物只有1种,符合条件的同分异构体有: 、
、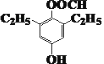 、
、、
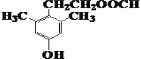 、
、 、
、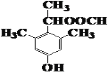 共6种;
共6种;
(6)由![]() 制备
制备![]() ,可用
,可用![]() 在氢氧化钠醇溶液中发生消去,再在双氧水条件下与溴化氢加成,再碱性水解、酯化可得
在氢氧化钠醇溶液中发生消去,再在双氧水条件下与溴化氢加成,再碱性水解、酯化可得![]() ,所以合成路线图为:
,所以合成路线图为: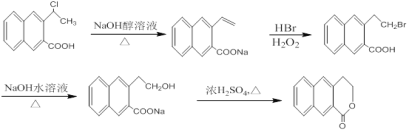 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图所示,从A处通入新制备的Cl2,关闭B阀时,C处的红色布条看不到明显现象;当打开B阀后,C处红色布条逐渐褪色。D瓶中装的是( )

①浓硫酸 ②NaOH溶液 ③H2O ④饱和NaCl溶液
A. ①③ B. ②④ C. ①② D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,Na、NaOH、NaHCO3分别与等物质的量的该物质恰好反应时,Na、NaOH、NaHCO3的物质的量之比为( )
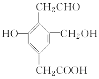
A. 3∶3∶2B. 3∶2∶1
C. 1∶1∶1D. 3∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】托盘天平、容量瓶、量筒是常见的中学化学计量仪器,熟知这些仪器的使用是定量研究化学的基础。
(1)其中标示出使用温度的仪器是________________。
(2)下列操作中,容量瓶所不具备的功能有________________ (填序号)。
A.配制一定体积准确浓度的标准溶液 B.贮存溶液
C.测量容量瓶规格以下的任意体积的溶液 D.准确稀释某一浓度的溶液
E.量取一定体积的液体 F.用来加热溶解固体溶质
(3)如图是某些仪器的刻度部分示意图,图中各仪器虚线为所示读数。其中为量筒的是________________ (填编号,),读数为_____mL。

(4)实验室用98%的浓硫酸配制(浓硫酸的密1.84g/mL)450mL 0.1 mol·L-1的硫酸。回答下列问题
① 配制中应选用的玻璃仪器有_________________,应量取________mL 98%的浓硫酸。
② 量筒在使用前已洗干净但不干燥,对结果是否造成影响________(填“是”或“否”),某同学认为将量筒内的浓硫酸倒出之后,应将量筒洗涤—下并将洗涤液倒入烧杯中,最后转移到容量瓶中,你认为他的做法______(填“对”或“错”)。
③对浓硫酸稀释过程中遇到下列情况,使所配制的硫酸浓度大于 0.1mol/L有 ______(填序号)
A.未经冷却趁热将溶液注入容量瓶中
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.容量瓶中原有少量蒸馏水
D.定容时俯视观察液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列叙述中正确的是
①106 g Na2CO3晶体中的离子总数大于3NA
②25 ℃、1.01×105 Pa下,14 g氮气所含的氮原子数为NA
③标准状况下,22.4LCCl4中所含的分子数约为6.02×1023
④标准状况下,aL的氧气和氮气的混合物含有的分子数约为![]() ×6.02×1023
×6.02×1023
⑤常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA
A.①②④B.②④⑤C.③④⑤D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数。下列说法中正确的是( )
A. 1molCl2与1molCH4恰好完全反应,则转移的电子总数为2NA
B. 15g甲基(—CH3)所含电子数为10NA
C. 2.8g ![]() 中含有的碳原子数为0.2n NA
中含有的碳原子数为0.2n NA
D. 标准状况下,2.24LCHCl3含有的分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 如图所示是分离混合物时常用的仪器,回答下列问题:
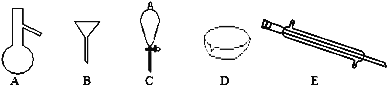
①写出仪器C、E的名称________________、________________。
②分离以下混合物应该主要选用上述什么仪器(填字母符号)
a.粗盐和泥沙:________ b.花生油和水___________。
(2)按照物质的树状分类和交叉分类,硫酸应属于___________。
①酸 ②能导电的纯净物 ③含氧酸 ④混合物 ⑤化合物 ⑥二元酸 ⑦电解质
A.①②③④⑦ B.①③⑤⑥⑦ C.①②③⑤⑥⑦ D.②③⑤⑥⑦
(3)往Fe(OH)3胶体中逐滴加入过量的3mol/L硫酸产生的现象是_______________________。
(4)现在有下列10种物质:① H2O ②空气 ③Mg ④ NH3 ⑤ 稀H2SO4⑥ Ca(OH)2 ⑦CuSO4 .5 H2O ⑧碘酒⑨无水乙醇⑩NaHCO3其中,⑤在水溶液中的电离方程式为______,属于电解质的是__________ (填序号,下同);属于非电解质的是__________ ;属于既不是电解质也不是非电解质的是__________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )
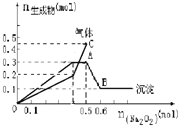
A. 1∶1∶2B. 2∶2∶1
C. 1∶2∶2D. 9∶2∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生反应的体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和H2O。
(1)写出并配平该反应的方程式____;
(2)发生氧化反应的物质是___,反应中4mol的氧化剂能得到___mol电子;
(3)反应中产生了11.2L(标准状况)的气体时,被还原的物质的质量为___g;
(4)向NH4Cl溶液中滴加NaOH溶液并加热会放出气体,发生反应的离子方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com