
����Ŀ��ij�����з���һ����ѧ��Ӧ����Ӧ�����д���H2O��ClO����CN����HCO3����N2��Cl���������ӣ��ڷ�Ӧ�����в��ClO����N2�����ʵ�����ʱ��仯��������ͼ��ʾ�������й��ж��в���ȷ���ǣ� �� 
A.��ԭ���Ǻ�CN�������ʣ��������ﲻֻ��N2
B.��������ClO�� �� ��ԭ������HCO3��
C.���뷴Ӧ���������뻹ԭ�������ʵ���֮��Ϊ5��2
D.��״����������2.24LN2��ת�Ƶ���1mol
���𰸡�B
���������⣺�����߱仯ͼ��֪���淴Ӧ����ClO�������ʵ������ͣ�N2�����ʵ�������ClO��Ϊ��Ӧ�N2����������ݵ���ת����ȿ�֪��CN���Ƿ�Ӧ�����Ԫ���غ��֪Cl�����������̼Ԫ���غ��֪HCO3�������������Ԫ���غ��֪H2O�Ƿ�Ӧ���Ӧ��ClԪ�ػ��ϼ���+1�۽���Ϊ��1�ۣ����ϼ��ܹ�����2�ۣ�CԪ�ػ��ϼ���+2������Ϊ+4�ۣ�NԪ�ػ��ϼ��ɩ�3������Ϊ0�ۣ����ϼ��ܹ�������С������Ϊ2[��4��2��+��3��0��]=10�ۣ���CN��ϵ��Ϊ2��ClO��ϵ��Ϊ5����Ԫ���غ��֪HCO3��ϵ��Ϊ2��N2ϵ��Ϊ1��Cl��ϵ��Ϊ5��H2Oϵ��Ϊ1����Ӧ����ʽΪ2CN��+5ClO��+H2O=2HCO3��+N2��+5Cl�� ��
A����Ӧ�У�CԪ�ػ��ϼ���CN����+2������ΪHCO3����+4�ۣ�NԪ�ػ��ϼ���CN���Щ�3������ΪN2��0�ۣ���֪����������HCO3����N2 �� ��A��ȷ��
B����Ӧ��ClԪ�ػ��ϼ���ClO����+1�۽���ΪCl���Щ�1�ۣ�ClO��������������ԭ������Cl�� �� ��B����
C��������������֪����ӦΪ2CN��+5ClO��+H2O=2HCO3��+N2��+5Cl�� �� ��Ӧ����CN���ǻ�ԭ����ClO�������������������뻹ԭ���Ļ�ѧ������֮��Ϊ5��2����C��ȷ��
D��2.24LN2����״���������ʵ���Ϊ0.1mol�����Բμӷ�Ӧ��ClO�������ʵ���Ϊ0.5mol����Ӧ��ֻ����Ԫ�ػ��ϼ۽��ͣ���ClO����+1�۽���ΪCl���Щ�1�ۣ�����ת�Ƶ���Ϊ0.5mol��2mol=1mol����D��ȷ��
��ѡB��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������20mL 0.01molL��l HNO2�����ᣩ��Һ����μ���һ��Ũ�ȵ��ռ���Һ����û����Һ���¶ȱ仯��ͼ��ʾ�������й�˵������ȷ���ǣ� ��
A.HNO2�ĵ���ƽ�ⳣ����c�㣾b��
B.b������Һ�����ԣ�c��Na+����c��NO2������c��H+����c��OH����
C.c������Һ�У�c��OH������c��HNO2��
D.d������Һ�У�c��Na+����c��OH������c��NO2������c��H+��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Ȼ��Ƶ�˵����ȷ����
A.�Ȼ��������Ȼ��Ʒ��ӹ��ɵ�B.Һ̬�����磬ˮ��Һ�ܵ���
C.��������̬�ܵ���D.�������Ӿ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ�����ʽ���ֶ�������ͼ������Ԫ�����ڱ���һ���֣��Ա���ѧ����Ԫ�����ڱ���������Ԫ�ص������ɣ��ж�����˵����ȷ���ǣ� �� 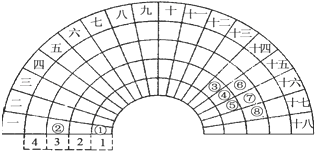
A.��Ԫ���γɵĵ��ʾ��������ԭ�Ӿ���
B.��Ԫ�ص���̬�⻯����Һ��������Ϊ����Ӽ�������
C.�ڡ��ߡ����Ӧ�ļ����Ӱ뾶���μ�С
D.�ڢݢ�����Ԫ���γɵ�����Һ��25��ʱ��pHֵΪ7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ����������������͵��ǣ���
A.ˮ��һ�ַdz��ȶ��Ļ�����
B.�����������������ʵ���У�����ʵ��ֵ���Ǵ���20
C.ˮ��ɱ���������ͣ��ܶȱ�С
D.��������Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȼ�ϵ�����Թ�������ﯡ�������Ϊ����ʣ����ֹ��������ڸ���������������(O2��)�����ͨ�����õ�صĹ���ԭ������ͼ��ʾ�����ж�缫a��b��������缫��Ӧ��

�����ж���ȷ����( )
A����O2�μӷ�Ӧ��a��Ϊ��صĸ���
B���������ĵ缫��ӦʽΪH2��2e����O2��===H2O
C��a����Ӧ�ĵ缫��ӦʽΪO2��2H2O��4e��===4OH��
D���õ�ص��ܷ�ӦʽΪ2H2��O2![]() 2H2O
2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɶ�����Ԫ����ɵ���ѧ�����ĺ���Ԫ�ص�����A��B��C��D��������ͼ1ת����ϵ������������ͷ�Ӧ��������ȥ���� 
��1����AΪ�����ƣ�A��ˮ��Ӧ�����ӷ���ʽΪ ��
��2����AΪ�������ƣ�A��ˮ��Ӧ�Ļ�ѧ����ʽΪ ��
��3��A������Na����Na2O2 �� ����ת����ϵ�ж�����D�� ��
��4����30mlijŨ�ȵ�B��Һ��ͨ��CO2��������ҺM����CO2ͨ�����IJ�ͬ����ҺM�����Ҳ��ͬ������M����μ���0.1mol/L���ᣬ����������V��CO2���������������V��HCl���Ĺ�ϵ����ͼ2��ʾ�������������CO2���ܽ⣩��������B����M�е�����Ϊ��ԭNaOH��Һ�����ʵ���Ũ��Ϊ��������A��B��֪������ʵ��ͨ���CO2�������Ϊ ��
��5��Na2CO3��NaHCO3Ũ�Ⱦ�Ϊ0.1mol/L�Ļ����Һ�У�����Ũ����С�����˳�����������һʵ��֤��Na2CO3��Һ���Ա�NaHCO3��Һ�ļ���ǿ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ԫ(C6H10O5)n��һ����Է��������ȵ��۸���Ķ��ǣ���Ҫ���ڸ���ͼ����У������ֽж�����ۺ��ǡ����й�����Ԫ˵����ȷ��(����)
A.��Ԫ�����ۡ���ά�ػ�Ϊͬ���칹��
B.��Ԫ����ۡ���ά������ͬϵ��
C.��Ԫˮ������ղ�����������
D.��Ԫ���л�ԭ�ԣ��ܷ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ��ʹ��������ƽ��ʳ��ʱ������Ľ�ʳ�η��������̣�����������������̣��Ƶ�ʳ�ε�����Ϊ15.5g(1g����ֻ��ʹ������)��.�������ȷ�ķ�����ʳ�ε�����ӦΪ
A. 15.5g B. 15.0g C. 14.5g D. 14.0g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com