
【题目】下图中,固体A是铁锈的主要成分。
![]()
请回答:
(1)白色沉淀E的化学式____________。
(2)写出A---B的化学方程式_____________________。
(3)写出C---D在溶液中发生氧化还原反应的离子方程式______________________。
【答案】 BaSO4 Fe2O3+3CO![]() 2Fe+3CO2 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
2Fe+3CO2 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
【解析】A是铁锈的主要成分,A为氧化铁,与一氧化碳反应生成单质铁和二氧化碳,铁与氯气反应生成氯化铁,所以固体C为氯化铁,氯化铁与二氧化硫和水反应生成硫酸亚铁,硫酸亚铁溶液中加入氯化钡生成白色沉淀硫酸钡,则E是硫酸钡。
(1)白色沉淀硫酸钡的化学式BaSO4,故答案为:BaSO4;
(2)一氧化碳还原氧化铁的化学方程式为:Fe2O3+3CO![]() 2Fe+3CO2,故答案为:Fe2O3+3CO
2Fe+3CO2,故答案为:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(3)氯化铁与二氧化硫与水反应生成硫酸亚铁,反应的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 熵增大的反应一定是自发反应 B. 焓增大的反应一定是自发反应
C. 熵、焓都为正值的反应是自发反应 D. ΔH-TΔS<0的反应一定是自发反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应热的叙述中正确的是
①已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为△H=-241.8 kJ·mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)![]() Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
④已知:
共价键 | C—C | C===C | C—H | H—H |
键能/(kJ·mol-1) | 348 | 610 | 413 | 436 |
上表数据可以计算出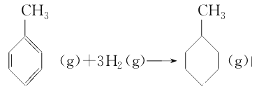 的焓变
的焓变
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1 mol CO2固体时,放出的热量相等
⑥25℃,101 kPa时,1 mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热
A.①②③④ B.③④⑤ C.④⑤ D.⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于平衡体系mA (g) +nB (g) ==C (g) +gD (g);△H <0,下列结论中错误的是
A. 若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q
B. 若温度不变,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小
C. 若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a
D. 若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m: n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空:
(1)氧化还原反应的本质是 , 通常可用元素化合价的升降来判断氧化剂、还原剂.所含元素化合价升高的物质是剂,发生反应.
(2)写出用稀氢氧化钠吸收氯气反应的离子方程式:
(3)0.1mol/L的Na2CO3溶液的含义是(填字母)
A.1L水中含有0.1mol Na2CO3
B.1L溶液中含有10.6g Na2CO3
C.将10.6g Na2CO3溶于1L水配成的溶液
D.1L溶液中含有0.2mol Na+
(4)关于钠及其化合物的叙述正确的是(填字母)
A.钠元素在自然界中都是以化合态存在
B.钠着火时可以用湿布盖灭
C.实验室少量的钠应保存在煤油或石蜡油中
D.实验中剩余的过氧化钠粉末可以用纸包裹好后,放入垃圾桶内
(5)下列反应的离子方程式书写不正确的是(填字母)
A.氯化钙溶液与碳酸钠溶液反应:Ca2++CO32﹣=CaCO3↓
B.氢氧化钡溶液与硫酸铜溶液反应:Ba2++SO42﹣=BaSO4↓
C.氢氧化镁与稀盐酸反应:Mg(OH)2+2H+=Mg2++2H2O
D.氢氧化钡溶液与盐酸的反应:OH﹣+H+=H2O
E.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag
F.碳酸钙溶于稀盐酸中:CaCO3+2H+=Ca2++H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I .合成氨工业在现代农业、国防工业中,有着重要的地位
己知:N2 (g) +3H2 (g) ![]() 2NH3 (g) △H=-92 kJ·mol-1
2NH3 (g) △H=-92 kJ·mol-1
(1)下列有关该反应速率的叙述,正确的是(选填序号)____________。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强不能增大活化分子百分数,但可以加快反应速率
c.使用催化剂可以使反应物分子平均能量升高,加快反应速率
d.在质量—定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
(2)对于合成氨反应而言,如图有关图象一定正确的是(选填序号) ______________。

II.向2L的密闭容器中充入7.6molNO和3.8mol O2,发生如下反应:
①2NO(g) + O2(g) =2NO2 (g) ②2NO2 (g) ==N2O4 (g)
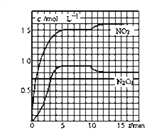
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃。
(1)计算前5min N2O4反应的平均速率为________________________。
(2)计算T1℃时反应②的化学平衡常数为_______________________。
(3)若起始时向该容器中充入3.6mol NO2和2.0mol N2O4,判断T1℃时反应②进行的方向_____(正向、逆向、不移动),并计算达到平衡时N2O4的物质的量为_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向恒温恒容密闭容器中充入气体A,发生反应:xA(g)![]() yB(g)+zC(g),各物质的浓度随时间的变化如下表所示。
yB(g)+zC(g),各物质的浓度随时间的变化如下表所示。
时间/s | c(A)/mol L-1 | c(B)/mol L-1 | c(C)/mol L-1 |
0 | 0.540 | 0 | 0 |
5 | 0.530 | 0.015 | 0.020 |
15 | 0.514 | 0.039 | 0.052 |
30 | 0.496 | 0.066 | 0.088 |
下列说法正确的是
A. x+y=3
B. 若起始时在容器中通入氦气,使容器压强增大,各物质反应速率均加快
C. 随着反应的进行,A的反应速率不断减慢,是因为该反应是吸热反应
D. 0~30 s内B的平均生成速率为2.2×10-3 mol L-1 S-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com