
【题目】甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,CO2 加氢合成甲醇是合理利用 CO2 的有效途径。由 CO2 制备甲醇过程可能涉及反应如下:
反应Ⅰ:CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH1=+41.19 kJ·mol-1
CO(g)+H2O(g) ΔH1=+41.19 kJ·mol-1
反应Ⅱ:CO(g)+2H2(g)![]() CH3OH(g) ΔH2
CH3OH(g) ΔH2
反应Ⅲ:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH3=-49.58 kJ·mol-1
CH3OH(g)+H2O(g) ΔH3=-49.58 kJ·mol-1
回答下列问题:
(1)反应Ⅲ的 ΔS_____(填“<”、“=”或“>”)0;反应Ⅱ的 ΔH2=_____。

(2)在恒压密闭容器中,充入一定量的 H2 和 CO2(假定仅发生反应Ⅲ),实验测得反应物在不同温度下,反应体系中 CO2 的平衡转化率与压强的关系曲线如图所示。
①比较T1与T2 的大小关系:T1_____T2 (填“ < ”、“= ”或“> ”) ,理由是:_____。
②在 T1 和 p6 的条件下,往密闭容器中充入 3 mol H2 和 1 mol CO2,该反应在第 5 min 时达到平衡,此时容器的体积为 1.8 L,则该反应在此温度下的平衡常数为_____。
a.若此条件下反应至 3 min 时刻,改变条件并于 A 点处达到平衡,CH3OH 的浓度随反应时间的变化趋势如图所示(3~4 min 的浓度变化未表示出来),则改变的条件为_____,请用 H2 的浓度变化计算从4 min 开始到A点的反应速率v(H2)=_____(保留两位小数)。
b.若温度不变,压强恒定在 p8 的条件下重新达到平衡时,容器的体积变为_____L。
【答案】 < -90.77 kJ·mol-1 < 反应Ⅲ为放热反应,温度降低,反应正向移动,所以 T1<T2 4/27 或 0.148 降低压强 0.08 mol·L-1min-1 8/15 或 0.533
【解析】
(1)气体物质的混乱度与分子数有关,分子数越大混乱度越大,反应III正反应气体分数目减小,所以混乱度减小,熵减小ΔS<0。根据盖斯定律,因为反应II=反应III反应I,所以ΔH2=-49.58kJ/mol-41.19kJ/mol=-90.77kJ/mol。
(2) 从CO2 的平衡转化率与压强的关系曲线图上看出,当压强相同时T1曲线的转化率大于T2曲线的转化率,说明T2→T1过程平衡向正反应方向移动,而反应III正反应是放热反应,根据勒夏特列原理,降低温度平衡向放热方向移动,所以T1<T2,答案:< 反应Ⅲ为放热反应,温度降低,反应正向移动,所以 T1<T2。
②由CO2 的平衡转化率与压强的关系曲线图知,T1和P6的条件下CO2的平衡转化率为40%,

此温度下平衡常数为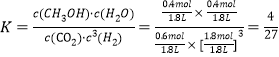 ;
;
a.由图像可知,改变条件达到平衡所用的时间大于5min,说明反应速率减慢,而且平衡时(A点)CH3OH浓度比原平衡(![]() )小,所以改变的条件只能是降低压强;由图像知第4min到A点甲醇浓度变化量Δc(CH3OH)=0.21mol/L-0.15mol/L=0.06mol/L,所以H2的变化浓度Δc(H2)=3Δc(CH3OH)=3×0.06mol/L=0.18mol/L,所以用H2表示的反应速率
)小,所以改变的条件只能是降低压强;由图像知第4min到A点甲醇浓度变化量Δc(CH3OH)=0.21mol/L-0.15mol/L=0.06mol/L,所以H2的变化浓度Δc(H2)=3Δc(CH3OH)=3×0.06mol/L=0.18mol/L,所以用H2表示的反应速率![]() ;
;
b.由图可知,T1和P8条件下CO2的转化率为60%,设此时容器容积为VL,因为温度不变平衡常数不变,K=![]() 。
。
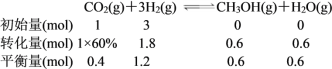
将数值代入平衡常数计算式中: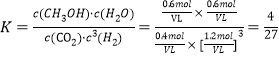 ,解得V=
,解得V=![]() 或0.533。
或0.533。


科目:高中化学 来源: 题型:
【题目】在一定温度时,将1 mol A和2 mol B放入容积为5 L的某密闭容器中发生反应A(s)+2B(g)![]() C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述中错误的是
C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述中错误的是
A. 在5 min内该反应用C的浓度变化表示的反应速率为0.02 mol/(Lmin)
B. 5 min时,容器内D的浓度为0.2 mol/L
C. 该可逆反应随着反应的进行,容器内压强逐渐增大
D. 5 min时,容器内气体总的物质的量为3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌电池是一种极具前景的电化学储能装置。VS2/Zn扣式可充电电池组成示意图如下。Zn2+可以在VS2晶体中可逆地嵌入和脱除,总反应为VS2+xZn![]() ZnxVS2。下列说法错误的是
ZnxVS2。下列说法错误的是

A. 放电时不锈钢箔为正极,发生还原反应
B. 放电时负极的反应为Zn-2e-== Zn2+
C. 充电时锌片与电源的负极相连
D. 充电时电池正极上的反应为:ZnxVS2+2xe-+xZn2+==VS2+2xZn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是未来非常理想能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O![]() 2H2+O2。制得的氢气可用于燃料电 池、合成氨工业。回答下列问题:
2H2+O2。制得的氢气可用于燃料电 池、合成氨工业。回答下列问题:
(1)分解海水时,__________能转变为_______________能。生成的氢气用于燃料电池时,___________能转变 为_____能。
(2)氢气可用于合成氨。一定温度下,向2L的密闭容器中加入1 molN2和3molH2 发生反应N2(g)+3H2(g)![]() 2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的
2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的![]() 。则前2min用NH3表示的化学反应速率为__________;平衡时,N2的转化率为_________。
。则前2min用NH3表示的化学反应速率为__________;平衡时,N2的转化率为_________。
(3)合成氨还需要大量的氮气为原料,工业上获得大量氮气的方法是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前我国主要采用硫酸法生产钛白(TiO2),每年产生至少100万吨钛白废液,其中含H2SO4约20%,还有少量Fe2+、TiO2+、Al3+。利用钛白废液浸出氧化锌生产七水硫酸锌,具有原料易得、工艺简单、回收率高和产品纯度高等优点。生产流程简化如下:

回答下列问题:
(1)“浸出”时发生的主要反应的离子方程式为_______。
(2)为寻找“浸出”的最佳条件,做9组对比实验得下表:
因素 | 温度/℃ | 反应时间/h | 固液比 | 产率/% |
1 | 70 | 2 | 1∶6.5 | 79.83 |
2 | 70 | 3 | 1∶7.5 | 86.18 |
3 | 70 | 4 | 1∶8.5 | 84.33 |
4 | 80 | 2 | 1∶7.5 | 83.06 |
5 | 80 | 3 | 1∶8.5 | 87.02 |
6 | 80 | 4 | 1∶6.5 | 95.38 |
7 | 90 | 2 | 1∶8.5 | 83.58 |
8 | 90 | 3 | 1∶6.5 | 88.95 |
9 | 90 | 4 | 1∶7.5 | 89.64 |
由表中数据可知,“浸出率”最高时的反应条件是_______。
(3)从生产实际考虑,调滤液的pH时选择加入石灰乳的原因是_______。
(4)常温下,按1:6固液质量比反应的浸出液中锌离子浓度最大值约为2.5mol/L,若Ksp[Zn(OH)2]=1.2×10-17,lg4.8≈0.68。则加入石灰乳调节的pH应不超过______(保留一位小数)。
(5)在加热下鼔入空气时,发生反应的化学方程式是___,此时TiO2+也会水解生成H2TiO3沉淀,发生反应的离子方程式为_____。
(6)加热下加入H2O2目的是进一步氧化除杂,氧化产物为__。抽滤得到的滤渣主要成分有___和H2TiO3(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把V L含有Na2SO4和MgSO4的混合溶液分成两等份,一份加入含a mol KOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钠离子的浓度为( )
A.2(2b-a)/V mol/LB.2(b-a)/V mol/LC.(2b-a)/V mol/LD.(b-a)/V mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向0.1mol·L-1NaA溶液中逐滴滴加盐酸,测得混合溶液的pH与p![]() 变化关系如图所示[
变化关系如图所示[![]() =-lg
=-lg![]() ]。下列说法正确的是
]。下列说法正确的是

A. a点溶液中c(Na+)=c(A-)
B. 电离常数K(HA)的数量级为10-4
C. 滴加过程中![]() 不断减小
不断减小
D. b点溶液中c(HA)>c(Na+)>c(A-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下把V体积氨气溶于1体积水中得到氨的饱和溶液,试完成下列填空。
(1)NH3通入水中发生的反应为____________________。
(2)氨水中存在的分子有__________________________。
(3)氨水中存在的离子有__________________________。
(4)所得氨水的质量分数为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。下面列出了几组物质,请将物质的合适组号填写在空格上。
A.金刚石与石墨;B.氕与氘;C.甲烷与戊烷;D.![]() 与
与 ;E.
;E.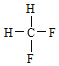 与
与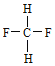 。
。
(1)同素异形体___;(2)同系物___;(3)同分异构体___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com