
【题目】按要求对下图中两极进行必要的联接并填空:
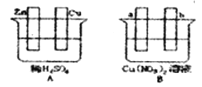
(1)在A图中,使铜片上冒H2气泡。请加以必要联接①______(在答题卡的图中画线),则联接后的装置叫②______。电极反应式:锌板:③_______;铜板:④_______。
(2)在B图中(a、b均为惰性电极),使a极析出铜,则b析出①______。加以必要的联接后,该装置叫②_____。电极反应式:a极:③_______b极:④___________。经过一段时间后,停止反应并搅均溶液,溶液的pH值⑤______(升高、降低、不变),加入一定量的⑥_____后,溶液能恢复至与电解前完全一致。
【答案】  原电池 Zn-2e- =Zn2+ 2H+ +2e-=H2↑ O2 电解池 Cu2++2e- =Cu 4OH--4e-=O2↑+2H2O 降低 CuO或者CuCO3
原电池 Zn-2e- =Zn2+ 2H+ +2e-=H2↑ O2 电解池 Cu2++2e- =Cu 4OH--4e-=O2↑+2H2O 降低 CuO或者CuCO3
【解析】(1)(1)在A图中,使铜片上冒H2气泡,说明氢离子在铜片得到电子,需要将锌铜之间连接导线,构成原电池,如图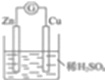 ;负极反应式为:Zn-2e- =Zn2+,正极反应为:2H+ +2e-=H2↑;(2)在B图中(a、b均为惰性电极),使a极析出铜,说明铜离子要在a电极上得到电子,a电极要与外电源的负极相连,b电极与外电源的正极相连,连接后的装置叫电解池,水(水的氢氧根离子)在b电极上失去电子生成氧气,电极反应式:a极:Cu2++2e- =Cu ,b极:4OH--4e-=O2↑+2H2O,经过一段时间后,停止反应并搅均溶液,溶液中氢离子浓度增大,pH值降低,加入一定量的CuO或者CuCO3后,溶液能恢复至与电解前完全一致。
;负极反应式为:Zn-2e- =Zn2+,正极反应为:2H+ +2e-=H2↑;(2)在B图中(a、b均为惰性电极),使a极析出铜,说明铜离子要在a电极上得到电子,a电极要与外电源的负极相连,b电极与外电源的正极相连,连接后的装置叫电解池,水(水的氢氧根离子)在b电极上失去电子生成氧气,电极反应式:a极:Cu2++2e- =Cu ,b极:4OH--4e-=O2↑+2H2O,经过一段时间后,停止反应并搅均溶液,溶液中氢离子浓度增大,pH值降低,加入一定量的CuO或者CuCO3后,溶液能恢复至与电解前完全一致。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】25℃时,向25mL 0.1000mo1·L-1 HA溶液滴加同浓度的BOH溶液,混合溶液pH随滴加BOH溶液的变化如下图所示。下列有关叙述错误的是
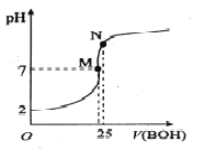
A. BA溶液呈碱性
B. 酸HA的电离常数约为0.0011
C. M点时c(B+)=c(A-)> c(H+)= c(OH-)
D. N点时加入10mL0.1mol/L HA溶液,将促进A-的水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10 mol·L-1盐酸分别滴定20.00 mL浓度均为0.10 mol·L-1 CH3COONa溶液和NaCN溶液,所得滴定曲线如右图(忽略体积变化)。下列说法正确的是

A. 溶液中阳离子的物质的量浓度之和:点②等于点③
B. 点①所示溶液中:c(CN—)+ c(HCN)=2c(Cl—)
C. 点②所示溶液中:c(Na+)> c(Cl-)> c(CH3COO-)> c(CH3COOH)
D. 点④所示溶液中:c(Na+)+ c(CH3COOH)+ c(H+)>0.10 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些物质的有关数据如下表,回答以下问题:
熔点(℃) | 沸点(℃) | 水溶性 | Ka1 | Ka2 | |||
乙醇 | -114.1 | 78.3 | 易溶 | 乙醇 | 2.6×10-16 | ||
乙醛 | -121 | 20.8 | 易溶 | H2SO3 | 1.23×10-2 | 5.6×10-8 | |
乙酸乙酯 | -83 | 77.0 | 难容 | H2CO3 | 4.2×10-7 | 5.6×10-11 |
实验一 乙醇在铜的催化下转化为乙醛
将一束质量为w的铜丝灼烧变黑后,迅速插入装有乙醇的试管a中。
(1)铜丝上可观察到的现象是______________,解释该现象的化学反应方程式为____________;
实验二 乙醛的提纯
上述实验获得的乙醛含有较多乙醇,可以通过以下操作提纯。

已知:CH3CHO+NaHSO3![]()
![]() (a-羟基乙磺酸钠)
(a-羟基乙磺酸钠)
(2)写出Na2CO3溶液参与反应的化学方程式:________________;
(3)某同学设计操作B的装置(夹持和加热装置已略去)如图所示。
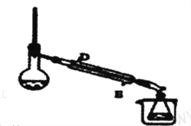
①冷凝管中的液体应从_____口进。(填“D”或“E”)
②下列有关操作与装置的分析,正确的是_____。(填字母)
a.烧杯中应装冰水 b.冷凝管应通温水 c.图示装置可用于除去乙酸乙酯中混有的乙醇
实验三 乙醛溶液浓度的测定
室温下利用反应Na2SO3+CH3CHO+H2O→CH3CH(OH)SO3Na↓+NaOH可以测定“实验一”中试管a内乙醛溶液浓度,操作如下:
取试管a中溶液4mL,加入1mL饱和Na2SO3溶液(过量),再加入5mL水,充分振荡后用pH计测定溶液pH;另取试管b,加入4mL乙醇做空白试验,实验结果如右表:
实验试管 | pH | ||
第一次 | 第二次 | 第三次 | |
A | 12.42 | 12.40 | 12.38 |
b | 10.43 | 10.43 | 10.40 |
(4)试管a中乙醛溶液的物质的量浓度为___mol/L。(列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质或应用正确的是( )
A.钠与硫酸铜溶液反应会置换出红色的铜
B.常温下干燥氯气与铁不反应,可以用钢瓶储存液氯
C.SO2具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色
D.普通玻璃的组成可用Na2OCaO6SiO2表示,是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖酸亚铁[(C6H11O7)2Fe2H2O]是重要的矿物质添加剂,它的吸收效果比无机铁盐好。一种工业上制备葡萄糖酸亚铁的工艺流程如下:
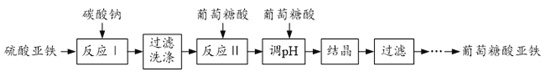
(1)反应Ⅰ的化学方程式为______。
(2)①碳酸亚铁过滤时需在表面保留水层的原因是______;
②检验FeCO3已经洗涤干净的操作为______。
(3)反应Ⅱ后加入葡萄糖酸调节溶液pH至5.8,其原因是______。
(4)葡萄糖酸亚铁溶液结晶、洗涤时均需加入乙醇,其目的分别是______,______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验装置和操作,回答有关问题。
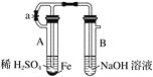
按图中所示装置,用两种不同的操作分别进行实验,观察B容器中的现象。
(1)先夹紧止水夹a,再使A容器中开始反应:①实验中B容器中观察到的现象是_________________;
②B容器中发生反应的离子方程式是____________________________________。
(2)打开止水夹a,使A容器开始反应一段时间后再夹紧止水夹a,①实验中观察到的现象是__________;②B容器中发生反应的离子方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学设计实验,完成Cu和 Fe2(SO4)3溶液的反应,用 KSCN 溶液检验是否还存在 Fe3+。
实验 I:

已知: i. Cu2+![]() CuSCN↓(白色) + (SCN)2(黄色)
CuSCN↓(白色) + (SCN)2(黄色)
ii. (SCN)2的性质与卤素单质相似
iii. CuSCN溶于稀硝酸,发生反应 CuSCN+HNO3==CuSO4+N2+CO2+H2O(未配平)
(1) 依据现象i可预测该反应的离子方程式为__________________________。
(2) 该小组同学查阅资料认为现象ii中的白色沉淀可能为CuSCN,设计实验进行验证。
实验II: 取少量实验I中的白色沉淀于试管中_______________________,证明该白色沉淀为CuSCN。(补充所加试剂及实验现象)
(3)该小组同学继续探究白色沉淀的成因,进行如下实验,
实验III:
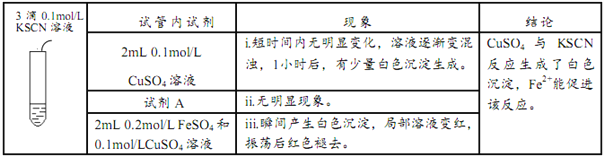
在实验III中:
①写出现象i中生成白色沉淀的离子方程式____________。
②试剂A为___________。
③根据现象iii结合化学用语及必要的文字解释Fe2+能加快沉淀生成的原因______。
(4)有的同学认为实验III不能充分证明其结论,并补充实验IV如下:
取2mL0.1 mol/L Fe2(SO4)3滴加3滴0.1mol/L KSCN溶液后,溶液变红,然后滴加2mL0.1mol/LCuSO4混合溶液于试管中, _____________________(现象)说明白色沉淀不是由Fe3+与SCN- 生成,且Fe3+不能加快CuSCN的生成。
(5)改变实验I铜的用量,设计实验V

该小组同学认为实验V中现象ii红色褪去与平衡移动有关,解释为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com