
【题目】氟及其化合物用途非常广泛。回答下列问题:
(1)基态锑(Sb)原子价电子排布的轨道式为____。[H2F]+[SbF6]—(氟酸锑)是一种超强酸,存在[H2F]+,该离子的空间构型为______,依次写出一种与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是_______、_________。
(2)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序_____(填元素符号)。
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为_____。
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在_______(填序号):
A 离子键 B σ键 C π键 D 配位键 E 范德华力
(3)某砷镍合金的晶胞如图所示,设阿伏加德罗常数的值为![]() ,该晶体的密度ρ_________g·cm-3。
,该晶体的密度ρ_________g·cm-3。
 。
。
【答案】![]() V形 H2O NH2 F>N>O>B sp3 ABD
V形 H2O NH2 F>N>O>B sp3 ABD ![]()
【解析】
(1)根据锑元素原子核外电子排布写出基态锑(Sb)原子价电子排布的轨道式;用价层电子对互斥理论判断[H2F]+的空间构型;用替代法书写与[H2F]+具有相同空间构型和键合形式的分子和阴离子;
(2)①同周期主族元素自左而右原子半径减小,第一电离能呈增大趋势;
②[B(OH)4]﹣中B的价层电子对=4+![]() (3+1-4×1) =4,所以采取sp3杂化;
(3+1-4×1) =4,所以采取sp3杂化;
③NH4BF4 (四氟硼酸铵)中含铵根离子和氟硼酸根离子,二者以离子键相结合;铵根离子中含3个σ键和1个配位键,氟硼酸根离子中含3个σ键和1个配位键;
(3)由晶胞结构可知,每个晶胞中含有2个Ni原子和2个As原子,计算晶胞的质量,晶胞的密度=![]() ;
;
(1)锑为51号元素,Sb 位于第五周期VA族,则基态锑(Sb)原子价电子排布的轨道式为![]() ;[H2F]+[SbF6]—(氟酸锑)是一种超强酸,存在[H2F]+,[H2F]+中中心原子F的价层电子对数为2+
;[H2F]+[SbF6]—(氟酸锑)是一种超强酸,存在[H2F]+,[H2F]+中中心原子F的价层电子对数为2+![]() =4,σ键电子对数为2,该离子的空间构型为V型,与[H2F]+具有相同空间构型和键合形式的分子为H2O、阴离子为NH2,
=4,σ键电子对数为2,该离子的空间构型为V型,与[H2F]+具有相同空间构型和键合形式的分子为H2O、阴离子为NH2,
故答案为:![]() ;V形; H2O;NH2;
;V形; H2O;NH2;
(2)①H3BO3和NH4BF4涉及的四种元素中第二周期元素是B、N、O、F四种元素,同周期元素从左向右第一电离能呈增大趋势,N的2p能级半充满较稳定,N的第一电离能大于O,则这四种元素第一电离能由大到小的顺序为F>N>O>B,
故答案为: F>N>O>B;
②[B(OH)4]﹣中B的价层电子对=4+![]() (3+1-4×1) =4,所以采取sp3杂化,
(3+1-4×1) =4,所以采取sp3杂化,
故答案为:sp3;
③NH4BF4 (四氟硼酸铵)中含铵根离子和氟硼酸根离子,二者以离子键相结合;铵根离子中含3个σ键和1个配位键,氟硼酸根离子中含3个σ键和1个配位键,铵根离子和氟硼酸根离子以离子键相结合,则四氟硼酸铵中存在离子键、σ键、配位键,
故答案为:ABD;
(3)由晶胞结构可知,每个晶胞中含有Ni原子数目=8×![]() +4×
+4×![]() =2,含有2个As原子,晶胞的质量=2×
=2,含有2个As原子,晶胞的质量=2×![]() g,晶胞的体积V=a×10-10cm×a×10-10cm×
g,晶胞的体积V=a×10-10cm×a×10-10cm×![]() ×c×10-10cm=
×c×10-10cm=![]() ×10-30cm3,故晶胞的密度ρ=
×10-30cm3,故晶胞的密度ρ=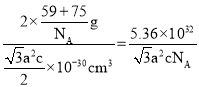 g·cm-3,
g·cm-3,
故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数。可供选用的试剂有:浓H2SO4、浓硝酸、6 mol·l-1NaOH溶液。

请填写下列空白:
(1)有关实验操作:a、往试管中放入适量的铝合金样品;b、从分液漏斗往试管中加入过量的A溶液;c、检查装置的气密性;d、测定收集到的水的体积。
正确的操作顺序为_________________________________________。
(2)A溶液可选用________________________________________
(3)若实验中测得样品的质量为W g ,氢气的体积为a L(标准状况),则样品中Al的质量分数为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计二氧化碳熔盐捕获及电化学转化装置,其示意图如下:

下列说法不正确的是
A. b为电源的正极
B. ①②中,捕获CO2时碳元素的化合价发生了变化
C. a极的电极反应式为2C2O52 4e == 4CO2 + O2
D. 上述装置存在反应:CO2 ===== C + O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,恒容密闭容器内某一反应体系中M、N的物质的量随反应时间变化的曲线如右图所示,下列叙述正确的是( )

A. 该反应的化学方程式为2M![]() N
N
B. t1时N的浓度是M浓度的2倍
C. t2时正、逆反应速率相等,反应达到平衡状态
D. t3时正反应速率大于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 有相同容积的定容密封容器甲和乙,甲中加入
有相同容积的定容密封容器甲和乙,甲中加入![]() 和
和![]() 各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
A.甲、乙提高相同温度 B. 甲中加入0.1mol He,乙不改变
C.甲降低温度,乙不变 D. 甲增加0.1mol ![]() ,乙增加0.1mol I2
,乙增加0.1mol I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量Cl2缓缓通入含0.02mol H2SO3和0.02mol HBr的混合溶液中。在此过程中溶液的pH与Cl2用量的关系示意图是(溶液体积变化忽略不计,且不考虑Cl2与水反应)
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某合金只含铝、铁、铜三种元素,取合金![]() ,加入到含
,加入到含![]() 稀硝酸的溶液中,恰好完全反应,放出无色气体
稀硝酸的溶液中,恰好完全反应,放出无色气体![]() 标准状况下
标准状况下![]() 。将反应后的溶液分成2等份,向一份溶液中滴加
。将反应后的溶液分成2等份,向一份溶液中滴加![]() ,无明显现象。向另一份溶液中滴加氨水至过量,过滤得沉淀bg,充分灼烧得固体
,无明显现象。向另一份溶液中滴加氨水至过量,过滤得沉淀bg,充分灼烧得固体![]() ,减轻了
,减轻了![]() ,再加入到过量的
,再加入到过量的![]() 溶液中,剩余不溶物
溶液中,剩余不溶物![]() 。下列说法不正确的是
。下列说法不正确的是![]()
![]()
已知:![]() 遇到
遇到![]() 会出现蓝色沉淀;
会出现蓝色沉淀; ![]()
A.![]()
B.原合金中铜的质量为![]()
C.若将上述![]() 稀硝酸逐滴加入到合金中,放出气体仍为
稀硝酸逐滴加入到合金中,放出气体仍为![]() 标准状况下
标准状况下![]()
D.d不是一确定值,可能为8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝及其化合物在生产生活中具有重要的作用。
(1)铝属于活泼金属却能在空气中稳定存在,原因是![]() 用化学用语及相关文字说明表达式为______
用化学用语及相关文字说明表达式为______
(2)下列实验能比较镁和铝的金属性强弱的是______![]() 填字母序号
填字母序号![]()
![]() 测定镁和铝的导电性强弱
测定镁和铝的导电性强弱
![]() 测定等物质的量浓度的
测定等物质的量浓度的![]() 和
和![]() 溶液的pH
溶液的pH
![]() 向
向![]() 和
和![]()
![]() 中加过量NaOH溶液
中加过量NaOH溶液
(3)冶炼金属铝时,用石墨做电极电解熔融______![]() 填化学式
填化学式![]() ,液态铝在______
,液态铝在______![]() 填“阴”或“阳”
填“阴”或“阳”![]() 极得到
极得到
(4)![]() 与
与![]() 在高温下反应可制得高温结构陶瓷氮化铝
在高温下反应可制得高温结构陶瓷氮化铝![]() ,且生成
,且生成![]() 。NaN3晶体中阴、阳离子个数比为______,写出反应化学方程式为______
。NaN3晶体中阴、阳离子个数比为______,写出反应化学方程式为______
(5)聚合铝![]() 是一种新型高效的无机高分子絮凝剂,广泛用于水的处理.用铝灰、铝土矿、铝渣等为原料
是一种新型高效的无机高分子絮凝剂,广泛用于水的处理.用铝灰、铝土矿、铝渣等为原料![]() 主要成分为Al、
主要成分为Al、![]() 可制取聚合铝.实验步骤如下:
可制取聚合铝.实验步骤如下:

①写出酸溶过程中发生的非氧化还原反应的离子方程式:______
②聚合铝![]() 的分子式为
的分子式为![]() ,聚合铝中
,聚合铝中![]() 与
与![]() 的比值对净水效果有很大影响,定义盐基度
的比值对净水效果有很大影响,定义盐基度![]() :
:![]() ,当
,当![]() 时,
时,![]() ______
______![]() 填入合适数字
填入合适数字![]()
③制取聚合铝的方法有多种,若将步骤I后的溶液pH直接调制![]() 时,将在过程④发生聚合而得到某种聚合铝
时,将在过程④发生聚合而得到某种聚合铝![]() ,写出生成该聚合铝的离子反应方程式是______
,写出生成该聚合铝的离子反应方程式是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z三种原子原子序数之和为25,且Z、Y原子序数之和是X的原子序数2倍还多![]() 已知它们可形成化合物
已知它们可形成化合物![]() 和
和![]() ,
,![]() 溶于水可与
溶于水可与![]() 反应生成一种化合物
反应生成一种化合物![]() ,下列有关分析不正确的是
,下列有关分析不正确的是
A.X、Y、Z在周期表中不可能处于同一周期
B.原子序数![]()
C.简单离子半径:![]()
D.Y单质在X单质中点燃生成物离子个数之比为1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com