
【题目】硼及其化合物在现代工业、生活和国防中有着重要的应用价值。
(1)最简单的硼烷是B2H6(乙硼烷),结构如图所示,其中B原子的杂化方式为________。

(2)三氯化硼和三氟化硼常温下都是气体,都有强烈的接受孤电子对的倾向。推测它们固态时的晶体类型为________;三氟化硼与氨气相遇,立即生成白色固体,写出该白色固体结构式,并标注出其中的配位键________。
(3)经结构研究证明,硼酸晶体中B(OH)3单元结构如图Ⅰ所示。各单元中的氧原子通过O—H…O氢键连结成层状结构,其片层结构及键长、层间距数据如图Ⅱ所示。层与层之间以微弱的分子间力相结合构成整个硼酸晶体。

①H3BO3是一元弱酸,写出它在水中的电离方程式(与氨类似)_____________________;
②根据结构判断下列说法正确的是________;
a.硼酸晶体有滑腻感,可作润滑剂
b.H3BO3分子的稳定性与氢键有关
c.含1 mol H3BO3的晶体中有3 mol氢键
d.H3BO3分子中硼原子最外层为8e-稳定结构
(4)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,图为其晶胞结构示意图。

①该功能陶瓷的化学式为________________;
②第一电离能介于B、N之间的第二周期元素有________种。
【答案】 sp3杂化 分子晶体 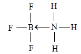 H3BO3+H2O
H3BO3+H2O![]() [B(OH)4]-+H+ ac BN 3
[B(OH)4]-+H+ ac BN 3
【解析】(1)根据每个硼原子含有4个共价键判断;
(2)根据常温下都是气体判断晶体类型;根据氮原子提供孤电子对,硼原子接受孤对电子分析;
(3)①根据与氨类似,进行迁移应用即可;
②根据硼酸晶体的结构特点分析解答;
(4)①根据均摊法计算该功能陶瓷的化学式;
②根据影响第一电离能大小的因素分析判断。
(1)乙硼烷分子中每个硼原子含有4个共价键,所以B原子采用sp3杂化;
(2)常温下为气体,说明晶体构型为分子晶体;硼元素具有缺电子性,其化合物可与具有孤电子对的分子或离子形成配合物,BF3能与NH3反应生成BF3NH3,B与N之间形成配位键,N原子含有孤电子对,所以氮原子提供孤电子对,BF3NH3结构式为: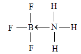 ;
;
(3)①硼酸为一元弱酸,在水溶液里,和水电离出的氢氧根离子形成配位键,其电离方程式为:H3BO3+H2O![]() [B(OH)4]-+H+;
[B(OH)4]-+H+;
②a.硼酸(H3BO3)是一种片层状结构白色晶体,片层状结构晶体有滑腻感,可作润滑剂,a正确;
b.分子的稳定性与分子内的B-O、H-O共价键有关,熔沸点与氢键有关,b错误;
c.1个硼酸分子形成了6个氢键,但每个氢键是2个硼酸分子共用的,所以平均含3个氢键,则含有1molH3BO3的晶体中有3mol氢键,c正确;
d.硼原子最外层只有3个电子,与氧原子形成3对共用电子对,因此B原子不是8e-稳定结构,d错误;
答案选ac;
(5)①根据原子半径大小知,B原子半径大于N原子,所以大球表示B原子,利用均摊法得B原子个数=1+8×1/8=2,N原子个数=1+4×1/4=2,B原子和N原子个数之比为2:2=1:1,所以其化学式为BN;
②同一周期元素中,元素的第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素,所以第一电离能介于B、N之间的第二周期元素有Be、C、O3种;


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与2.24LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入2 mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A. 60 mL B. 50 mL
C. 45 mL D. 15 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象或事实可用同一原理解释的是( )
A. 浓硫酸和浓盐酸长期暴露在空气中浓度降低
B. ![]() 能使溴水和品红溶液褪色
能使溴水和品红溶液褪色
C. ![]() 和
和![]() 溶液使酸性高锰酸钾溶液的紫色褪去
溶液使酸性高锰酸钾溶液的紫色褪去
D. 新制的氨水、氯水放置时间较久而变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列事实的解释正确的是( )
A. 蘸有浓硫酸和蘸有浓氨水的玻璃棒靠近没有白烟,说明硫酸与氨气不反应
B. 医疗上可用硫酸钡作X射线透视肠胃的内服药,是因为硫酸钡不溶于酸
C. ![]() 是还原性气体,浓
是还原性气体,浓![]() 是强氧化性物质,因此
是强氧化性物质,因此![]() 不能用浓
不能用浓![]() 作干燥剂
作干燥剂
D. 常温下,浓![]() 可以用铝制容器贮存,说明铝与浓硝酸不反应
可以用铝制容器贮存,说明铝与浓硝酸不反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将两份等质量的铝片,分别投入等物质的量浓度等体积的稀硫酸和氢氧化钠溶液中充分反应,消耗的铝的质量比为( )
A.1:1B.1:6C.2:3D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对反应A(s)+ 3B(g)![]() 2C(g)+ D(g)来说,下列反应速率最快的是
2C(g)+ D(g)来说,下列反应速率最快的是
A. v(A)=0.3 mol/(Ls) B. v(B)=0.6 mol/(Lmin)
C. v(C)=0.5 mol/(Lmin) D. v(D)=0.01 mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。

(1)起始时X的浓度为c(X)=________;反应从开始至2分钟末,Y的转化率为α(Y)=________;用Z的浓度变化表示0~2分钟内的平均反应速率为v(Z)=________。
(2)由图中所给数据进行分析,该反应的化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐中的碘以碘酸钾(KIO3)形式存在,可根据反应:IO3-+5I-+6H+═ 3I2+3H2O验证食盐中存在IO3-。根据上述反应,下列说法正确的是
A.IO3- 得电子,被氧化
B.I2 是氧化产物,H2O 是还原产物
C.该条件下还原性:I- > I2
D.每生成 3 mol I2,转移电子的物质的量为 6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若在已达到平衡的2SO2 + O2 ![]() 2SO3反应体系中,充入少量的18O2,一段时间后,18O这种原子存在于
2SO3反应体系中,充入少量的18O2,一段时间后,18O这种原子存在于
A. O2B. SO2C. SO3D. O2、SO2、SO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com